Σύστημα διασφάλισης ποιότητας σε οργανισμούς φαρμακείων. Δημιουργία συστήματος διαχείρισης ποιότητας φαρμάκων σε φαρμακείο
Αναζήτηση πλήρους κειμένου:
Αρχική > Περίληψη >Ιατρική, υγεία
φάρμακασε φαρμακειο
Διάταγμα του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας αριθ. οργανώσεις φαρμακείων. Βασικές Διατάξεις». Περιέχει Ενότητα IX Διασφάλιση Ποιότητας φάρμακα(φάρμακα) στα φαρμακεία.
Σε οργανισμούς φαρμακείων ή μεμονωμένους επιχειρηματίες, θα πρέπει να δημιουργηθεί ένα σύστημα διασφάλισης ποιότητας, το οποίο περιλαμβάνει:
εγκαταστάσεις και εξοπλισμός που αντιστοιχούν στο πεδίο των δραστηριοτήτων του φαρμακείου και επιτρέπουν τη διασφάλιση της συμμόρφωσης με τις προϋποθέσεις αποθήκευσης και παρασκευής φαρμάκων·
τεκμηρίωση που επιτρέπει τον προσδιορισμό της προέλευσης, της ποσότητας και της ποιότητας των εισερχόμενων φαρμάκων και την τήρηση αρχείων για τα αποθηκευμένα και πωλούμενα φάρμακα·
έλεγχος εισροών φαρμάκων που εισέρχονται στον οργανισμό φαρμακείου ή σε μεμονωμένο επιχειρηματία·
προσωπικό με τα απαραίτητα προσόντα·
Σύστημα συνεχούς εκπαίδευσης προσωπικού·
ένα ταμείο κανονιστικού και υλικού αναφοράς που θα πρέπει να παρέχεται σε όλες τις εγκαταστάσεις φαρμακείων ενός συγκεκριμένου οργανισμού φαρμακείου.
Ένας οργανισμός φαρμακείου πρέπει να σχηματίζει ένα σύστημα διαχείρισης ποιότητας για έναν οργανισμό φαρμακείου.
Κάθε οργανισμός φαρμακείου πρέπει να έχει εσωτερικούς κανονισμούς εργασίας εγκεκριμένους από τον επικεφαλής του οργανισμού, με ένδειξη εξοικείωσης των εργαζομένων. Αναθεώρηση των κανόνων και επανεξοικείωση των εργαζομένων του οργανισμού φαρμακείου με αυτούς πραγματοποιείται ετησίως.
Ο οργανισμός φαρμακείου πρέπει να διεξάγει τακτικά εσωτερικούς ελέγχους για τη συμμόρφωση με τις απαιτήσεις της GOST. Κατά τη διεξαγωγή επιθεωρήσεων, πρέπει να δίνεται προσοχή στην παρουσία στον οργανισμό φαρμακείου σχετικών εγγράφων για τις εγκαταστάσεις που καταλαμβάνονται, περιγραφές θέσεων εργασίας των εργαζομένων, πρότυπα και άλλα απαραίτητα έγγραφα.
Οι επιθεωρήσεις μπορούν να διενεργούνται τόσο από υπαλλήλους του φαρμακείου, ανεξάρτητα από τα άτομα που εμπλέκονται άμεσα στην ελεγχόμενη δραστηριότητα, όσο και από ανεξάρτητους εμπειρογνώμονες. Η συχνότητα των επιθεωρήσεων καθορίζεται από τον ίδιο τον οργανισμό του φαρμακείου. Τα αποτελέσματα των επιθεωρήσεων καταγράφονται και γνωστοποιούνται στο προσωπικό που είναι υπεύθυνο για την περιοχή εργασίας που επιθεωρείται και στη διεύθυνση του οργανισμού φαρμακείου. Οι επακόλουθες ανασκοπήσεις παρακολουθούν την εφαρμογή των συστάσεων και την αποτελεσματικότητά τους. Κάθε υπάλληλος του οργανισμού φαρμακείου πρέπει να είναι εξοικειωμένος με το GOST, τη διαδικασία εκπλήρωσης των καθηκόντων που του έχουν ανατεθεί, τις κανονιστικές νομικές πράξεις και τα πρότυπα που σχετίζονται με τις δραστηριότητες του οργανισμού. Στους οργανισμούς φαρμακείων, κάθε εργαζόμενος πρέπει να έχει εγκεκριμένες περιγραφές θέσεων εργασίας με τον κατάλληλο τρόπο.
Οι Φαρμακευτικοί Οργανισμοί θα πρέπει να προβλέπουν σύστημα συνεχούς επαγγελματικής εξέλιξης των εργαζομένων σε θέματα ισχύουσας νομοθεσίας, χρήσης φαρμάκων κ.λπ. Το σχέδιο και τα θέματα των μαθημάτων εγκρίνονται από τον επικεφαλής του οργανισμού φαρμακείου. Ο επικεφαλής του οργανισμού φαρμακείου διορίζει έναν ποιοτικό εκπρόσωπο από το διοικητικό προσωπικό.
Από αυτή την άποψη, δεν υπάρχει αμφιβολία η ανάγκη για συνεχή βελτίωση των επαγγελματικών δεξιοτήτων του φαρμακευτικού προσωπικού. Ένας από τους τρόπους επίλυσης αυτού του προβλήματος είναι η αύξηση της αποτελεσματικότητας του συστήματος μεταπτυχιακής εκπαίδευσης των φαρμακοποιών.
Ο οργανισμός φαρμακείου διασφαλίζει τη διατήρηση της τεκμηρίωσης σύμφωνα με νομοθετικές και κανονιστικές νομικές πράξεις Ρωσική Ομοσπονδία.
Πρώτα απ 'όλα, το καθήκον του φαρμακείου είναι να παρέχει τα διατηρημένα χαρακτηριστικά των αγαθών που λαμβάνονται από τον οργανισμό φαρμακείου. Αυτές είναι δύο ομάδες: λειτουργικές ιδιότητες - αποτελεσματικότητα και ασφάλεια, φυσικές και φυσικοχημικές, που απαιτούν συμμόρφωση με τους κανόνες για το χειρισμό τους. Ως μέρος του συστήματος διαχείρισης ποιότητας ενός οργανισμού φαρμακείου, κάθε φαρμακείο θα πρέπει να οργανώνει:
1. Έλεγχος αποδοχής. Πραγματοποιείται για την αποτροπή παραλαβής και πώλησης παραποιημένων, απορριφθέντων και κακής ποιότητας προϊόντων μέσω του δικτύου φαρμακείων. Ρυθμίζεται από το Βιομηχανικό Πρότυπο OST 91500.05.0007.-2003 "Κανόνες για την κυκλοφορία (πώληση) φαρμάκων σε οργανισμούς φαρμακείων." Οι ζώνες (εγκαταστάσεις) για την παραλαβή και τη χορήγηση φαρμάκων πρέπει να διαχωρίζονται από τον χώρο αποθήκευσης και πρέπει να παρέχουν επαρκή (αξιόπιστη) προστασία των παραληφθέντων φαρμάκων από τις κακές καιρικές συνθήκες κατά τις εργασίες φόρτωσης (εκφόρτωσης). Τα παραλαμβανόμενα προϊόντα υπόκεινται σε εισερχόμενο ποιοτικό έλεγχο. Τα αποτελέσματα του ελέγχου εισροών πρέπει να καταχωρούνται σύμφωνα με τα καθιερωμένα στο φαρμακείο εσωτερική τάξη. Στη διάρκεια εκφόρτωση προϊόντοςδιενεργεί έλεγχο για τη συμμόρφωσή του με την παραγγελία και την απουσία ζημιών σε συσκευασίες ή δοχεία. Φάρμακα και άλλα προϊόντα που επιτρέπονται προς πώληση από φαρμακευτικούς οργανισμούς που έχουν λήξει, δεν πληρούν τις απαιτήσεις ποιότητας, τα πρότυπα και χωρίς έγγραφα που πιστοποιούν την ποιότητά τους δεν υπόκεινται σε αποδοχή. Για φαρμακευτικά προϊόντα (φάρμακα) σε κατεστραμμένη συσκευασία, χωρίς πιστοποιητικά ή/και απαραίτητα συνοδευτικά έγγραφα, που απορρίφθηκαν κατά την αποδοχή ή τη χορήγηση στον ασθενή, όχι σύμφωνα με την παραγγελία ή με ληγμένη διάρκεια ζωής, συντάσσεται πράξη. πρέπει να φέρουν την κατάλληλη επισήμανση και να τοποθετηθούν σε καθορισμένο χώρο χωριστά από άλλα φαρμακευτικά προϊόντα μέχρι να αναγνωριστούν, να επιστραφούν στον προμηθευτή ή να απορριφθούν με τον προβλεπόμενο τρόπο. Δηλητηριώδεις και ισχυρές ουσίες, φάρμακα, ψυχοτρόπες ουσίες, θερμοευαίσθητα φάρμακα πρέπει να τοποθετούνται αμέσως σε χώρους αποθήκευσης σύμφωνα με τις απαιτήσεις της παρούσας OCTa.
Ο αριθμός των φαρμάκων που λαμβάνονται και απαιτούν ειδικές συνθήκες αποθήκευσης πρέπει να αντιστοιχεί στη διαθέσιμη χωρητικότητα του ειδικού εξοπλισμού. Τα αποδεκτά φαρμακευτικά προϊόντα και άλλα αγαθά που επιτρέπονται για διανομή από οργανισμούς φαρμακείων πιστώνονται εντός των προθεσμιών που έχουν καθοριστεί για την αποδοχή των προϊόντων ως προς τον αριθμό των εμπορικών μονάδων και την πληρότητα με τον καθορισμένο τρόπο. 6. Όλες οι αποστολές εμπορευμάτων πρέπει να συνοδεύονται από έγγραφα που επιτρέπουν τον καθορισμό της ημερομηνίας αποστολής, της ονομασίας του φαρμακευτικού προϊόντος (συμπεριλαμβανομένης της δοσολογικής μορφής και της δοσολογίας), του αριθμού παρτίδας και παρτίδας, της ποσότητας των προϊόντων που παραδόθηκαν, της τιμής του φαρμακευτικό προϊόν, το όνομα και τη διεύθυνση του προμηθευτή και του παραλήπτη, καθώς και έγγραφα που επιβεβαιώνουν την ποιότητα των φαρμάκων. Τα έγγραφα που επιβεβαιώνουν την ποιότητα των φαρμάκων είναι μια δήλωση συμμόρφωσης ή ένα πιστοποιητικό συμμόρφωσης Σημαντικός δείκτηςείναι επίσης ότι το φαρμακείο ή αλυσίδα φαρμακείωνσυνεργάζονται με έναν αξιόπιστο σύνδεσμο χονδρικής, γνωστές διεθνικές εταιρείες, που έχουν πολύ σοβαρά τη δική τους «υπηρεσία ασφάλειας ναρκωτικών».
Ο έλεγχος αποδοχής, μαζί με τον έλεγχο της ορθότητας της γραφειοκρατίας, περιλαμβάνει την επαλήθευση των φαρμάκων με όρους "Περιγραφή", "Συσκευασία", "Ετικέτα", η οποία καθορίζεται από τις απαιτήσεις της εντολής του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας 16.07.97. Νο 214 «Περί ποιοτικού ελέγχου φαρμάκων που παρασκευάζονται σε οργανισμούς φαρμακείων (φαρμακεία)». Ο έλεγχος σύμφωνα με την ένδειξη "Περιγραφή" περιλαμβάνει έλεγχο εμφάνισης, χρώματος, μυρωδιάς. Η ασυνέπεια στο χρώμα, η παρουσία ξένης οσμής, ίζημα, νιφάδες, μηχανικά εγκλείσματα, κατάψυξη, αποκόλληση αποτελούν λόγους απόρριψης. Σε περίπτωση αμφιβολίας για την ποιότητα των φαρμάκων, τα δείγματα αποστέλλονται στο περιφερειακό κέντρο ποιοτικού ελέγχου των φαρμάκων. Τέτοια φάρμακα με την ονομασία: «Απορρίφθηκαν κατά τον έλεγχο αποδοχής» φυλάσσονται στο φαρμακείο χωριστά από άλλα φάρμακα. Ο έλεγχος από τον δείκτη «Συσκευασία» περιλαμβάνει έλεγχο της ακεραιότητας της συσκευασίας, της παρουσίας δευτερεύουσας συσκευασίας και της συμμόρφωσης της συσκευασίας με τις φυσικές και χημικές ιδιότητες των φαρμάκων.
2. Χώροι και εξοπλισμός.Βασικές απαιτήσεις για την οργάνωση αποθήκευσης φαρμάκων και προϊόντων ιατρικό σκοπόστα φαρμακεία καθορίζονται με την Οδηγία από την οργάνωση αποθήκευσης στα φαρμακεία διαφορετικές ομάδεςφάρμακα και ιατρικές προμήθειες. Τα φαρμακευτικά προϊόντα που απαιτούν ειδικές συνθήκες αποθήκευσης θα πρέπει να ταυτοποιούνται αμέσως και να τοποθετούνται στο κατάλληλο μέρος αποθήκες (ζώνες)σύμφωνα με τις απαιτήσεις της ισχύουσας νομοθεσίας. Ο χώρος αποθήκευσης σε ένα φαρμακείο θα πρέπει να είναι αρκετά μεγάλος ώστε να επιτρέπει την τακτική αποθήκευση διαφορετικών κατηγοριών υλικών και προϊόντων. Καθαρό και προστατευμένο. Φάρμακα στην παραγωγή αποθήκεςπρέπει να αποθηκεύεται σε ράφια, παλέτες, βάθρα, ντουλάπια, ψύξη και άλλα ειδικός εξοπλισμόςγια τη διασφάλιση των συνθηκών αποθήκευσης των φαρμάκων σύμφωνα με τις ισχύουσες απαιτήσεις . Εάν η βάση του φαρμακείου (αποθήκη) διαθέτει ανοσοβιολογικά σκευάσματα, ο συνολικός όγκος του ψυκτικού εξοπλισμού πρέπει να διασφαλίζει, σύμφωνα με τις ισχύουσες απαιτήσεις, την αποθήκευση ολόκληρης της ποσότητας αυτών των φαρμάκων που περιέχεται στη βάση (αποθήκη). Κατά την αποθήκευση των φαρμάκων, ο κάτοχος της άδειας υποχρεούται να αποκλείει τη ζημιά τους (διαρροή, διαρροή, θραύση), μόλυνση από μικροοργανισμούς και διασταυρούμενη μόλυνση. Η αποθήκευση των φαρμάκων απαιτεί ειδικές συνθήκες θερμοκρασίας που ελέγχονται από συσκευές παρακολούθησης σταθερής θερμοκρασίας ή θερμικά δοχεία.
3. Προσωπικό. Όσον αφορά τους πόρους, ισχύει η τρίτη αρχή της διαχείρισης - αυτή είναι η συμμετοχή των εργαζομένων. Είναι οι εργαζόμενοι σε όλα τα επίπεδα που αποτελούν τη ραχοκοκαλιά του οργανισμού. Η πλήρης συμμετοχή τους επιτρέπει στον οργανισμό να αξιοποιήσει τις ικανότητές του. Αφενός, η διαχειριστική απόφαση της διοίκησης ότι το σύστημα διαχείρισης πρέπει να λειτουργεί, και αφετέρου, μόνο εάν όλο το προσωπικό αντιληφθεί ότι το σύστημα διαχείρισης δεν είναι απλώς μια συλλογή από πρόσθετα κομμάτια χαρτιού που θα σταθούν στο ράφι . Αυτή θα πρέπει να είναι μια αποτελεσματική δομή και θα λειτουργήσει μόνο όταν όλοι καταλάβουν σε τι βασίζεται και γιατί γίνεται. Σε κάθε φαρμακείο, με τη μία ή την άλλη μορφή, έχει δημιουργηθεί και λειτουργεί με επιτυχία ένα σύστημα διαχείρισης ποιότητας - για κάποιους κατά 10%, για άλλους κατά 90%.
4. ΤεκμηρίωσηΟι εργασίες που επηρεάζουν την ποιότητα των αγαθών θα πρέπει να περιγράφονται με γραπτές διαδικασίες. Το σύστημα διαχείρισης ποιότητας στοχεύει στη συστηματοποίηση των διαδικασιών, για να διαπιστωθεί εάν σε όλες παρέχονται οι απαραίτητοι πόροι και έγγραφα. Είναι σημαντικό να γνωρίζουμε εάν όλες οι διαδικασίες έχουν τεκμηριωμένες διαδικασίες και κανόνες εκτέλεσης. Απαιτείται η διαδικασία ανάλυσης και βελτίωσης προκειμένου να ληφθούν αποφάσεις διαχείρισης βασισμένες σε γεγονότα - αυτή είναι η έβδομη αρχή διαχείρισης των προτύπων ISO. Αποτελεσματική λύσημε βάση την ανάλυση δεδομένων και πληροφοριών.
7. Επιστροφές. Δεν επιτρέπεται η παρουσία σε κυκλοφορία φαρμάκων χαμηλής ποιότητας ή ψευδεπίγραφων, εξαιρουμένων αυτών των οποίων η ημερομηνία λήξης έχει παρέλθει. Έχοντας αποκαλύψει το γεγονός της παρουσίας φαρμάκων χαμηλής ποιότητας, πλαστών και παρόμοιων φαρμάκων, μια επιχειρηματική οντότητα πρέπει να συντάξει κατάλληλη πράξη και να λάβει μέτρα για τον αποκλεισμό τους από την κυκλοφορία. Ο αποκλεισμός από την κυκλοφορία τέτοιων φαρμακευτικών προϊόντων γίνεται με ανακύκλωση και καταστροφή σύμφωνα με τους Κανόνες για την Απόρριψη Φαρμακευτικών Προϊόντων. Η διαδικασία εργασίας με επιστολές από την Roszdravnador σχετικά με τα απορριφθέντα και παραποιημένα προϊόντα για τους ειδικούς του Κέντρου έχει αναπτυχθεί σύμφωνα με τις απαιτήσεις και με τις μορφές που καθορίζονται στην επιστολή Ομοσπονδιακή Υπηρεσίαγια την Υγειονομική Εποπτεία και κοινωνική ανάπτυξημε ημερομηνία 28.09.2004. αριθμ. 4082/04.
5. Βελτιστοποίηση του συστήματος διαχείρισης ποιότητας φαρμακευτικές δραστηριότητεςσε φαρμακειο
Ως αποτέλεσμα της μελέτης της βιβλιογραφίας σχετικά με τη διαχείριση ποιότητας των ιατρικών προϊόντων, μπορεί να προταθεί η βελτιστοποίηση των δραστηριοτήτων των φαρμακευτικών οργανισμών εισάγοντας τις ακόλουθες αρχές:
Η ποιότητα της διαχείρισης είναι μια πολύπλευρη έννοια, περιλαμβάνει πολλά στοιχεία, όπως: διαφάνεια και δυνατότητα ελέγχου των διαδικασιών, ποιότητα πληροφοριών, δυνατότητα λειτουργικού ελέγχου των τρεχουσών δραστηριοτήτων και πολλά άλλα. Ταυτόχρονα, διάφορα έγγραφα χρησιμεύουν ως πρακτικά το μόνο εργαλείο διαχείρισης. Έτσι, ο προφανής τρόπος αλλαγής της ποιότητας της διαχείρισης της επιχείρησης είναι η βελτίωση της αποτελεσματικότητας της εργασίας με έγγραφα.
Η διαχείριση της ποιότητας του φαρμακείου βασίζεται σε ακολουθώντας αρχές:
Επαρκής ποικιλία και όγκος προσιτές τιμές LS
Το καθήκον του φαρμακείου δεν είναι άλλο από το να παρέχει στον πληθυσμό φάρμακα και είδη φαρμακείουσε σωστό μέροςκαι σε ώρα βολική για τους επισκέπτες, για την οποία καθορίζονται οι ανάγκες, συντάσσεται ο προμηθευτής, γίνεται αίτηση, γίνεται αγορά, μελετάται η δοσολογία.
κοινωνική προσβασιμότητα
Διεξαγωγή έρευνας για το εύρος εντός συνωνύμων και αναλόγων. Υπάρχουν περισσότερες από μία εμπορικές ονομασίες μιας δραστικής ουσίας στο φαρμακείο. Οι εμπορικές ονομασίες μερικές φορές ποικίλλουν κατά 100–700%, ανάλογα με τον κατασκευαστή. Το φαρμακείο αγοράζει μια ποικιλία επωνυμιών με διαφορετικά επίπεδα για να εξασφαλίσει κοινωνική προσβασιμότητα σε διάφορους Κοινωνικές Ομάδεςεπισκέπτες. Σε μία φαρμακοθεραπευτική ομάδα, μπορείτε να πάρετε ακριβά, μεσαίου και χαμηλού κόστους φάρμακα.
Ενημερωτική και συμβουλευτική υποστήριξη
Οι εργαζόμενοι στα φαρμακεία πρέπει να προβλέπουν τις προσδοκίες του καταναλωτή και να διασφαλίζουν ότι το προϊόν ανταποκρίνεται σε αυτές τις προσδοκίες. Δεν είναι πάντα δυνατό. Για παράδειγμα, ένας καταναλωτής θέλει να λάβει συμβουλές από έναν φαρμακοποιό πριν αγοράσει ένα φάρμακο. Όμως ένας φαρμακοποιός δεν είναι γιατρός και δεν φέρει καμία νομική ευθύνη για την υγεία ενός ασθενούς στη χώρα μας. Ωστόσο, μη λαμβάνοντας το αναμενόμενο, ο καταναλωτής παραμένει δυσαρεστημένος.
Εφαρμογή υπολογιστικών συστημάτων στα φαρμακεία και χρήση barcodes στον ποιοτικό έλεγχο φαρμάκων στα φαρμακεία
Το σύστημα αυτοματισμού μιας επιχείρησης φαρμακείου διαφέρει από τα συστήματα αυτοματισμού των εμπορικών επιχειρήσεων. Τα φαρμακεία έχουν πολλές δικές τους ιδιαιτερότητες, που σχετίζονται κυρίως με την τιμολόγηση, η οποία στη Ρωσία ήταν πάντα μια πολύπλοκη και συγκεχυμένη διαδικασία. Η τιμολόγηση σε ένα φαρμακείο πραγματοποιείται σύμφωνα με ορισμένα νομοθετικά έγγραφα και ρυθμίζεται αυστηρά, υπάρχει κατάλογος φαρμάκων που δεν φορολογούνται. Για τέτοια φάρμακα, η λιανική τιμή διαμορφώνεται διαφορετικά. Παλαιότερα, για τους εργαζόμενους στα φαρμακεία, η διαδικασία παραλαβής αγαθών και καταχώρησης τιμών ήταν χρονοβόρα και χρονοβόρα. Επομένως, η αυτοματοποίηση είναι απλώς απαραίτητη εδώ.
Τα συστήματα αυτοματισμού επιτρέπουν στους εργαζόμενους στα φαρμακεία να βλέπουν δεδομένα σχετικά με το τι υπάρχει σε απόθεμα, ποια φάρμακα έχουν εξαντληθεί και τι πρέπει να αγοραστεί επιπλέον. Η διαδικασία γρήγορης προβολής πραγματικών υπολοίπων είναι μία από τις πιο σημαντικές κατά την επιλογή ενός συστήματος αυτοματισμού.
Σε κάθε συνηθισμένο φαρμακείο, όπου υπάρχει απλή ταμειακή μηχανή, όταν κάνουμε μια αγορά, τα χρήματα που πληρώνουμε στο ταμείο δεν σχετίζονται άμεσα με το προϊόν που λαμβάνουμε.
Και εδώ προκύπτουν αμέσως πολλά προβλήματα:
Πρώτον, το φαρμακείο δεν έχει πλήρη και λεπτομερή καταγραφή της κίνησης των αγαθών και των οικονομικών πόρων. Είναι αδύνατο, για παράδειγμα, να πούμε ανά πάσα στιγμή πόσο από ένα δεδομένο εμπόρευμα πουλήθηκε, πόσα έμεινε πάτωμα συναλλαγώνή σε μια αποθήκη, είναι αδύνατο να απαγορευθεί αυτόματα η διάτρηση εμπορευμάτων που έχουν ήδη τελειώσει κ.λπ.
Δεύτερον, είναι δύσκολο να αποφευχθούν τα λάθη που μπορεί να κάνει ο ταμίας.
Τρίτον, η έλλειψη λεπτομερούς λογιστικής καθιστά αδύνατη τη διεξαγωγή στατιστικών στοιχείων και τη λεπτομερή ανάλυση της δυναμικής των πωλήσεων, γεγονός που καθιστά δύσκολη την πιο ευέλικτη ανταπόκριση στις αλλαγές της ζήτησης.
6. Ανάλυση και τρόποι βελτίωσης του συστήματος διαχείρισης ποιότητας των φαρμάκων στο φαρμακείο της MAIR LLC
Η MAIR LLC δραστηριοποιείται στη φαρμακευτική αγορά για περισσότερα από 15 χρόνια στην Επικράτεια Primorsky. Το δίκτυο φαρμακείων του περιλαμβάνει 5 καταστήματα και είναι πολύ δημοφιλές - αρκετές χιλιάδες κάτοικοι του Βλαδιβοστόκ έχουν κάρτες συχνοί πελάτες. Καταλαμβάνει τον δεύτερο όροφο διώροφης οικοδομής. Το φαρμακείο είναι καινούργιο, λειτουργεί από τον Μάιο του 2010, πληροί όλες τις προϋποθέσεις επιστημονικής και τεχνικής τεκμηρίωσης και υγειονομικών προδιαγραφών, είναι ανοιχτό από τις 9:00 έως τις 20:00 επτά ημέρες την εβδομάδα. Υπάρχουν πινακίδες με το όνομα του φαρμακείου και τις ώρες λειτουργίας. Βρίσκεται σε βολικό σημείο για τους επισκέπτες, κοντά στη στάση του λεωφορείου.
Η Mair θεωρεί την κύρια αποστολή της όχι τόσο την πώληση φαρμάκων, την πώληση φαρμάκων και φαρμάκων, ιατρικών προϊόντων, αλλά την παροχή φαρμακευτικών υπηρεσιών σε υψηλό επίπεδοΩς εκ τούτου, η εταιρεία προσπαθεί να είναι πελατοκεντρική, να εγγυάται την ποιότητα των φαρμάκων και να εξυπηρετεί τον πελάτη όσο το δυνατόν καλύτερα. Όλα αυτά, μαζί με μια κατανοητή επιθυμία να κάνουν τη δουλειά τους πιο αποτελεσματική, έκαναν τη διοίκηση να σκεφτεί την εφαρμογή ενός συστήματος διαχείρισης ποιότητας.
Δουλεύοντας σε ένα σύστημα διαχείρισης ποιότητας για λιγότερο από ένα χρόνο, ένα φαρμακείο μπορεί να βγάλει κάποια συμπεράσματα. Οι αντικειμενικοί δείκτες επιβεβαιώνουν ότι η εισαγωγή ενός συστήματος διαχείρισης ποιότητας συνέβαλε στη βελτιστοποίηση του κεφαλαίου κίνησης: αυξήθηκε ο όγκος πωλήσεων στα φαρμακεία της αλυσίδας, μειώθηκε ο αριθμός των προϊόντων χαμηλού εισοδήματος και μη ρευστοποιήσιμων, καθώς και των ληγμένων προϊόντων. Ο αριθμός των τακτικών πελατών έχει αυξηθεί. Η ανάλυση της ζήτησης, των επιθυμιών και των προτάσεών τους κατέστησε δυνατή την ουσιαστική απαλλαγή από ελαττώματα. Επιπλέον, λόγω του προσανατολισμού του προσωπικού προς τη συνεργασία με πελάτες, όχι μόνο ο αριθμός των ηλεκτρονικών αγορών έχει αυξηθεί σημαντικά, αλλά μέσο κόστος. Οι ειδικοί στη διαχείριση ποιότητας σημειώνουν τώρα ότι ο κύριος και πιο προβληματικός κρίκος σε οποιαδήποτε δομή διαχείρισης είναι οι άνθρωποι. Στην περίπτωσή μας είναι φαρμακοποιοί. Αυτοί που βρίσκονται σε άμεση επαφή με πελάτες, επισκέπτες, καταναλωτές. Για την εισαγωγή ενός συστήματος διαχείρισης ποιότητας στο φαρμακείο, έγιναν κάποιες αλλαγές στην οργανωτική δομή και στις σχέσεις στην ομάδα. Ένα αποτελεσματικό σύστημα εκπαίδευσης προσωπικού και η συνεχής παρακολούθηση της εκπαίδευσης έχουν βελτιώσει την ποιότητα της εργασίας του προσωπικού.
Ως αποτέλεσμα της ανάλυσης δεδομένων από ξένη και εγχώρια βιβλιογραφία, διαπιστώθηκε ότι δίνονται τα ζητήματα του συστήματος διαχείρισης ποιότητας φαρμάκων σε φαρμακολογικά ιδρύματα τόσο στη Ρωσία όσο και στο εξωτερικό. μεγάλη προσοχή. Κατά τη μελέτη των βασικών εννοιών στην κατασκευή μοντέλων και τη λειτουργία συστημάτων διαχείρισης ποιότητας, προσεγγίσεις που βασίζονται στην έννοια της διαχείρισης ολικής ποιότητας (TQM) και στα πρότυπα της σειράς ISO 9000, τα οποία παρέχουν μια σειρά από γενικές αρχές: προσανατολισμός προς τον πελάτη, ηγεσία διαχείρισης, προσέγγιση επεξεργαστή, προσέγγιση συστήματος, συνεχής βελτίωση, αμοιβαία επωφελείς σχέσεις με προμηθευτές κ.λπ.
Το σύστημα διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων στη Ρωσία καθορίζεται από τον ομοσπονδιακό νόμο αριθ. βιομηχανικά πρότυπα: OST91500.05.0005-2002 "Κανόνες για το χονδρικό εμπόριο φαρμάκων. Βασικές διατάξεις", που εγκρίθηκε με εντολή του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 15ης Μαρτίου 2002 Αρ. 80. ΟΣΤ 91500.05.0007-2003.
Σύμφωνα με τη διεθνή πρακτική, το φαρμακείο είναι πλήρως υπεύθυνο για την ποιότητα των προϊόντων που αγοράζονται από προμηθευτές, μόνο οι υποχρεωτικές απαιτήσεις για τα προϊόντα καθορίζονται από το νόμο και όλοι οι άλλοι όροι διαπραγματεύονται σε συμφωνία μεταξύ των συμμετεχόντων στην αγορά.
Το σύστημα διαχείρισης ποιότητας στον τομέα της κυκλοφορίας φαρμάκων πρέπει να είναι αξιόπιστο, προληπτικό, να μην επιτρέπει την παροχή κατώτερων φαρμακευτικών υπηρεσιών στον καταναλωτή, καθώς και εξατομικευμένο, δηλ. έχει συγκεκριμένα άτομα υπεύθυνα για αυτό.
Θεωρούνται ορισμένες αρχές που επιτρέπουν τη βελτιστοποίηση του συστήματος διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων σε ένα φαρμακείο Μελετώντας τη βιβλιογραφία για τη διαχείριση ποιότητας των ιατρικών προϊόντων, είναι δυνατόν να προτείνουμε τη βελτιστοποίηση των δραστηριοτήτων των φαρμακευτικών οργανισμών εισάγοντας τις ακόλουθες αρχές.
ΒΙΒΛΙΟΓΡΑΦΙΑ
Διάταγμα του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 03/04/2003. Αρ. 80 «Περί έγκρισης του βιομηχανικού προτύπου «Κανόνες για τη διανομή (πώληση) φαρμακευτικών προϊόντων σε οργανισμούς φαρμακείων. Βασικές Διατάξεις».
Skulkova R.S., Yagudina R.I., Parkhomenko D.V. Διαμόρφωση συστήματος διαχείρισης ποιότητας για οργανισμούς φαρμακείων. Νέο φαρμακείο. Κανονισμοί. 2005.-Ν 4.-Σ.32-37 .
Komissinskaya I. G. Σύγχρονη έννοιαδιαχείριση ποιότητας ενός οργανισμού φαρμακείου // Moskovskie apteki. - 2007. - Νο. 11.
Alferova, T.V. Διαχείριση παραγωγής στις επιχειρήσεις της φαρμακευτικής βιομηχανίας / T.V. Alferova, E.A. Tretyakova, A.V. Buylin. - Αικατερινούπολη: Εκδοτικός Οίκος του Ινστιτούτου Οικονομικών Επιστημών του Παραρτήματος Ουραλίων της Ρωσικής Ακαδημίας Επιστημών, 2008. - 214σ.
Moskvin V.A. Εξέλιξη στον τομέα της διαχείρισης ποιότητας / V.A. Moskvin // Investments in Russia.2004. Νο. 5.- Σ. 27-28.
Lagutkina T.P. Π αρχές διαχείρισης ποιότητας στις δραστηριότητες ενός οργανισμού φαρμακείου // Δελτίο του Πανεπιστημίου Φιλίας των Λαών της Ρωσίας. 2008.-Ν 4.-Σ.36-39.
Polessky V.A. Εξέλιξη μοντέλων συστημάτων ποιότητας: διεθνής πρακτική / V.A. Polessky, S.A. Martynchik, V.G. Zaporozhchenko, V.Z. Kucherenko // Οικονομικά της Υγείας. - 2005. - Νο. 8. - Σ. 25-36.
ο ομοσπονδιακός νόμος"On Medicines" No. 86-FZ με ημερομηνία 22/06/98
Drugova Z.K., Biteryakova A.M. Σύστημα εσωτερικού ελέγχου και ποιότητα διαχείρισης // Ρωσικά φαρμακεία. - Νο 2. – 2007.
Kononova S.V. Σύστημα για τη διασφάλιση της ποιότητας των φαρμακευτικών υπηρεσιών στο περιφερειακό φαρμακευτικό συγκρότημα: Μονογραφία. -Νίζνι Νόβγκοροντ: Εκδοτικός Οίκος VGIPA, 2003.
Συνθήκες αποθήκευσης φαρμάκων. - Μ.: Ιατρική, 2006. - 184 σελ.
Kulaev V.A. Egorov V.A., Gladunova E.P., Ezhkov V.N. Ολοκληρωμένο σύστημα διαχείρισης ποιότητας για τη φαρμακευτική φροντίδα // Pharmacy, 2011, No. 3, C. 30-33
SEI HPE "PERM ΚΡΑΤΙΚΗ ΦΑΡΜΑΚΕΥΤΙΚΗ ΑΚΑΔΗΜΙΑ"
Τμήμα Διοίκησης και Οικονομίας Φαρμακευτικής FDPO και FZO
Επαναληπτικά μαθήματα για εξωσχολικές σπουδές
χρήση τεχνολογιών εξ αποστάσεως στην ειδικότητα «Διοίκηση και Οικονομία της Φαρμακευτικής»
Όροι σπουδών (από 15.10.2010 έως 14.09.2011)
Εργασία μαθήματοςπανω σε αυτο το θεμα:
“Δημιουργία συστήματος διαχείρισης ποιότητας φαρμάκων σε φαρμακείο ”
ΕΚΤΕΛΕΣΤΗΣ ΔΙΑΘΗΚΗΣ:
Fadeeva Maria Valerievna, φαρμακοποιός- πρακτική
Ερευνητική βάση:
Φαρμακείο "MAIR"
πόλη Βλαδιβοστόκ
Perm 2011
Εισαγωγή
1. Τωρινή κατάστασησυστήματα διαχείρισης ποιότητας για φάρμακα σε δραστηριότητες φαρμακείου σε ξένες χώρες…………....……5
2. Το νομοθετικό πλαίσιοδιαχείριση ποιότητας φαρμάκων στα φαρμακεία σύμφωνα με βιβλιογραφία και κανονιστικά έγγραφα ………………………………………………………………………..…..10
3. Διαχείριση φαρμακευτικών δραστηριοτήτων σε φαρμακείο ………………… 12
4. Δημιουργία συστήματος διαχείρισης ποιότητας για φάρμακα σε φαρμακείο ………………………………………………………………………………………………………………………………………………………………………
5. Βελτιστοποίηση του συστήματος διαχείρισης ποιότητας για φαρμακευτικές δραστηριότητες σε φαρμακείο……………………………………………………………….22
6. Ανάλυση και τρόποι βελτίωσης του συστήματος διαχείρισης ποιότητας των φαρμάκων στο φαρμακείο της MAIR LLC ……………………………23
Συμπεράσματα ………………………………………………………………………………………………….
Κατάλογος χρησιμοποιημένης βιβλιογραφίας ……………………………………………..26
ΕΙΣΑΓΩΓΗ
Ο κοινωνικός προσανατολισμός της φαρμακευτικής αγοράς, που προβλέπει την ανάγκη για ζωτικής σημασίας φάρμακα και, κατά συνέπεια, την ανάγκη διατήρησης και βελτίωσης της υγείας, επιβάλλει την ανάπτυξη ενός συστήματος διαχείρισης ποιότητας για τα φαρμακευτικά προϊόντα και τις υπηρεσίες που εισάγονται στην αγορά. Η βάση αυτού του συστήματος είναι το σύστημα διαχείρισης ποιότητας των φαρμάκων σε όλα τα στάδια της λειτουργίας τους κύκλος ζωήςκαι την ποιότητα της φαρμακευτικής περίθαλψης ως δραστηριότητα για την παροχή φαρμακευτικών υπηρεσιών στον πληθυσμό. Η ποιότητα των φαρμάκων σε ομοσπονδιακό επίπεδο ορίζεται νομικά ως συμμόρφωση με το κρατικό πρότυπο.
Η τρέχουσα λειτουργία της ρωσικής φαρμακευτικής αγοράς χαρακτηρίζεται από ένα συνεχώς διευρυνόμενο φάσμα φαρμάκων και έναν αδικαιολόγητα μεγάλο αριθμό προμηθευτών. Υπό αυτές τις συνθήκες, το πρόβλημα της διασφάλισης της ποιότητας της φροντίδας των ναρκωτικών που παρέχεται στον πληθυσμό είναι ιδιαίτερα σημαντικό. Σύμφωνα με τις απαιτήσεις του τρέχοντος βιομηχανικού προτύπου «Κανόνες για την κυκλοφορία (πώληση) φαρμάκων σε οργανισμούς φαρμακείων. Βασικές διατάξεις «σε κάθε οργανισμό φαρμακείου που ασχολείται με τη λιανική πώληση φαρμάκων, πρέπει να δημιουργηθεί ένα σύστημα διαχείρισης ποιότητας. Αυτό οφείλεται στην ειδική επαγγελματική ευθύνη για την ποιότητα της φαρμακευτικής φροντίδας που ανατίθεται στα φαρμακεία. Σήμερα υπάρχει ολόκληρη γραμμήδημοσιεύσεις σε κορυφαίες φαρμακευτικές εκδόσεις, διάφορους τομείς της οικονομίας, αλλά, δυστυχώς, στη φαρμακευτική, η διαχείριση ποιότητας και οι δραστηριότητες ενός επιτρόπου ποιότητας συγχέονται με την εκτέλεση των λειτουργικών καθηκόντων ενός φαρμακοποιού-αναλυτή.
Εάν στη βιομηχανία το σύστημα διαχείρισης ποιότητας έχει εισαχθεί εδώ και πολύ καιρό, τότε στις δραστηριότητες του οργανισμού φαρμακείου μόλις αρχίζει να ζει και να εργάζεται. Μέχρι σήμερα, δεν υπάρχουν (τεκμηριωμένες) συστάσεις για την εφαρμογή του συστήματος σε οργανισμούς φαρμακείων, οι οποίες θα πρέπει να δημιουργηθούν με βάση διεθνή πρότυπαποιότητα.
Η έννοια της ποιότητας συνίσταται στη σχέση μεταξύ του παραγωγού και του καταναλωτή των αγαθών. Τα προϊόντα είναι τόσο υψηλής ποιότητας, άρα ικανοποιούν τις απαιτήσεις και τις ανάγκες του καταναλωτή. Οι κύριες ιδιότητες της ποιότητας είναι οι εξής: αναπαλλοτρίωτο από το αντικείμενο (αν μιλάμε για δίκτυο λιανικής, τότε η ποιότητα πρέπει να υπάρχει σε κάθε σημείο). μεταβλητότητα με την πάροδο του χρόνου, είναι αδύνατο να μετρηθεί η ποιότητα μία φορά, επειδή οι παράγοντες επιρροής αλλάζουν και η ποιότητα αλλάζει ανάλογα (για παράδειγμα, ήρθε νέο προσωπικό, αυξήθηκε ο φόρτος εργασίας και, ως αποτέλεσμα, άλλαξε η ποιότητα). Ο τύπος ποιότητας μπορεί να εκφραστεί ως εξής: η αναλογία των αντιληπτών χαρακτηριστικών των υπηρεσιών προς τα χαρακτηριστικά των υπηρεσιών που αναμένει ο πελάτης. Η ποιότητα είναι μέγιστη εάν ο δείκτης της είναι ίσος με ένα.
Η εισαγωγή ενός συστήματος διαχείρισης ποιότητας για τις φαρμακευτικές δραστηριότητες σύμφωνα με τις διεθνείς απαιτήσεις καθιστά δυνατή την απομάκρυνση από την αδειοδότηση φαρμακευτικών δραστηριοτήτων. Είναι πιο σημαντικό να έχετε άδεια ειδικού. Εάν υπάρχουν παραβιάσεις στις δραστηριότητες που πραγματοποιούνται από ειδικό, χάνει την άδειά του και η επιχείρηση συνεχίζει να εργάζεται.
Εκτός, σύγχρονη σκηνήΗ ανάπτυξη της ρωσικής φαρμακευτικής αγοράς χαρακτηρίζεται από μια ανάπτυξη που μοιάζει με χιονοστιβάδα στο φάσμα των φαρμάκων που εισάγονται για πρώτη φορά στην αγορά. Αυτό, αφενός, επιτρέπει στον γιατρό, με την επιφύλαξη επαρκούς επαγγελματικής επίγνωσης της διαθεσιμότητας προτάσεων και των ιδιοτήτων των φαρμάκων, να επιλέξει το βέλτιστο σχήμα για τη φαρμακοθεραπεία της νόσου, αφετέρου, περιπλέκει την ίδια τη διαδικασία επιλογής λόγω στα πολλά κριτήρια για την επιλογή του βέλτιστου φαρμάκου. Ένας φαρμακοποιός που ασχολείται με την πώληση φαρμάκων, όταν παρέχει συμβουλές στους καταναλωτές, συναντά επίσης συχνά ορισμένες δυσκολίες που προκαλούνται από την ανεπαρκή επίγνωση των φαρμακοοικονομικών χαρακτηριστικών των νέων φαρμάκων. Για να απαντήσει κάποιος ειδικός σύγχρονα πρότυπακαι απαιτήσεις, είναι απαραίτητο να καθοριστεί με σαφήνεια ο βαθμός ευθύνης του για την εργασία που του ανατέθηκε. Ακριβώς επαγγελματικό επίπεδοο ειδικός θα πρέπει να γίνει ένα από τα κύρια στοιχεία του συστήματος διαχείρισης ποιότητας στην επιχείρηση φαρμακείου.
Ως εκ τούτου, σκοπός αυτής της εργασίας είναι η μελέτη θεωρητικών και πρακτικών προσεγγίσεων για τη δημιουργία συστήματος διαχείρισης ποιότητας φαρμάκων σε ένα φαρμακείο, καθώς και η ανάλυση των προβλημάτων που προκύπτουν σε αυτή την περίπτωση και η ανάπτυξη τρόπων επίλυσής τους.
Για την επίτευξη αυτού του στόχου απαιτείται η επίλυση των ακόλουθων εργασιών:
1. Μελέτη της τρέχουσας κατάστασης του συστήματος διαχείρισης ποιότητας φαρμάκων στις δραστηριότητες φαρμακείων σε ξένες χώρες και στη Ρωσική Ομοσπονδία
2. Συνεκτίμηση θεωρητικές βάσειςσυστήματα διαχείρισης ποιότητας για φάρμακα σε οργανισμούς φαρμακείων σύμφωνα με τη βιβλιογραφία και τα κανονιστικά έγγραφα.
3. Βελτιστοποίηση του συστήματος διαχείρισης ποιότητας για φαρμακευτικές δραστηριότητες στο φαρμακείο.
4. Ανάλυση διαχείρισης ποιότητας φαρμάκων στο φαρμακείο MAIR στο Βλαδιβοστόκ.
Η μεθοδολογία της έρευνας βασίζεται στις συνταγματικές αρχές των κρατικών εγγυήσεων για την προστασία της υγείας των πολιτών, νομοθετικές και κανονιστικές πράξεις της Ρωσικής Ομοσπονδίας στον τομέα της υγειονομικής περίθαλψης και προμήθεια φαρμάκων, την έννοια της ΠΟΥ για την εθνική πολιτική στον τομέα της προμήθειας φαρμάκων, επιστημονικές εργασίες εγχώριων και ξένων συγγραφέων στον τομέα της διαχείρισης και της οικονομίας της φαρμακευτικής και της υγειονομικής περίθαλψης και της φαρμακευτικής διαχείρισης. Για τη συγγραφή της εργασίας χρησιμοποιήθηκε επίσης η εκπαιδευτική βιβλιογραφία για τον κλάδο, άρθρα από εξειδικευμένα περιοδικά, καθώς και πηγές του Διαδικτύου.
1. Η τρέχουσα κατάσταση του συστήματος διαχείρισης ποιότητας φαρμάκων στις δραστηριότητες φαρμακείων σε χώρες του εξωτερικού
Αναπτύσσοντας τη δική της εθνική πολιτική στον τομέα της προμήθειας ναρκωτικών, η Ρωσία θα πρέπει να λάβει υπόψη τις αποδεκτές διεθνείς απαιτήσεις στο μέγιστο δυνατό βαθμό. Σε ειδική εντολή του Προέδρου της Ρωσίας Βλαντιμίρ Πούτιν, που δόθηκε τον Σεπτέμβριο του 2003, τονίζεται η ανάγκη εναρμόνισης των κανονισμών της Ρωσικής Ομοσπονδίας στον τομέα της κυκλοφορίας των φαρμάκων με τους κανόνες που είναι αποδεκτοί στη διεθνή πρακτική. Στον Βασικό Νόμο το 1998 και αργότερα το 2003, στο 80ο βιομηχανικό πρότυπο, έννοιες όπως φαρμακείο (συμπεριλαμβανομένου νοσοκομειακού), φαρμακείο υγειονομικής περίθαλψης, φαρμακείο, κατάστημα φαρμακείου, περίπτερο φαρμακείου ονομάζονταν "φαρμακείο ιδρύματα". Στην πραγματικότητα, στη φαρμακευτική αγορά σήμερα υπάρχουν δύο τύποι φαρμακευτικών οργανισμών - ιδρύματα φαρμακείων που συνδέονται με το λιανικό εμπόριο και άλλοι - χονδρέμποροι φαρμάκων.
Ι.Γ. Ο Komissinskaya (2007) εξέτασε λεπτομερώς τη σύγχρονη έννοια της διαχείρισης ποιότητας ενός οργανισμού φαρμακείου στον κόσμο. ISO (ISO) - Ο Διεθνής Οργανισμός Τυποποίησης είναι ένας διεθνής οργανισμός που βοηθά στην ανάπτυξη παγκοσμίως αναγνωρισμένων προτύπων, κανόνων και άλλων παρόμοιων εγγράφων, προκειμένου να διευκολυνθεί η διεθνής ανταλλαγή αγαθών και υπηρεσιών. Το ISO είναι συντομογραφία της ελληνικής λέξης isos, «καθολική». Είναι σημαντικό να κατανοήσουμε τι είναι τα πρότυπα ISO, γιατί ακριβώς ρυθμίζουν τις απαιτήσεις σε όλο τον κόσμο, δίνουν τις βασικές διατάξεις και έννοιες στον τομέα του συστήματος διαχείρισης ποιότητας.
Η ιστορία της εμφάνισης των προτύπων ISO 9000 συνδέεται με την Παγκόσμια Αντίληψη της Νομοθετικής Διασφάλισης Ποιότητας Αγαθών και Υπηρεσιών που υιοθετήθηκε στην ΕΕ, η οποία περιλαμβάνει: το σύστημα διαχείρισης ποιότητας ενός κατασκευαστή. Έλεγχος προϊόντων σε εργαστήρια δοκιμών· πιστοποίηση προϊόντος· εφαρμογή του συστήματος διαχείρισης ποιότητας σε οργανισμούς ως εγγύηση σταθερής ποιότητας προϊόντων και υπηρεσιών.
Η παγκόσμια εμπειρία στην οργάνωση εργασιών στον τομέα της διαχείρισης ποιότητας συνοψίζεται και συστηματοποιείται στα πρότυπα της σειράς ISO 9000 - αυτό είναι ένα πακέτο εγγράφων διασφάλισης ποιότητας που προετοιμάστηκε από την 176η επιτροπή του Διεθνούς Οργανισμού Τυποποίησης.
Σύμφωνα με τη διεθνή πρακτική, μόνο οι υποχρεωτικές απαιτήσεις για τα προϊόντα καθορίζονται από το νόμο και όλοι οι άλλοι όροι ορίζονται σε συμφωνία μεταξύ των συμμετεχόντων στην αγορά, δηλ. Το φαρμακείο είναι πλήρως υπεύθυνο για την ποιότητα των προϊόντων που αγοράζονται από τους προμηθευτές. Η σειρά προτύπων ISO 9000 είναι το διεθνές σημείο αναφοράς για τις απαιτήσεις ποιότητας για τις επιχειρηματικές δραστηριότητες. Ο κύριος στόχος τους είναι να βοηθήσουν τα φαρμακεία να εντοπίσουν πιθανούς προμηθευτές με ένα αποτελεσματικό σύστημα διαχείρισης ποιότητας. μείωση του κόστους ποιότητας λόγω της εμπιστοσύνης στην ποιότητα του προμηθευτή· βοήθεια και μεθοδολογική βοήθεια σε οργανισμούς στη δημιουργία συστημάτων ποιότητας. Τα κυριότερα είναι: ISO 9000-2001, που ονομάζεται «Σύστημα Διαχείρισης Ποιότητας. Basic Provisions and Vocabulary» είναι το θεμελιώδες πρότυπο από το οποίο βασίζονται όλες οι ορολογίες και έννοιες. Η λογική του συνέχεια είναι το GOST R ISO 9001-2001, το οποίο ονομάζεται «Σύστημα Διαχείρισης Ποιότητας. Απαιτήσεις". Μέχρι σήμερα, υπάρχουν περισσότερα από 20 πρότυπα ISO στην παγκόσμια πρακτική.
Ως ποιότητα των φαρμακευτικών προϊόντων νοείται η συμμόρφωσή τους με όλους τους όρους καταχώρισης, τους όρους παραγωγής (τεχνολογία, χώρο παραγωγής, προσωπικό) και τα καθορισμένα χαρακτηριστικά. Τα φαρμακευτικά προϊόντα, όπως και κάθε άλλο προϊόν, περνούν από διάφορα στάδια του κύκλου ζωής (βρόχοι ποιότητας) (Εικ. 1).
Ρύζι. 1. Σύστημα διασφάλισης ποιότητας φαρμάκων
Η τρέχουσα παγκόσμια τάση στον τομέα του δελτισμού και της ρύθμισης της παραγωγής φαρμάκων είναι η παγκόσμια εναρμόνιση των απαιτήσεων για την παραγωγή φαρμάκων καθ' όλη τη διάρκεια του κύκλου ζωής του φαρμάκου και η έμφαση στην ικανοποίηση του καταναλωτή σύμφωνα με το σκοπό του φαρμάκου (Εικ. . 2).
Κατά την είσοδό του στην αγορά από την επιχείρηση, το φαρμακευτικό προϊόν λαμβάνει πιστοποιητικό ποιότητας υπογεγραμμένο από εξουσιοδοτημένο άτομοκατασκευαστή, εάν πληροί τους δείκτες ποιότητας του φακέλου καταχώρισης για την ασφάλεια, την αποτελεσματικότητα και παράγεται σύμφωνα με τους κανόνες GMP.
Ταυτόχρονα, υπάρχουν δύο σαφώς εκφρασμένες κατευθύνσεις - η αυξανόμενη κοινωνική ευθύνη του κατασκευαστή φαρμάκων, που επιβάλλεται από το κράτος και την κοινωνία συνολικά, και η έμφαση στη διασφάλιση της κυκλοφορίας των προϊόντων καλής ποιότηταςμέσω οργανωτικών και διαχειριστικών μέτρων σε όλα τα στάδια - από την ανάπτυξη ενός νέου φαρμάκου έως την εφαρμογή ολοκληρωμένο προϊόν– με ενεργό ρυθμιστικό ρόλο των κρατικών φορέων.

Ρύζι. 2. Βασικές απαιτήσεις της ΠΟΥ για την ποιότητα των φαρμάκων
Ως αποτέλεσμα των εργασιών της εκτελεστικής επιτροπής για αυτή τη στιγμήήταν η ανάπτυξη και υιοθέτηση εγγράφων που σχετίζονται με τη διαδικασία δημιουργίας φαρμάκων (Ε8 «Φαρμακευτική Ανάπτυξη»), τη διαχείριση κινδύνων ποιότητας (Ε9 «Διαχείριση Κινδύνου Ποιότητας») και το σύστημα ποιότητας (Ε10 «Συστήματα Φαρμακευτικής Ποιότητας») (Εικ. 3) .
Επιπλέον, από τη σκοπιά των προτύπων ISO, θα εξετάσουμε τι κάνει ένας οργανισμός φαρμακείων, ποιος ενδιαφέρεται για τι και πώς να κάνει αυτή τη δραστηριότητα πιο αποτελεσματική και αποτελεσματική. Η έννοια της διασφάλισης ποιότητας των φαρμάκων παρέχει μια ευκαιρία για την καλύτερη κατανόηση, αναγνώριση και εκπλήρωση των υποχρεώσεων που βαρύνουν όλους τους ασκούμενους φαρμακοποιούς. Η Ορθή Φαρμακευτική Πρακτική (GPP) είναι μια δραστηριότητα που σχετίζεται με την προμήθεια, αποθήκευση και χρήση φαρμάκων και ιατροτεχνολογικών προϊόντων που πραγματοποιείται σε φαρμακεία.
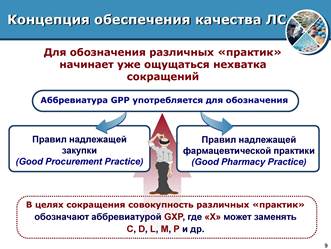
Εικ.3. Κανόνες Ορθής Φαρμακευτικής Πρακτικής για Διασφάλιση Ποιότητας Φαρμακευτικών Προϊόντων
Ο εκκινητής των δραστηριοτήτων καθορισμού προτύπων είναι οι εθνικές ρυθμιστικές αρχές σε στενή συνεργασία με κατασκευαστές που εκπροσωπούνται από φαρμακευτικές ενώσεις.
Το πρότυπο ISO και το πιστοποιητικό είναι δύο αχώριστες έννοιες. Φυσικά, μπορείτε να εφαρμόσετε το σύστημα ISO χωρίς να το πιστοποιήσετε, αλλά ποιος θα ελέγξει πόσο καλά είναι κατασκευασμένο; ΣΤΟ αυτή η υπόθεσηυπάρχει ένα έγγραφο που ονομάζεται "Πιστοποιητικό ISO 9000", το οποίο επιβεβαιώνει τη συμμόρφωση του συστήματος διαχείρισης ποιότητας του οργανισμού με τις καθιερωμένες απαιτήσεις. Το πιστοποιητικό φαρμάκου είναι ένα έγγραφο που επιβεβαιώνει τη συμμόρφωση ενός φαρμάκου με την ποιότητα. Το πιστοποιητικό ISO είναι ένα έγγραφο που επιβεβαιώνει τη συμμόρφωση του συστήματος διαχείρισης ποιότητας με τις απαιτήσεις των σχετικών GOST. Μιλώντας για το σύστημα διαχείρισης ποιότητας, δεν μπορούμε παρά να μιλήσουμε για πρότυπα ISO.
Οι κύριες διατάξεις του συστήματος διαχείρισης ποιότητας περιγράφονται στο πρότυπο ISO 9000. Διατυπώνει 8 αρχές διαχείρισης ποιότητας:
1. Προσανατολισμός στον καταναλωτή: κατανόηση των τρεχουσών και μελλοντικών του αναγκών, ικανοποίηση των απαιτήσεών του και προσπάθεια υπέρβασης των προσδοκιών του.
2. Ηγεσία του επικεφαλής, διασφαλίζοντας την ενότητα του σκοπού και της κατεύθυνσης του οργανισμού.
3. Συμμετοχή των εργαζομένων, δίνοντας τη δυνατότητα να επωφεληθούν από τις ικανότητές τους.
4. Διαδικαστική προσέγγιση για τη διαχείριση δραστηριοτήτων και συναφών πόρων.
5. Συστημική προσέγγιση στη διαχείριση: ο εντοπισμός, η κατανόηση και η διαχείριση αλληλένδετων διαδικασιών ως σύστημα συμβάλλουν στην αποτελεσματικότητα και αποδοτικότητα του οργανισμού στην επίτευξη των στόχων του.
6. Συνεχής βελτίωση των δραστηριοτήτων του οργανισμού.
7. Λήψη αποφάσεων με βάση την ανάλυση δεδομένων και πληροφοριών.
8. Αμοιβαία επωφελείς σχέσεις με προμηθευτές.
Η επίτευξη στόχων ποιότητας μπορεί να έχει θετικό αντίκτυπο στην ποιότητα των προϊόντων, στη λειτουργική αποτελεσματικότητα και στην οικονομική απόδοση, και συνεπώς στην ικανοποίηση και την εμπιστοσύνη των ενδιαφερομένων.
Οι κύριες διατάξεις του συστήματος διαχείρισης ποιότητας περιλαμβάνουν τεκμηρίωση, η οποία καθιστά δυνατή τη μεταφορά του νοήματος και της αλληλουχίας των ενεργειών.
Επί του παρόντος, δεν αναμένεται πλέον να παρέχει μόνοτην ποιότητα του προϊόντος και την παράδοση στόχοςικανοποίηση των καταναλωτών με την ικανοποίηση και υπέρβαση των απαιτήσεών τους μέσω της εφαρμογής αποτελεσματικών συστημάτων διαχείρισης ποιότητας, της συνεχούς βελτίωσης της αποτελεσματικότητάς της, καθώς και της πρόληψης διαφορών μεταξύ των προσδοκιών των καταναλωτών και της ποιότητας των προϊόντων και υπηρεσιών που τους προσφέρονται.
Αναγνωρίζεται σήμερα το πιο ισχυρό, αποτελεσματικό και δημοφιλές μεθοδολογικά μοντέλο διαχείρισης ποιότητας (Total Quality Management - TQM), το οποίο βασίζεται στην εφαρμογή αρχών όπως: προσανατολισμός προς τον πελάτη, διευθυντική ηγεσία, συμμετοχή όλου του προσωπικού στην επίλυση προβλημάτων ποιότητας, συστημική και διαδικασία προσέγγισηςστη διαχείριση, συνεχής βελτίωση της παραγωγής, αμοιβαία επωφελής συνεργασία, λήψη αποφάσεων βάσει δεδομένων.
2. Νομοθετικό πλαίσιοδιαχείριση της ποιότητας των φαρμάκων σε οργανισμούς φαρμακείων σύμφωνα με τη βιβλιογραφία και τα νομικά έγγραφα
Είναι σημαντικό να εξεταστεί ποια θεμελιώδη πρότυπα υπάρχουν στη Ρωσία, ποια από αυτά παρέχουν μια αποκωδικοποίηση των βασικών εννοιών και ορισμών, ποιο πρότυπο επιβάλλει απαιτήσεις στη διαδικασία πιστοποίησης ενός οργανισμού και σε ένα σύστημα διαχείρισης ποιότητας. Από τη Ρωσία συμμετέχει στις δραστηριότητες του ISO κρατική υπηρεσία- Gosstandart της Ρωσίας.
Σε σχέση με την ένταξη στην παγκόσμια κοινότητα, το σύνολο των προτύπων ISO λαμβάνεται υπόψη και εφαρμόζεται στη Ρωσία, όπου, με βάση αυτά τα πρότυπα, αναπτύχθηκαν τα ακόλουθα:
Το GOST R ISO 9000-2001 περιγράφει τις κύριες διατάξεις και περιέχει ορολογία που σχετίζεται με το σύστημα διαχείρισης ποιότητας.
Το GOST R ISO 9001-2001 ορίζει τις απαιτήσεις για ένα σύστημα διαχείρισης ποιότητας
Το πρότυπο (GOST R ISO 9004-2001) ονομάζεται «Σύστημα Διαχείρισης Ποιότητας. Συστάσεις για βελτίωση των δραστηριοτήτων». Τα πρότυπα 9001 και 9004 είναι ακριβώς τα ίδια στη δομή, αλλά το πρότυπο 9001 είναι πιο σαφές και συνοπτικό. Το πρότυπο 9004 βασίζεται, όπως ήταν, στο πρότυπο 9001, περιέχει τις ίδιες ενότητες, αλλά σε διευρυμένη μορφή, με επεξηγήσεις και προσθήκες. Αντικατοπτρίζει όχι μόνο τον τρόπο δημιουργίας ενός συστήματος διαχείρισης ποιότητας, λήψης πιστοποιητικού ISO για αυτό, αλλά και χρήσης του για τη βελτίωση των δραστηριοτήτων του οργανισμού. Και τα τρία καθορισμένα πρότυπα είναι στενά συνδεδεμένα.
Το τρέχον σύστημα διαχείρισης ποιότητας έχει αναπτυχθεί και εφαρμοστεί αυστηρά σύμφωνα με τις απαιτήσεις των εθνικών προτύπων της Ρωσικής Ομοσπονδίας GOST R 52249–2009 (GMP) «Κανόνες για την παραγωγή και τον ποιοτικό έλεγχο φαρμάκων» και το GOST R ISO 9001–2008 (ISO 9001:2008) «Συστήματα διαχείρισης ποιότητας. Απαιτήσεις".
Το ρωσικό πρότυπο GMP εκπονήθηκε από την Ένωση Μηχανικών Μικρορρύπανσης (ASINCOM). Το 2004, εγκρίθηκε με το Διάταγμα του Κρατικού Προτύπου της Ρωσίας t 10 Μαρτίου 2004 No. (Good Manufacturing Practice for φαρμακευτικά προϊόντα) της Ευρωπαϊκής Ένωσης. Το Διάταγμα του Υπουργείου Υγείας και του Υπουργείου Οικονομίας τέθηκε σε ισχύ την 1η Ιανουαρίου 2005 και η συμμόρφωση με τους κανόνες GMP στη φαρμακευτική παραγωγή στη Ρωσική Ομοσπονδία είναι υποχρεωτική.
Η διασφάλιση της ποιότητας των φαρμάκων (PM) είναι ένα από τα σημαντικότερα καθήκοντα του σύγχρονου φαρμακείου. Προκειμένου να τυποποιηθεί και να ενοποιηθεί η διαδικασία διασφάλισης της ποιότητας των φαρμάκων στο στάδιο της άμεσης παραλαβής τους από τους ασθενείς (η αλυσίδα λιανικής διανομής φαρμάκων), αναγνωρίζεται απαραίτητη χρήσηαρχές και μέθοδοι προτύπων Ορθής Φαρμακευτικής Πρακτικής (GPP). Ένας οργανισμός φαρμακείου όσον αφορά τα πρότυπα ISO είναι μια ομάδα εργαζομένων και απαραίτητα κεφάλαιαμε την κατανομή αρμοδιοτήτων, εξουσιών και σχέσεων που ασκούν φαρμακευτικές δραστηριότητες σε εγκαταστάσεις φαρμακείων όπως φαρμακείο, σημείο, περίπτερο, κατάστημα κ.λπ. .
Απαραίτητη προϋπόθεση για την υλοποίηση των φαρμακευτικών δραστηριοτήτων είναι η διασφάλιση της ποιότητας στους χονδρεμπόρους και στους φαρμακευτικούς οργανισμούς, κάτι που αντικατοπτρίζεται στους OST. Το πρώτο βήμα για τη δημιουργία ενός σύγχρονου Νομικό πλαίσιορύθμιση της φαρμακευτικής αγοράς, λαμβάνοντας υπόψη τους διεθνείς κανόνες, είναι η υιοθέτηση των ακόλουθων βιομηχανικών προτύπων:
OST 91500.05.0005-2002 "Κανόνες για το χονδρικό εμπόριο φαρμάκων. Βασικές διατάξεις", που εγκρίθηκε με εντολή του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 15ης Μαρτίου 2002 Αρ. 80.
OST 91500.05.0007-2003 "Κανόνες για την πώληση (πώληση) φαρμάκων στα φαρμακεία. Βασικές διατάξεις", που εγκρίθηκε με εντολή του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 04.03.2003 Αρ. 80.
3. Συστήματα διαχείρισης ποιότητας για φαρμακευτικές δραστηριότητες σε φαρμακείο
Τα προβλήματα δημιουργίας ενός αποτελεσματικού συστήματος διαχείρισης ποιότητας για φάρμακα (PM) σε ένα φαρμακείο αντικατοπτρίζονται στις δημοσιεύσεις ορισμένων εγχώριων επιστημόνων: D.V. Παρχομένκο, Ι.Γ. Komissinskaya, Z.K. Drugova, A.M. Biteryakova, S.V. Kononova και άλλοι.
Ένα σύστημα είναι μια συλλογή αλληλένδετων και αλληλεπιδρώντων αρχών. Σε κάθε σύστημα υπάρχει μια λεγόμενη είσοδος - δηλαδή διαδικασίες και υλικές αξίες που ξεκινούν ενέργειες, μέσα στο σύστημα υπάρχουν οι δικές τους διαδικασίες. Το σύστημα διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων στη Ρωσία καθορίζεται από τον ομοσπονδιακό νόμο αριθ. καταχώριση φαρμάκου, αδειοδότηση παραγωγής φαρμάκου και αδειοδότηση φαρμακευτικών δραστηριοτήτων .
Σύμφωνα με το άρθρο 45 του νόμου αυτού, οι εργαζόμενοι στα φαρμακεία έχουν ειδική επαγγελματική ευθύνη για την παροχή ποιοτικής φαρμακευτικής φροντίδας στον καταναλωτή. Η ζημιά που σχετίζεται με βλάβη στην υγεία που προκαλείται από τη χρήση φαρμάκων που έχουν καταστεί άχρηστα ως αποτέλεσμα παραβιάσεων των κανόνων φαρμακευτικής δραστηριότητας αποζημιώνεται από τον οργανισμό με υπαιτιότητα του οποίου διαπράχθηκε η παράβαση.
Η πολυπλοκότητα, η φύση πολλών σταδίων και η διάρκεια του "κύκλου ζωής των φαρμάκων" - από τη δημιουργία τους έως την παραλαβή τους από τον τελικό χρήστη - προκαθορίζουν την ανάγκη εισαγωγής ενός αποτελεσματικού συστήματος προληπτικής διαχείρισης ποιότητας φαρμάκων που αποτρέπει την είσοδο φαρμάκων χαμηλής ποιότητας στο φαρμακευτικό αγορά. Στην πορεία των φαρμάκων από τον κατασκευαστή στον καταναλωτή, ο τελευταίος κρίκος όπου η ποιότητα των φαρμάκων αξιολογείται από ειδικευμένους ειδικούς είναι το φαρμακείο. Η διαχείριση της ποιότητας του φαρμακείου βασίζεται στις αρχές της TQM και των προτύπων της σειράς ISO 9000.
ΣΤΟ φαρμακείαθα πρέπει να διαμορφωθεί ένα σύστημα διαχείρισης ποιότητας, μία από τις λειτουργίες του οποίου είναι ο έλεγχος της συμμόρφωσης με τις απαιτήσεις των κανονιστικών εγγράφων του συστήματος τυποποίησης στην υγειονομική περίθαλψη, ιδίως των προαναφερθέντων OST. Ο κύριος στόχος της δημιουργίας ενός αποτελεσματικού συστήματος για τη διαχείριση της ποιότητας των φαρμάκων (φαρμάκων) και των φαρμακευτικών δραστηριοτήτων σε ένα φαρμακείο είναι να διασφαλιστεί ότι ο καταναλωτής μπορεί να αγοράσει καλοήθη φάρμακα και να λάβει υψηλής ποιότητας ιατρική φροντίδα. .
Το OST 91500.05.0007-2003 «Κανόνες για τη διανομή (πώληση) φαρμάκων σε οργανισμούς φαρμακείων, βασικές διατάξεις» (εγκεκριμένο από το διάταγμα του Υπουργείου Υγείας της Ρωσίας) ρυθμίζει τους κανόνες για τις λιανικές πωλήσεις σε οργανισμούς φαρμακείων, ενότητα 9, ρήτρα Το 9.1 λέει: «Θα πρέπει να διαμορφωθεί ένα σύστημα στη διαχείριση ποιότητας ενός οργανισμού φαρμακείου». Η ρήτρα 9.9 αναφέρει: «Ο επικεφαλής του οργανισμού φαρμακείου διορίζει έναν ποιοτικό εκπρόσωπο από το διοικητικό προσωπικό».
Οι φαρμακευτικές υπηρεσίες έχουν υψηλή καταναλωτική αξία, καθώς αποτελούν ένα από τα είδη πνευματικών υπηρεσιών που συμβάλλουν στη διατήρηση και διατήρηση της ανθρώπινης υγείας. Το υψηλό καταναλωτικό κόστος προκαθορίζει τη νομιμότητα των υψηλών τιμών για αυτές τις υπηρεσίες.
Τα αποτελέσματα των υπηρεσιών είναι, κατά κανόνα, καθυστερημένα και διαφοροποιημένα, γεγονός που καθορίζει ειδική προσέγγισηστη διαμόρφωση τιμών για τις υπηρεσίες και ειδικό καθεστώς χρηματοδότησης φαρμακευτικών οργανισμών. Ο καταναλωτής των φαρμακευτικών υπηρεσιών είναι τόσο άτομο όσο και κοινωνία συνολικά.
Αυτά τα χαρακτηριστικά καθορίζουν τη διττή προσέγγιση του προβλήματος της ποιότητας των φαρμακευτικών υπηρεσιών. Πρώτον, η βελτίωση της ποιότητας είναι ένας από τους κύριους παράγοντες για το ανταγωνιστικό πλεονέκτημα ενός φαρμακευτικού οργανισμού και τη μεγιστοποίηση των κερδών. Αυτός είναι ο λόγος για τον οποίο το πρόβλημα της ποιότητας των φαρμακευτικών υπηρεσιών ξεκινά στο επίκεντρο των οικονομικών συμφερόντων του οργανισμού και επιτρέπει την ενίσχυση της οικονομικής βιωσιμότητάς του. Από την άλλη, η ποιότητα των φαρμακευτικών υπηρεσιών είναι ουσιαστική προϋπόθεσηεκπλήρωση της κοινωνικής τους λειτουργίας - παροχή ποιοτικής φαρμακευτικής περίθαλψης και εν τέλει - διατήρηση της ανθρώπινης υγείας. Ένας φαρμακευτικός οργανισμός μπορεί να θεωρήσει ότι έχει επιτύχει τους στόχους και τους στόχους του μόνο εάν έχει εξασφαλίσει υψηλό επίπεδο ποιότητας των παρεχόμενων υπηρεσιών. Γι' αυτό είναι απαραίτητο να αναπτυχθεί ένα σύστημα ποιότητας σε έναν οργανισμό ή μάλλον ένα σύστημα διαχείρισης (διαχείρισης) ποιότητας.
Η ποιότητα των φαρμακευτικών υπηρεσιών αποτελείται από δύο βασικά στοιχεία: ποιότητα φαρμάκων (PM)και την ποιότητα της φαρμακευτικής δραστηριότητας.
Ποιότητα φαρμάκωνκαθορίζεται από τα ακόλουθα στοιχεία :
Προσδιορισμός των αναγκών της αγοράς (ποιότητα επιλογής καταναλωτή).
Η ποιότητα του σχεδιασμού του φαρμάκου.
Η ποιότητα της παραγωγικής διαδικασίας.
Συμμόρφωση της ποιότητας του τελικού προϊόντος με το έργο.
Ποιοτική εξυπηρέτηση μετά την πώληση.
Οι κύριες ιδιότητες που καθορίζουν την ποιότητα των φαρμακευτικών και ιατρικών προϊόντων περιλαμβάνουν:
ασφάλεια- την κατάσταση των εμπορευμάτων φυσιολογικές συνθήκεςχρήση, αποθήκευση, μεταφορά και απόρριψή του, κατά την οποία ο κίνδυνος βλάβης στη ζωή, την υγεία και την ιδιοκτησία του καταναλωτή περιορίζεται σε αποδεκτό επίπεδο.
λειτουργικές ιδιότητες . Καθορίζουν την καταλληλότητα των προϊόντων για την εκτέλεση των προβλεπόμενων λειτουργιών τους υπό συγκεκριμένες συνθήκες χρήσης ή κατανάλωσης.
H αξιοπιστία. Σε πολλές περιπτώσεις, η ασφάλεια ενός προϊόντος καθορίζεται από την αξιοπιστία του, δηλ. το ακίνητο να διατηρεί τα αρχικά του χαρακτηριστικά για μεγάλο χρονικό διάστημα εντός ορισμένων ορίων κατά τη λειτουργία.
φιλικότητα προς το περιβάλλον. Χαρακτηρίζει το πτυχίο βλαβερές συνέπειεςιατρικά είδη σε περιβάλλονεμφανίζεται στο στάδιο ολόκληρης της διάρκειας ζωής του προϊόντος. Δείκτες περιβαλλοντικών επιδόσεων: το επίπεδο των επικίνδυνων χημικών εκπομπών, ακτινοβολία, συγκέντρωση βλαβερές ουσίες, καθώς και τη δυνατότητα ανακύκλωσης.
αισθητική- δείκτης ποιοτικής και ποσοτικής αξιολόγησης της αισθητικής αξίας των προϊόντων, ανάλογα με την ομάδα καταναλωτών, τις ειδικές συνθήκες κατανάλωσης και τον σκοπό του προϊόντος.
κατανάλωση πόρων. Χαρακτηρίζεται από το κόστος του καταναλωτή για την αγορά, τη λειτουργία και τη συντήρηση του προϊόντος κατά την περίοδο του μέσου τεχνικού πόρου, δηλ. πριν τεθεί εκτός λειτουργίας το προϊόν.
Αξιολόγηση της ποιότητας των φαρμάκων
Η ποιότητα των φαρμάκων αξιολογείται σύμφωνα με τις Οδηγίες για την αξιολόγηση της ποιότητας των φαρμάκων που παράγονται στα φαρμακεία (Διάταγμα του Υπουργείου Υγείας της Ρωσίας της 16ης Οκτωβρίου 1997 αριθ. 305) «Σχετικά με τους κανόνες των αποκλίσεων που επιτρέπονται στην παρασκευή φαρμάκων και συσκευασία βιομηχανικών προϊόντων στα φαρμακεία»). Η παρούσα εντολή ισχύει για όλα τα φαρμακεία, τα σημεία φαρμακείων (με δικαίωμα παρασκευής φαρμάκων) και τα εργαστήρια εδαφικού ελέγχου και ανάλυσης που ελέγχουν την ποιότητα των φαρμάκων που παρασκευάζονται στα φαρμακεία.
Η ποιότητα των φαρμάκων (συμπεριλαμβανομένων των ομοιοπαθητικών) που παρασκευάζονται στα φαρμακεία καθορίζεται από ένα σύνολο δεικτών. Το επίπεδο ποιότητας των φαρμάκων αξιολογείται σύμφωνα με τις απαιτήσεις που ρυθμίζονται από το τρέχον Παγκόσμιο Ταμείο, τις παραγγελίες και τις οδηγίες του Υπουργείου Υγείας της Ρωσίας.
Για την αξιολόγηση της ποιότητας, χρησιμοποιούνται οι όροι "Ικανοποιώ" ("Καλά προϊόντα") και "Μη ικανοποιητικό" ("Γάμος"). Το επίπεδο ποιότητας των παρασκευαζόμενων φαρμάκων καθορίζεται με οργανοληπτικές και μετρητικές μεθόδους.
Η μη ικανοποιητική ποιότητα των παρασκευασμένων φαρμάκων καθορίζεται από τους ακόλουθους δείκτες:
αναντιστοιχία σύμφωνα με την περιγραφή ( εμφάνιση, χρώμα, μυρωδιά).
αναντιστοιχία στη διαφάνεια ή στο χρώμα.
ασυμφωνία αποσύνθεσης;
ετερογένεια όσον αφορά το άλεσμα ή την ανάμειξη σκονών, αλοιφών, υπόθετων, ομοιοπαθητικών κονιοποιήσεων.
παρουσία ορατών μηχανικών εγκλεισμάτων.
Ασυνέπεια της συνταγής για τη γνησιότητα.
εσφαλμένη αντικατάσταση ενός φαρμάκου με άλλο, απουσία συνταγογραφούμενης ή παρουσία μη συνταγογραφούμενης ουσίας.
Αντικατάσταση φαρμάκων με παρόμοια φαρμακολογική δράσηχωρίς να αναφέρεται αυτή η αντικατάσταση στην απαίτηση, συνταγή (αντίγραφο της συνταγής, ετικέτα).
Αποκλίσεις από τη συνταγή κατά βάρος ή όγκο.
αποκλίσεις στη συνολική μάζα (όγκος).
αποκλίσεις στη μάζα των μεμονωμένων δόσεων και τον αριθμό τους.
· αποκλίσεις στο βάρος (ή τη συγκέντρωση) του δείγματος μεμονωμένων φαρμάκων.
αναντιστοιχία στην τιμή του pH.
ασυμφωνία στην τιμή της πυκνότητας.
μη συμμόρφωση με τη στειρότητα.
Αναντιστοιχία μικροβιολογικής καθαρότητας.
Παραβίαση της στερέωσης του πώματος (για στείρες μορφές δοσολογίας).
Παραβίαση των κανόνων για την έκδοση φαρμάκων που προορίζονται για διακοπές.
Οι αλλαγές στη σύνθεση της δοσολογικής μορφής (εάν είναι απαραίτητο) θα πρέπει να γίνονται μόνο με τη συγκατάθεση του γιατρού και θα πρέπει να σημειώνονται στην απαίτηση, συνταγή (αντίγραφο της συνταγής, ετικέτα). Εάν δεν υπάρχει το υποδεικνυόμενο σήμα στην απαίτηση, συνταγή (αντίγραφο της συνταγής, ετικέτα), η ποιότητα της κατασκευής LF αξιολογείται ως "Μη ικανοποιητική".
Οι αλλαγές στην ποσότητα των φαρμάκων που χορηγούνται ή που χορηγούνται δισκία αντί για σκόνες θα πρέπει επίσης να σημειώνονται στην απαίτηση, τη συνταγή κ.λπ.
Κατά τον προσδιορισμό των αποκλίσεων στις δοκιμασμένες δοσολογικές μορφές, θα πρέπει να χρησιμοποιούνται όργανα μέτρησης του ίδιου τύπου (με τα ίδια μετρολογικά χαρακτηριστικά) όπως και στην κατασκευή τους στα φαρμακεία.
Έχουν καθιερωθεί οι κανόνες των αποκλίσεων που επιτρέπονται στην κατασκευή μορφών δοσολογίας (συμπεριλαμβανομένων των ομοιοπαθητικών) στα φαρμακεία (εντολή του Υπουργείου Υγείας της Ρωσίας με ημερομηνία 16/10/97 Αρ. 305).
Κατά τον προσδιορισμό των επιτρεπόμενων αποκλίσεων στα ελεγχόμενα φάρμακα, που παρασκευάζονται με τη μορφή μιας σειράς παρασκευασμάτων στο φαρμακείο, θα πρέπει να χρησιμοποιηθούν τα παραπάνω πρότυπα απόκλισης, καθώς και η τρέχουσα κανονιστική τεκμηρίωση που διέπει την παρασκευή και τον ποιοτικό έλεγχο διαφόρων μορφών δοσολογίας στα φαρμακεία .
Ποιότητα φαρμακευτικής δραστηριότητας
Η αγορά φαρμακευτικών υπηρεσιών έχει σαφώς καθορισμένα εδαφικά όρια. Κατά τη λειτουργία της φαρμακευτικής αγοράς είναι απαραίτητος ο κρατικός έλεγχος, αφού οι φαρμακευτικές υπηρεσίες είναι δημόσιο αγαθό και είναι απαραίτητο να αποφευχθεί η μονοπώλησή τους. Το κράτος εκτελεί λειτουργίες που σχετίζονται κυρίως με τη νομική ρύθμιση, την υποστήριξη πληροφοριών και άλλες πτυχές της ανάπτυξης της αγοράς. Έτσι, μπορούμε να μιλάμε για ένα είδος διττής φύσης των φαρμακευτικών υπηρεσιών. Από τη μια πλευρά, είναι ένα προϊόν που έχει τη δική του καταναλωτική αξία και μπορεί να λειτουργήσει ως υποκείμενο των σχέσεων της αγοράς. Η υλοποίηση, σε αυτή την περίπτωση, θα πρέπει να είναι εμπορικού χαρακτήρα και να επιδιώκει το μέγιστο κέρδος.
Από την άλλη πλευρά, οι φαρμακευτικές υπηρεσίες είναι κοινό καλό,τα διακριτικά χαρακτηριστικά των οποίων είναι το αδιαίρετο, η κοινή φύση της κατανάλωσης, η υψηλή κοινωνική σημασία, η κυριαρχία της δημόσιας-κρατικής ιδιοκτησίας στην παραγωγή και την κατανάλωσή τους. Από την πλευρά του καταναλωτή, οι φαρμακευτικοί οργανισμοί παρέχουν ολοκληρωμένη υπηρεσία, ικανοποιώντας τις σημαντικότερες κοινωνικές ανάγκες τόσο του ατόμου όσο και της κοινωνίας συνολικά. Ένα σημαντικό χαρακτηριστικόείναι επίσης το γεγονός ότι η παροχή φαρμακευτικών υπηρεσιών απαιτεί συμμόρφωση με ορισμένα ηθικά και ηθικά πρότυπα. Όλα αυτά το κάνουν δύσκολο ποσοτικοποίησηδραστηριότητα, η οποία περιορίζει την εφαρμογή των εμπορικών αρχών δραστηριότητας στη φαρμακευτική δραστηριότητα.
Από αυτό προκύπτει ότι το σύστημα διαχείρισης ποιότητας φαρμάκων συνήθως νοείται ως ένα σύνολο οργανωτικών μέτρων που διασφαλίζουν την παροχή υψηλής ποιότητας φαρμακευτικής φροντίδας στον καταναλωτή, η οποία είναι ένας συνδυασμός της ποιότητας των φαρμάκων καθαυτών και της ποιότητας του φαρμακευτικού προϊόντος. δραστηριότητες του Φαρμακευτικού Οργανισμού. Η τρέχουσα κατάσταση στον τομέα της διαχείρισης ποιότητας απαιτεί την ανάπτυξη πρακτικών προσεγγίσεων και αρχών διαχείρισης για την επίλυση του προβλήματος της εξασφάλισης της διαθεσιμότητας ποιοτικών φαρμάκων στον πληθυσμό σε κάθε οργανισμό φαρμακείου.
4. Δημιουργία συστήματος διαχείρισης ποιότητας
φάρμακα σε φαρμακείο
Διάταγμα του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας αριθ. 80 της 4ης Μαρτίου 2003 «Σχετικά με την έγκριση του βιομηχανικού προτύπου «Κανόνες για τη διανομή (πώληση) φαρμακευτικών προϊόντων σε οργανισμούς φαρμακείων. Βασικές Διατάξεις». Περιέχει ενότητα IX Διασφάλιση ποιότητας φαρμάκων (φαρμάκων) σε οργανισμούς φαρμακείων.
Σε οργανισμούς φαρμακείων ή μεμονωμένους επιχειρηματίες, θα πρέπει να δημιουργηθεί ένα σύστημα διασφάλισης ποιότητας, το οποίο περιλαμβάνει:
Χώροι και εξοπλισμός που αντιστοιχούν στο πεδίο των δραστηριοτήτων του φαρμακείου και επιτρέπουν τη διασφάλιση της συμμόρφωσης με τις προϋποθέσεις αποθήκευσης και παρασκευής φαρμάκων·
Τεκμηρίωση που επιτρέπει την αναγνώριση της προέλευσης, της ποσότητας και της ποιότητας των εισερχόμενων φαρμάκων και την τήρηση αρχείων αποθηκευμένων και πωληθέντων φαρμάκων·
Έλεγχος εισόδου που εισέρχεται στον οργανισμό φαρμακείου ή ατομικός επιχειρηματίας LS;
Προσωπικό με τα απαραίτητα προσόντα.
Σύστημα συνεχούς εκπαίδευσης προσωπικού.
περιγραφές εργασίας;
Ένα ταμείο ρυθμιστικού και υλικού αναφοράς που θα πρέπει να παρέχεται σε όλες τις εγκαταστάσεις φαρμακείων ενός συγκεκριμένου οργανισμού φαρμακείου.
Ένας οργανισμός φαρμακείου πρέπει να σχηματίζει ένα σύστημα διαχείρισης ποιότητας για έναν οργανισμό φαρμακείου.
Κάθε οργανισμός φαρμακείου πρέπει να έχει εσωτερικούς κανονισμούς εργασίας εγκεκριμένους από τον επικεφαλής του οργανισμού, με ένδειξη εξοικείωσης των εργαζομένων. Αναθεώρηση των κανόνων και επανεξοικείωση των εργαζομένων του οργανισμού φαρμακείου με αυτούς πραγματοποιείται ετησίως.
Ο οργανισμός φαρμακείου πρέπει να διεξάγει τακτικά εσωτερικούς ελέγχους για τη συμμόρφωση με τις απαιτήσεις της GOST. Κατά τη διεξαγωγή επιθεωρήσεων, πρέπει να δίνεται προσοχή στην παρουσία στον οργανισμό φαρμακείου σχετικών εγγράφων για τις εγκαταστάσεις που καταλαμβάνονται, περιγραφές θέσεων εργασίας των εργαζομένων, πρότυπα και άλλα απαραίτητα έγγραφα.
Οι επιθεωρήσεις μπορούν να διενεργούνται τόσο από υπαλλήλους του φαρμακείου, ανεξάρτητα από τα άτομα που εμπλέκονται άμεσα στην ελεγχόμενη δραστηριότητα, όσο και από ανεξάρτητους εμπειρογνώμονες. Η συχνότητα των επιθεωρήσεων καθορίζεται από τον ίδιο τον οργανισμό του φαρμακείου. Τα αποτελέσματα των επιθεωρήσεων καταγράφονται και γνωστοποιούνται στο προσωπικό που είναι υπεύθυνο για την περιοχή εργασίας που επιθεωρείται και στη διεύθυνση του οργανισμού φαρμακείου. Οι επακόλουθες ανασκοπήσεις παρακολουθούν την εφαρμογή των συστάσεων και την αποτελεσματικότητά τους. Κάθε υπάλληλος του οργανισμού φαρμακείου πρέπει να είναι εξοικειωμένος με το GOST, τη διαδικασία εκπλήρωσης των καθηκόντων που του έχουν ανατεθεί, τις κανονιστικές νομικές πράξεις και τα πρότυπα που σχετίζονται με τις δραστηριότητες του οργανισμού. Στους οργανισμούς φαρμακείων, κάθε εργαζόμενος πρέπει να έχει εγκεκριμένες περιγραφές θέσεων εργασίας με τον κατάλληλο τρόπο.
Οι Φαρμακευτικοί Οργανισμοί θα πρέπει να προβλέπουν σύστημα συνεχούς επαγγελματικής εξέλιξης των εργαζομένων σε θέματα ισχύουσας νομοθεσίας, χρήσης φαρμάκων κ.λπ. Το σχέδιο και τα θέματα των μαθημάτων εγκρίνονται από τον επικεφαλής του οργανισμού φαρμακείου. Ο επικεφαλής του οργανισμού φαρμακείου διορίζει έναν ποιοτικό εκπρόσωπο από το διοικητικό προσωπικό.
Από αυτή την άποψη, δεν υπάρχει αμφιβολία η ανάγκη για συνεχή βελτίωση των επαγγελματικών δεξιοτήτων του φαρμακευτικού προσωπικού. Ένας από τους τρόπους επίλυσης αυτού του προβλήματος είναι η αύξηση της αποτελεσματικότητας του συστήματος μεταπτυχιακής εκπαίδευσης των φαρμακοποιών.
Ο οργανισμός φαρμακείου διασφαλίζει τη διατήρηση της τεκμηρίωσης σύμφωνα με τις νομοθετικές και κανονιστικές νομικές πράξεις της Ρωσικής Ομοσπονδίας.
Πρώτα απ 'όλα, το καθήκον του φαρμακείου είναι να παρέχει τα διατηρημένα χαρακτηριστικά των αγαθών που λαμβάνονται από τον οργανισμό φαρμακείου. Αυτές είναι δύο ομάδες: λειτουργικές ιδιότητες - αποτελεσματικότητα και ασφάλεια, φυσικές και φυσικοχημικές, που απαιτούν συμμόρφωση με τους κανόνες για το χειρισμό τους. Ως μέρος του συστήματος διαχείρισης ποιότητας ενός οργανισμού φαρμακείου, κάθε φαρμακείο θα πρέπει να οργανώνει:
1. Έλεγχος αποδοχής. Πραγματοποιείται για την αποτροπή παραλαβής και πώλησης παραποιημένων, απορριφθέντων και κακής ποιότητας προϊόντων μέσω του δικτύου φαρμακείων. Ρυθμίζεται από το Βιομηχανικό Πρότυπο OST 91500.05.0007.-2003 "Κανόνες για την κυκλοφορία (πώληση) φαρμάκων σε οργανισμούς φαρμακείων." Οι ζώνες (εγκαταστάσεις) για την παραλαβή και τη χορήγηση φαρμάκων πρέπει να διαχωρίζονται από τον χώρο αποθήκευσης και πρέπει να παρέχουν επαρκή (αξιόπιστη) προστασία των παραληφθέντων φαρμάκων από τις κακές καιρικές συνθήκες κατά τις εργασίες φόρτωσης (εκφόρτωσης). Τα παραλαμβανόμενα προϊόντα υπόκεινται σε εισερχόμενο ποιοτικό έλεγχο. Τα αποτελέσματα του ελέγχου εισροών πρέπει να καταχωρούνται σύμφωνα με την εσωτερική διαδικασία που έχει θεσπιστεί στο φαρμακείο. Κατά την εκφόρτωση, τα προϊόντα ελέγχονται για συμμόρφωση με την παραγγελία και για ζημιές σε συσκευασίες ή δοχεία. Φάρμακα και άλλα προϊόντα που επιτρέπονται προς πώληση από φαρμακευτικούς οργανισμούς που έχουν λήξει, δεν πληρούν τις απαιτήσεις ποιότητας, τα πρότυπα και χωρίς έγγραφα που πιστοποιούν την ποιότητά τους δεν υπόκεινται σε αποδοχή. Για φαρμακευτικά προϊόντα (φάρμακα) σε κατεστραμμένη συσκευασία, χωρίς πιστοποιητικά ή/και απαραίτητα συνοδευτικά έγγραφα, που απορρίφθηκαν κατά την αποδοχή ή τη χορήγηση στον ασθενή, όχι σύμφωνα με την παραγγελία ή με ληγμένη διάρκεια ζωής, συντάσσεται πράξη. πρέπει να φέρουν την κατάλληλη επισήμανση και να τοποθετηθούν σε καθορισμένο χώρο χωριστά από άλλα φαρμακευτικά προϊόντα μέχρι να αναγνωριστούν, να επιστραφούν στον προμηθευτή ή να απορριφθούν με τον προβλεπόμενο τρόπο. Δηλητηριώδες και ισχυρές ουσίες, ναρκωτικά, ψυχοτρόπες ουσίες, θερμοευαίσθητα φάρμακα πρέπει να τοποθετούνται αμέσως σε χώρους αποθήκευσης σύμφωνα με τις απαιτήσεις της παρούσας OCTa.
Ο αριθμός των φαρμάκων που λαμβάνονται και απαιτούν ειδικές συνθήκες αποθήκευσης πρέπει να αντιστοιχεί στη διαθέσιμη χωρητικότητα του ειδικού εξοπλισμού. Τα αποδεκτά φαρμακευτικά προϊόντα και άλλα αγαθά που επιτρέπονται για διανομή από οργανισμούς φαρμακείων πιστώνονται εντός των προθεσμιών που έχουν καθοριστεί για την αποδοχή των προϊόντων ως προς τον αριθμό των εμπορικών μονάδων και την πληρότητα με τον καθορισμένο τρόπο. 6. Όλες οι αποστολές εμπορευμάτων πρέπει να συνοδεύονται από έγγραφα που επιτρέπουν τον καθορισμό της ημερομηνίας αποστολής, της ονομασίας του φαρμακευτικού προϊόντος (συμπεριλαμβανομένης της δοσολογικής μορφής και της δοσολογίας), του αριθμού παρτίδας και παρτίδας, της ποσότητας των προϊόντων που παραδόθηκαν, της τιμής του φαρμακευτικό προϊόν, το όνομα και τη διεύθυνση του προμηθευτή και του παραλήπτη, καθώς και έγγραφα που επιβεβαιώνουν την ποιότητα των φαρμάκων. Τα έγγραφα που επιβεβαιώνουν την ποιότητα των φαρμάκων είναι μια δήλωση συμμόρφωσης ή ένα πιστοποιητικό συμμόρφωσης Σημαντικός δείκτης είναι το γεγονός ότι μια αλυσίδα φαρμακείων ή φαρμακείων συνεργάζεται με έναν αξιόπιστο σύνδεσμο χονδρικής, γνωστές διεθνικές εταιρείες που έχουν τη δική τους «υπηρεσία ασφάλειας φαρμάκων». πολύ σοβαρά.
Ο έλεγχος αποδοχής, μαζί με τον έλεγχο της ορθότητας της γραφειοκρατίας, περιλαμβάνει την επαλήθευση των φαρμάκων με όρους "Περιγραφή", "Συσκευασία", "Ετικέτα", η οποία καθορίζεται από τις απαιτήσεις της εντολής του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας 16.07.97. Νο 214 «Περί ποιοτικού ελέγχου φαρμάκων που παρασκευάζονται σε οργανισμούς φαρμακείων (φαρμακεία)». Ο έλεγχος σύμφωνα με την ένδειξη "Περιγραφή" περιλαμβάνει έλεγχο εμφάνισης, χρώματος, μυρωδιάς. Η ασυνέπεια στο χρώμα, η παρουσία ξένης οσμής, ίζημα, νιφάδες, μηχανικά εγκλείσματα, κατάψυξη, αποκόλληση αποτελούν λόγους απόρριψης. Σε περίπτωση αμφιβολίας για την ποιότητα των φαρμάκων, τα δείγματα αποστέλλονται στο περιφερειακό κέντρο ποιοτικού ελέγχου των φαρμάκων. Τέτοια φάρμακα με την ονομασία: «Απορρίφθηκαν κατά τον έλεγχο αποδοχής» φυλάσσονται στο φαρμακείο χωριστά από άλλα φάρμακα. Ο έλεγχος από τον δείκτη «Συσκευασία» περιλαμβάνει έλεγχο της ακεραιότητας της συσκευασίας, της παρουσίας δευτερεύουσας συσκευασίας και της συμμόρφωσης της συσκευασίας με τις φυσικές και χημικές ιδιότητες των φαρμάκων.
2. Χώροι και εξοπλισμός.Οι βασικές απαιτήσεις για την οργάνωση της αποθήκευσης φαρμάκων και ιατρικών προϊόντων στα φαρμακεία καθορίζονται από την Οδηγία από την οργάνωση αποθήκευσης σε φαρμακεία διαφορετικών ομάδων φαρμάκων και ιατρικών προμηθειών. Τα φαρμακευτικά προϊόντα που απαιτούν ειδικές συνθήκες αποθήκευσης θα πρέπει να ταυτοποιούνται αμέσως και να τοποθετούνται στο κατάλληλο μέρος αποθήκες (ζώνες)σύμφωνα με τις απαιτήσεις της ισχύουσας νομοθεσίας. Ο χώρος αποθήκευσης σε ένα φαρμακείο θα πρέπει να είναι αρκετά μεγάλος ώστε να επιτρέπει την τακτική αποθήκευση διαφορετικών κατηγοριών υλικών και προϊόντων. Καθαρό και προστατευμένο. Τα φαρμακευτικά προϊόντα στις αποθήκες παραγωγής θα πρέπει να αποθηκεύονται σε ράφια, παλέτες, βάθρα, ντουλάπια, ψύξη και άλλο ειδικό εξοπλισμό ώστε να διασφαλίζονται οι συνθήκες αποθήκευσης για τα φαρμακευτικά προϊόντα σύμφωνα με τις ισχύουσες απαιτήσεις . Εάν η βάση του φαρμακείου (αποθήκη) διαθέτει ανοσοβιολογικά σκευάσματα, ο συνολικός όγκος του ψυκτικού εξοπλισμού πρέπει να διασφαλίζει, σύμφωνα με τις ισχύουσες απαιτήσεις, την αποθήκευση ολόκληρης της ποσότητας αυτών των φαρμάκων που περιέχεται στη βάση (αποθήκη). Κατά την αποθήκευση των φαρμάκων, ο κάτοχος της άδειας υποχρεούται να αποκλείει τη ζημιά τους (διαρροή, διαρροή, θραύση), μόλυνση από μικροοργανισμούς και διασταυρούμενη μόλυνση. Η αποθήκευση των φαρμάκων απαιτεί ειδικές συνθήκες θερμοκρασίας που ελέγχονται από συσκευές παρακολούθησης σταθερής θερμοκρασίας ή θερμικά δοχεία.
3. Προσωπικό. Όσον αφορά τους πόρους, ισχύει η τρίτη αρχή της διαχείρισης - αυτή είναι η συμμετοχή των εργαζομένων. Είναι οι εργαζόμενοι σε όλα τα επίπεδα που αποτελούν τη ραχοκοκαλιά του οργανισμού. Η πλήρης συμμετοχή τους επιτρέπει στον οργανισμό να αξιοποιήσει τις ικανότητές του. Αφενός, η διαχειριστική απόφαση της διοίκησης ότι το σύστημα διαχείρισης πρέπει να λειτουργεί, και αφετέρου, μόνο εάν όλο το προσωπικό αντιληφθεί ότι το σύστημα διαχείρισης δεν είναι απλώς μια συλλογή από πρόσθετα κομμάτια χαρτιού που θα σταθούν στο ράφι . Αυτή θα πρέπει να είναι μια αποτελεσματική δομή και θα λειτουργήσει μόνο όταν όλοι καταλάβουν σε τι βασίζεται και γιατί γίνεται. Σε κάθε φαρμακείο, με τη μία ή την άλλη μορφή, έχει δημιουργηθεί και λειτουργεί με επιτυχία ένα σύστημα διαχείρισης ποιότητας - για κάποιους κατά 10%, για άλλους κατά 90%.
4. ΤεκμηρίωσηΟι εργασίες που επηρεάζουν την ποιότητα των αγαθών θα πρέπει να περιγράφονται με γραπτές διαδικασίες. Το σύστημα διαχείρισης ποιότητας στοχεύει στη συστηματοποίηση των διαδικασιών, για να διαπιστωθεί εάν σε όλες παρέχονται οι απαραίτητοι πόροι και έγγραφα. Είναι σημαντικό να γνωρίζουμε εάν όλες οι διαδικασίες έχουν τεκμηριωμένες διαδικασίες και κανόνες εκτέλεσης. Απαιτείται η διαδικασία ανάλυσης και βελτίωσης προκειμένου να ληφθούν αποφάσεις διαχείρισης βασισμένες σε γεγονότα - αυτή είναι η έβδομη αρχή διαχείρισης των προτύπων ISO. Οι αποτελεσματικές αποφάσεις βασίζονται στην ανάλυση δεδομένων και πληροφοριών.
7. Επιστροφές. Δεν επιτρέπεται η παρουσία σε κυκλοφορία φαρμάκων χαμηλής ποιότητας ή ψευδεπίγραφων, εξαιρουμένων αυτών των οποίων η ημερομηνία λήξης έχει παρέλθει. Έχοντας αποκαλύψει το γεγονός της παρουσίας φαρμάκων χαμηλής ποιότητας, πλαστών και παρόμοιων φαρμάκων, μια επιχειρηματική οντότητα πρέπει να συντάξει κατάλληλη πράξη και να λάβει μέτρα για τον αποκλεισμό τους από την κυκλοφορία. Ο αποκλεισμός από την κυκλοφορία τέτοιων φαρμακευτικών προϊόντων γίνεται με ανακύκλωση και καταστροφή σύμφωνα με τους Κανόνες για την Απόρριψη Φαρμακευτικών Προϊόντων. Η διαδικασία χειρισμού επιστολών από τη Roszdravnador σχετικά με τα απορριφθέντα και παραποιημένα προϊόντα για τους ειδικούς του Κέντρου αναπτύχθηκε σύμφωνα με τις απαιτήσεις και τα έντυπα που καθορίζονται στην επιστολή της Ομοσπονδιακής Υπηρεσίας Εποπτείας της Υγείας και Κοινωνικής Ανάπτυξης της 28ης Σεπτεμβρίου 2004. αριθμ. 4082/04.
5. Βελτιστοποίηση του συστήματος διαχείρισης ποιότητας για φαρμακευτικές δραστηριότητες σε ένα φαρμακείο
Ως αποτέλεσμα της μελέτης της βιβλιογραφίας σχετικά με τη διαχείριση ποιότητας των ιατρικών προϊόντων, μπορεί να προταθεί η βελτιστοποίηση των δραστηριοτήτων των φαρμακευτικών οργανισμών εισάγοντας τις ακόλουθες αρχές:
Η ποιότητα της διαχείρισης είναι μια πολύπλευρη έννοια, περιλαμβάνει πολλά στοιχεία, όπως: διαφάνεια και δυνατότητα ελέγχου των διαδικασιών, ποιότητα πληροφοριών, δυνατότητα λειτουργικού ελέγχου των τρεχουσών δραστηριοτήτων και πολλά άλλα. Ταυτόχρονα, διάφορα έγγραφα χρησιμεύουν ως πρακτικά το μόνο εργαλείο διαχείρισης. Έτσι, ο προφανής τρόπος αλλαγής της ποιότητας της διαχείρισης της επιχείρησης είναι η βελτίωση της αποτελεσματικότητας της εργασίας με έγγραφα.
Η διαχείριση της ποιότητας του φαρμακείου βασίζεται στις ακόλουθες αρχές:
Επαρκής ποικιλία και όγκος σε προσιτές τιμές
Το καθήκον του φαρμακείου δεν είναι άλλο από την παροχή στον πληθυσμό φαρμάκων και προϊόντων φαρμακείου στο σωστό μέρος και σε κατάλληλη στιγμή για τους επισκέπτες, για τον οποίο καθορίζονται οι ανάγκες, συντάσσεται ο προμηθευτής, υποβάλλεται αίτηση, γίνεται αγορά και η δοσολογία μελετάται.
κοινωνική προσβασιμότητα
Διεξαγωγή έρευνας για το εύρος εντός συνωνύμων και αναλόγων. Υπάρχουν περισσότερες από μία εμπορικές ονομασίες μιας δραστικής ουσίας στο φαρμακείο. Οι εμπορικές ονομασίες μερικές φορές ποικίλλουν κατά 100–700%, ανάλογα με τον κατασκευαστή. Το φαρμακείο αγοράζει διάφορες εμπορικές ονομασίες με διαφορετικά επίπεδα για να εξασφαλίσει κοινωνική προσβασιμότητα σε διαφορετικές κοινωνικές ομάδες επισκεπτών. Σε μία φαρμακοθεραπευτική ομάδα, μπορείτε να πάρετε ακριβά, μεσαίου και χαμηλού κόστους φάρμακα.
- Ενημερωτική και συμβουλευτική υποστήριξη
Οι εργαζόμενοι στα φαρμακεία πρέπει να προβλέπουν τις προσδοκίες του καταναλωτή και να διασφαλίζουν ότι το προϊόν ανταποκρίνεται σε αυτές τις προσδοκίες. Δεν είναι πάντα δυνατό. Για παράδειγμα, ένας καταναλωτής θέλει να λάβει συμβουλές από έναν φαρμακοποιό πριν αγοράσει ένα φάρμακο. Όμως ένας φαρμακοποιός δεν είναι γιατρός και δεν φέρει καμία νομική ευθύνη για την υγεία ενός ασθενούς στη χώρα μας. Ωστόσο, μη λαμβάνοντας το αναμενόμενο, ο καταναλωτής παραμένει δυσαρεστημένος.
- Εφαρμογή υπολογιστικών συστημάτων στα φαρμακεία και χρήση barcodes στον ποιοτικό έλεγχο φαρμάκων στα φαρμακεία
Το σύστημα αυτοματισμού μιας επιχείρησης φαρμακείου διαφέρει από τα συστήματα αυτοματισμού των εμπορικών επιχειρήσεων. Τα φαρμακεία έχουν πολλές δικές τους ιδιαιτερότητες, που σχετίζονται κυρίως με την τιμολόγηση, η οποία στη Ρωσία ήταν πάντα μια πολύπλοκη και συγκεχυμένη διαδικασία. Η τιμολόγηση σε ένα φαρμακείο πραγματοποιείται σύμφωνα με ορισμένα νομοθετικά έγγραφα και ρυθμίζεται αυστηρά, υπάρχει κατάλογος φαρμάκων που δεν φορολογούνται. Για τέτοια φάρμακα, η λιανική τιμή διαμορφώνεται διαφορετικά. Παλαιότερα, για τους εργαζόμενους στα φαρμακεία, η διαδικασία παραλαβής αγαθών και καταχώρησης τιμών ήταν χρονοβόρα και χρονοβόρα. Επομένως, η αυτοματοποίηση είναι απλώς απαραίτητη εδώ.
Τα συστήματα αυτοματισμού επιτρέπουν στους εργαζόμενους στα φαρμακεία να βλέπουν δεδομένα σχετικά με το τι υπάρχει σε απόθεμα, ποια φάρμακα έχουν εξαντληθεί και τι πρέπει να αγοραστεί επιπλέον. Η διαδικασία γρήγορης προβολής πραγματικών υπολοίπων είναι μία από τις πιο σημαντικές κατά την επιλογή ενός συστήματος αυτοματισμού.
Σε κάθε συνηθισμένο φαρμακείο, όπου υπάρχει απλή ταμειακή μηχανή, όταν κάνουμε μια αγορά, τα χρήματα που πληρώνουμε στο ταμείο δεν σχετίζονται άμεσα με το προϊόν που λαμβάνουμε.
Και εδώ προκύπτουν αμέσως πολλά προβλήματα:
Πρώτον, το φαρμακείο δεν έχει πλήρη και λεπτομερή καταγραφή της κίνησης των αγαθών και των οικονομικών πόρων. Είναι αδύνατο, για παράδειγμα, να πούμε ανά πάσα στιγμή πόσο από ένα δεδομένο προϊόν πωλήθηκε, παρέμεινε στον χώρο συναλλαγών ή στην αποθήκη, είναι αδύνατο να απαγορευτεί αυτόματα η διάτρηση ενός προϊόντος που έχει ήδη τελειώσει κ.λπ.
Δεύτερον, είναι δύσκολο να αποφευχθούν τα λάθη που μπορεί να κάνει ο ταμίας.
Τρίτον, η έλλειψη λεπτομερούς λογιστικής καθιστά αδύνατη τη διεξαγωγή στατιστικών στοιχείων και τη λεπτομερή ανάλυση της δυναμικής των πωλήσεων, γεγονός που καθιστά δύσκολη την πιο ευέλικτη ανταπόκριση στις αλλαγές της ζήτησης.
6. Ανάλυση και τρόποι βελτίωσης του συστήματος διαχείρισης ποιότητας των φαρμάκων στο φαρμακείο της MAIR LLC
Η MAIR LLC δραστηριοποιείται στη φαρμακευτική αγορά για περισσότερα από 15 χρόνια στην Επικράτεια Primorsky. Η αλυσίδα φαρμακείων της περιλαμβάνει 5 καταστήματα λιανικής και είναι πολύ δημοφιλής - αρκετές χιλιάδες κάτοικοι του Βλαδιβοστόκ έχουν κάρτες επιβράβευσης. Καταλαμβάνει τον δεύτερο όροφο διώροφης οικοδομής. Το φαρμακείο είναι καινούργιο, λειτουργεί από τον Μάιο του 2010, πληροί όλες τις προϋποθέσεις επιστημονικής και τεχνικής τεκμηρίωσης και υγειονομικών προδιαγραφών, είναι ανοιχτό από τις 9:00 έως τις 20:00 επτά ημέρες την εβδομάδα. Υπάρχουν πινακίδες με το όνομα του φαρμακείου και τις ώρες λειτουργίας. Βρίσκεται σε βολικό σημείο για τους επισκέπτες, κοντά στη στάση του λεωφορείου.
Η Mair θεωρεί ότι η κύρια αποστολή της δεν είναι τόσο η πώληση φαρμάκων, η πώληση φαρμάκων και φαρμάκων, ιατρικών προϊόντων, αλλά η παροχή φαρμακευτικών υπηρεσιών σε υψηλό επίπεδο, επομένως η εταιρεία προσπαθεί να επικεντρωθεί στον πελάτη, να εγγυηθεί την ποιότητα φάρμακα και να εξυπηρετούν όσο το δυνατόν καλύτερα τον αγοραστή. Όλα αυτά, μαζί με μια κατανοητή επιθυμία να κάνουν τη δουλειά τους πιο αποτελεσματική, έκαναν τη διοίκηση να σκεφτεί την εφαρμογή ενός συστήματος διαχείρισης ποιότητας.
Δουλεύοντας σε ένα σύστημα διαχείρισης ποιότητας για λιγότερο από ένα χρόνο, ένα φαρμακείο μπορεί να βγάλει κάποια συμπεράσματα. Οι αντικειμενικοί δείκτες επιβεβαιώνουν ότι η εισαγωγή του συστήματος διαχείρισης ποιότητας συνέβαλε στη βελτιστοποίηση του κεφαλαίου κίνησης: αυξήθηκε ο όγκος πωλήσεων στα φαρμακεία της αλυσίδας, μειώθηκε ο αριθμός των προϊόντων χαμηλού εισοδήματος και μη ρευστοποιήσιμων, καθώς και των ληγμένων προϊόντων. Ο αριθμός των τακτικών πελατών έχει αυξηθεί. Η ανάλυση της ζήτησης, των επιθυμιών και των προτάσεών τους κατέστησε δυνατή την ουσιαστική απαλλαγή από ελαττώματα. Επιπλέον, λόγω του προσανατολισμού του προσωπικού προς τη συνεργασία με πελάτες, όχι μόνο ο αριθμός των διαδικτυακών αγορών έχει αυξηθεί σημαντικά, αλλά το μέσο κόστος τους έχει βελτιστοποιηθεί. Οι ειδικοί στη διαχείριση ποιότητας σημειώνουν τώρα ότι ο κύριος και πιο προβληματικός κρίκος σε οποιαδήποτε δομή διαχείρισης είναι οι άνθρωποι. Στην περίπτωσή μας είναι φαρμακοποιοί. Αυτοί που βρίσκονται σε άμεση επαφή με πελάτες, επισκέπτες, καταναλωτές. Για την εισαγωγή ενός συστήματος διαχείρισης ποιότητας στο φαρμακείο, έγιναν κάποιες αλλαγές στην οργανωτική δομή και στις σχέσεις στην ομάδα. Ένα αποτελεσματικό σύστημα εκπαίδευσης προσωπικού και η συνεχής παρακολούθηση της εκπαίδευσης έχουν βελτιώσει την ποιότητα της εργασίας του προσωπικού.
1. Ως αποτέλεσμα της ανάλυσης δεδομένων από ξένη και εγχώρια βιβλιογραφία, διαπιστώθηκε ότι δίνεται μεγάλη προσοχή στα ζητήματα του συστήματος διαχείρισης ποιότητας για φάρμακα σε φαρμακολογικά ιδρύματα τόσο στη Ρωσία όσο και στο εξωτερικό. Κατά τη μελέτη των βασικών εννοιών για την κατασκευή μοντέλων και τη λειτουργία συστημάτων διαχείρισης ποιότητας, προσεγγίσεις που βασίζονται στην έννοια της διαχείρισης ολικής ποιότητας (TQM) και των προτύπων της σειράς ISO 9000 επιδεικνύουν μια ξεκάθαρη ηγεσία, παρέχοντας μια σειρά από γενικές αρχές: προσανατολισμός προς τον πελάτη, ηγεσία διαχείρισης, προσέγγιση επεξεργαστή, προσέγγιση συστημάτων, συνεχής βελτίωση, αμοιβαία επωφελείς σχέσεις με προμηθευτές κ.λπ.
2. Το σύστημα διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων στη Ρωσία καθορίζεται από τον ομοσπονδιακό νόμο αριθ. βιομηχανικά πρότυπα: OST91500.05.0005-2002 "Κανόνες για το χονδρικό εμπόριο φαρμάκων. Βασικές διατάξεις", που εγκρίθηκε με εντολή του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 15.03.2002 Αρ. 80. ΟΣΤ 91500.05.0007-2003.
3. Σύμφωνα με τη διεθνή πρακτική, το φαρμακείο είναι πλήρως υπεύθυνο για την ποιότητα των προϊόντων που αγοράζονται από προμηθευτές, μόνο οι υποχρεωτικές απαιτήσεις για τα προϊόντα καθορίζονται από το νόμο και όλοι οι άλλοι όροι αποτελούν αντικείμενο διαπραγμάτευσης σε συμφωνία μεταξύ των συμμετεχόντων στην αγορά.
4. Το σύστημα διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων πρέπει να είναι αξιόπιστο, προληπτικό, να μην επιτρέπει την παροχή χαμηλής ποιότητας φαρμακευτικών υπηρεσιών στον καταναλωτή, καθώς και εξατομικευμένο, δηλ. έχει συγκεκριμένα άτομα υπεύθυνα για αυτό.
5. Θεωρούνται ορισμένες αρχές που επιτρέπουν τη βελτιστοποίηση του συστήματος διαχείρισης ποιότητας στον τομέα της κυκλοφορίας των φαρμάκων σε ένα φαρμακείο Μελετώντας τη βιβλιογραφία για τη διαχείριση ποιότητας του LP, μπορούμε να προτείνουμε τη βελτιστοποίηση των δραστηριοτήτων των φαρμακευτικών οργανισμών εισάγοντας τις ακόλουθες αρχές.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Διάταγμα του Υπουργείου Υγείας της Ρωσικής Ομοσπονδίας της 03/04/2003. Αρ. 80 «Περί έγκρισης του βιομηχανικού προτύπου «Κανόνες για τη διανομή (πώληση) φαρμακευτικών προϊόντων σε οργανισμούς φαρμακείων. Βασικές Διατάξεις».
2. Skulkova R.S., Yagudina R.I., Parkhomenko D.V. Διαμόρφωση συστήματος διαχείρισης ποιότητας για οργανισμούς φαρμακείων. Νέο φαρμακείο. Κανονισμοί. 2005.-Ν 4.-Σ.32-37.
3. Komissinskaya I. G. Η σύγχρονη έννοια της διαχείρισης ποιότητας ενός φαρμακευτικού οργανισμού // Moscow apteki. - 2007. - Νο. 11.
4. Alferova, T.V. Διαχείριση παραγωγής στις επιχειρήσεις της φαρμακευτικής βιομηχανίας / T.V. Alferova, E.A. Tretyakova, A.V. Buylin. - Αικατερινούπολη: Εκδοτικός Οίκος του Ινστιτούτου Οικονομικών Επιστημών του Παραρτήματος Ουραλίων της Ρωσικής Ακαδημίας Επιστημών, 2008. - 214σ.
5. Moskvin V.A. Εξέλιξη στον τομέα της διαχείρισης ποιότητας / V.A. Moskvin // Investments in Russia.2004. Νο. 5.- Σ. 27-28.
6. Lagutkina T.P. Αρχές διαχείρισης ποιότητας στις δραστηριότητες ενός οργανισμού φαρμακείου // Δελτίο του Πανεπιστημίου Φιλίας των Λαών της Ρωσίας. 2008.-Ν 4.-Σ.36-39.
7. Polessky V.A. Εξέλιξη μοντέλων συστημάτων ποιότητας: διεθνής πρακτική / V.A. Polessky, S.A. Martynchik, V.G. Zaporozhchenko, V.Z. Kucherenko // Οικονομικά της Υγείας. - 2005. - Νο. 8. - Σ. 25-36.
8. Ομοσπονδιακός νόμος "Για τα φάρμακα" αριθ. 86-FZ της 22/06/98
9. Drugova Z.K., Biteryakova A.M. Σύστημα εσωτερικού ελέγχου και ποιότητα διαχείρισης // Ρωσικά φαρμακεία. – №2. – 2007.
10. Kononova S.V. Σύστημα διασφάλισης ποιότητας για φαρμακευτικές υπηρεσίες στο περιφερειακό φαρμακευτικό συγκρότημα: Μονογραφία. - Nizhny Novgorod: Εκδοτικός Οίκος VGIPA, 2003.
11. Συνθήκες αποθήκευσης των φαρμακευτικών προϊόντων. - Μ.: Ιατρική, 2006. - 184 σελ.
12. Kulaev V.A., Egorov V.A., Gladunova E.P., Ezhkov V.N. Ολοκληρωμένο σύστημα διαχείρισης ποιότητας για τη φαρμακευτική φροντίδα // Pharmacy, 2011, No. 3, C. 30-33
I. Έλεγχος αποδοχής
ένα. Ο έλεγχος αποδοχής διενεργείται προκειμένου να αποτραπεί η παραλαβή φαρμάκων χαμηλής ποιότητας στο φαρμακείο.
σι. Ο έλεγχος αποδοχής συνίσταται στον έλεγχο των εισερχόμενων φαρμάκων για συμμόρφωση με τις απαιτήσεις όσον αφορά: «Περιγραφή». "Πακέτο"; "Βαθμολόγηση"; στον έλεγχο της ορθότητας της καταχώρισης των εγγράφων διακανονισμού (λογαριασμών), καθώς και της διαθεσιμότητας πιστοποιητικών συμμόρφωσης του κατασκευαστή και άλλων εγγράφων που επιβεβαιώνουν την ποιότητα των φαρμάκων σύμφωνα με την τρέχουσα κανονιστικά έγγραφα.
Εγώ. Ο έλεγχος σύμφωνα με την ένδειξη "Περιγραφή" περιλαμβάνει έλεγχο εμφάνισης, χρώματος, μυρωδιάς. Σε περίπτωση αμφιβολίας για την ποιότητα των φαρμάκων, τα δείγματα αποστέλλονται στο εργαστήριο εδαφικού ελέγχου και ανάλυσης. Τέτοια φάρμακα με την ονομασία: «Απορρίφθηκε κατά τον έλεγχο αποδοχής» φυλάσσονται σε φαρμακείο απομονωμένο από άλλα φάρμακα.
ii. Κατά τον έλεγχο του δείκτη «Συσκευασία», δίνεται ιδιαίτερη προσοχή στην ακεραιότητά του και στη συμμόρφωσή του με τις φυσικές και χημικές ιδιότητες των φαρμάκων.
iii. Κατά τον έλεγχο για τον δείκτη "Ετικέτα", εφιστάται η προσοχή στη συμμόρφωση του σχεδιασμού των φαρμάκων με τις τρέχουσες απαιτήσεις.
iv. Ιδιαίτερη προσοχήθα πρέπει να δώσετε προσοχή στη συμμόρφωση της επισήμανσης της κύριας, δευτερογενούς και ομαδικής συσκευασίας, στην παρουσία φυλλαδίου στα ρωσικά στη συσκευασία (ή χωριστά σε συσκευασία για ολόκληρο τον αριθμό των τελικών φαρμακευτικών προϊόντων).
v. Στις ετικέτες της συσκευασίας με φαρμακευτικές ουσίες που προορίζονται για την παρασκευή ενέσιμων διαλυμάτων και διαλυμάτων έγχυσης, πρέπει να υπάρχει η ένδειξη «Καλό για ενέσιμα». Οι συσκευασίες με δηλητηριώδη και ναρκωτικά φάρμακα πρέπει να εκδίδονται σύμφωνα με τις απαιτήσεις της νομοθεσίας της Ρωσικής Ομοσπονδίας και των κανονιστικών εγγράφων.
vi. Τα φαρμακευτικά φυτικά υλικά που λαμβάνονται από τον πληθυσμό ελέγχονται σύμφωνα με τον δείκτη " Εξωτερικά σημάδια» σύμφωνα με τις απαιτήσεις της Κρατικής Φαρμακοποιίας ή του ισχύοντος κανονιστικού εγγράφου, μετά την οποία αποστέλλεται για ανάλυση στο εργαστήριο εδαφικού ελέγχου και ανάλυσης.
II. Προληπτικά μέτρα
1. Τα προληπτικά μέτρα συνίστανται στην εκπλήρωση των ακόλουθων απαιτήσεων:
ένα. Συμμόρφωση με τους υγειονομικούς κανόνες και κανόνες. αντιεπιδημικό καθεστώς, καθώς και τις προϋποθέσεις για την άσηπτη παρασκευή φαρμάκων σύμφωνα με τα ισχύοντα κανονιστικά έγγραφα.
σι. Συμμόρφωση με τους κανόνες για τη λήψη, τη συλλογή και την αποθήκευση καθαρού νερού, νερού για ένεση. έγκαιρη αποχέτευση του αγωγού · έλεγχος της έγκαιρης απόσυρσης αποστειρωμένων διαλυμάτων, καθαρού νερού, ενέσιμου νερού για έλεγχο στειρότητας σύμφωνα με τις ισχύουσες απαιτήσεις.
2. Οι συλλογές για κεκαθαρμένο νερό, ενέσιμο νερό πρέπει να φέρουν καθαρή επιγραφή: «Καθαρισμένο νερό», «Νερό για έγχυση». Στον συλλέκτη νερού επικολλάται μια ετικέτα που αναφέρει την ημερομηνία παραλαβής του, τον αριθμό της ανάλυσης και την υπογραφή του επιθεωρητή. Όταν χρησιμοποιείτε πολλές συλλογές ταυτόχρονα, πρέπει να είναι αριθμημένες.
ένα. Εξασφάλιση της λειτουργικότητας και της ακρίβειας των οργάνων, των συσκευών και των εγκαταστάσεων ζύγισης, της κανονικότητας των ελέγχων τους.
σι. Προσεκτική εξέταση των συνταγών που λαμβάνονται από το φαρμακείο και των απαιτήσεων των ιατρικών οργανώσεων προκειμένου να επαληθευτεί η ορθότητα της συνταγογράφησης τους. συμβατότητα των ουσιών που απαρτίζουν τα φάρμακα· τη συμμόρφωση των συνταγογραφούμενων δόσεων με την ηλικία του ασθενούς και τη διαθεσιμότητα οδηγιών για τον τρόπο χρήσης φαρμάκων.
ντο. Συμμόρφωση με την τεχνολογία των φαρμάκων (συμπεριλαμβανομένων των ομοιοπαθητικών) σύμφωνα με τις απαιτήσεις της ισχύουσας Κρατικής Φαρμακοποιίας, κανονιστικά έγγραφα, οδηγίες.
ρε. Διασφάλιση των συνθηκών αποθήκευσης των φαρμάκων στο φαρμακείο σύμφωνα με τους ΦΥΣΙΚΕΣ ΚΑΙ ΧΗΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣκαι τις απαιτήσεις της Κρατικής Φαρμακοποιίας, ισχύοντα κανονιστικά έγγραφα.
Εγώ. Στους χώρους αποθήκευσης, σε όλες τις μπάρες με φάρμακα, πρέπει να αναγράφονται τα ακόλουθα: ο αύξων αριθμός του κατασκευαστή, ο αριθμός ανάλυσης του εργαστηρίου ελέγχου και ανάλυσης (το κέντρο ποιοτικού ελέγχου φαρμάκων), η ημερομηνία λήξης, η ημερομηνία γέμισμα και την υπογραφή που γέμιζε τη μπάρα. Ο αριθμός των μονάδων δράσης σε ένα γραμμάριο φαρμακευτικού φυτικού υλικού ή σε ένα χιλιοστόλιτρο του φαρμακευτικού προϊόντος πρέπει να αναγράφεται στις μπάρες με φάρμακα που περιέχουν καρδιακές γλυκοσίδες.
ii. Στα δωμάτια του βοηθού σε όλες τις μπάρες με φαρμακευτικές ουσίες πρέπει να αναγράφονται: η ημερομηνία πλήρωσης, η υπογραφή του ατόμου που συμπλήρωσε τη μπάρα και επαλήθευσε τη γνησιότητα της φαρμακευτικής ουσίας. Οι υψηλότερες εφάπαξ και ημερήσιες δόσεις πρέπει να αναγράφονται στις ράβδους με τοξικές και ισχυρές φαρμακευτικές ουσίες και η προειδοποιητική ετικέτα "Για στείρες δοσολογικές μορφές" πρέπει να αναγράφεται στις ράβδους με φαρμακευτικές ουσίες που προορίζονται για την παρασκευή στείρων δοσολογικών μορφών.
iii. Τα βαρέλια με διαλύματα, βάμματα και υγρά ημικατεργασμένα προϊόντα πρέπει να παρέχονται με κανονικά σταγονόμετρα ή σιφώνια. Ο αριθμός των σταγόνων σε έναν συγκεκριμένο όγκο πρέπει να προσδιορίζεται με ζύγιση και να αναγράφεται στη ράβδο.
iv. Η πλήρωση ενός στελέχους γυαλιού, μιας προχοΐδας σε ρύθμιση προχοΐδας, ενός στελέχους γυαλιού με κανονικό σταγονόμετρο ή μιας πιπέτας πρέπει να πραγματοποιείται μόνο μετά από πλήρη χρήσηφαρμακευτικό προϊόν και την αντίστοιχη θεραπεία της μπάρας.
μι. Η ονοματολογία των συμπυκνωμάτων, των ημικατεργασμένων προϊόντων και των ενδοφαρμακευτικών παρασκευασμάτων φαρμάκων που παρασκευάζονται σε φαρμακεία πρέπει να εγκρίνεται από το εργαστήριο εδαφικού ελέγχου και ανάλυσης και να τίθεται υπόψη όλων των φαρμακείων της αντίστοιχης επικράτειας. Αυτή η λίστα μπορεί να περιλαμβάνει μόνο συνταγές που περιέχουν συμβατές φαρμακευτικές ουσίες για τις οποίες υπάρχουν μέθοδοι ανάλυσης για χημικό έλεγχο *.
φά. Οι υπεύθυνοι φαρμακείων πρέπει να παρακολουθούν τη συμμόρφωση με τους κανόνες για την αποθήκευση φαρμάκων στα τμήματα των ιατρικών οργανώσεων που συνδέονται με το φαρμακείο μία φορά το τρίμηνο.
3. Στα τμήματα των ιατρικών οργανώσεων δεν επιτρέπεται η παρασκευή φαρμάκων, η συσκευασία, η μεταφορά από το ένα δοχείο (πακέτο) στο άλλο και η αντικατάσταση ετικετών. Τα φάρμακα πρέπει να φυλάσσονται στα τμήματα μόνο στην αρχική (εργοστασιακή, εργοστασιακή ή φαρμακείο) συσκευασία.
4. Για τον έλεγχο της ημερομηνίας λήξης στη συσκευασία της συσκευασίας που χορηγείται από το φαρμακείο στο τμήμα του ιατρικού οργανισμού, πρέπει να αναγράφεται η σειρά του κατασκευαστή.
5. Τα φαρμακευτικά προϊόντα από φαρμακεία σε ιατρικούς οργανισμούς θα πρέπει να διανέμονται μόνο σε εξουσιοδοτημένο ιατρικό προσωπικό.
III. Γραπτός έλεγχος
1. Κατά την κατασκευή δοσολογικών μορφών σύμφωνα με συνταγές και απαιτήσεις ιατρικών οργανισμών, συμπληρώνονται γραπτά διαβατήρια ελέγχου. Το διαβατήριο πρέπει να περιέχει: την ημερομηνία κατασκευής, τον αριθμό της συνταγής (αριθμό του ιατρικού οργανισμού, το όνομα του τμήματος), το όνομα των φαρμακευτικών ουσιών που λαμβάνονται και τις ποσότητες τους, τον αριθμό των δόσεων, την υπογραφή του πρόσωπο που κατασκεύασε, συσκεύασε και έλεγξε τη δοσολογική μορφή. Στην περίπτωση παρασκευής δοσολογικής μορφής, ο ασκούμενος υπογράφει τον υπεύθυνο για την παραγωγική πρακτική.
2. Όλοι οι υπολογισμοί πρέπει να γίνονται πριν από την παρασκευή της δοσολογικής μορφής και να καταγράφονται στις αντιθετη πλευραδιαβατήρια. Το διαβατήριο συμπληρώνεται αμέσως μετά την κατασκευή του δοσολογικού εντύπου, από μνήμης, και μετά λατινικά, σύμφωνα με τη σειρά των τεχνολογικών λειτουργιών. Κατά τη συμπλήρωση διαβατηρίου για ομοιοπαθητικό δοσολογικές μορφέςαναφέρονται οι ομοιοπαθητικές ονομασίες των διαδοχικών λαμβανόμενων φαρμάκων.
3. Σε περίπτωση χρήσης ημικατεργασμένων προϊόντων και συμπυκνωμάτων, η σύσταση, η συγκέντρωση, ο λαμβανόμενος όγκος ή η μάζα τους αναγράφονται στο διαβατήριο. Στην παρασκευή σκονών, υπόθετων και χαπιών, υποδεικνύεται το συνολικό βάρος, η ποσότητα και το βάρος των μεμονωμένων δόσεων. Το συνολικό βάρος των χαπιών ή των υπόθετων, η συγκέντρωση και ο όγκος (ή το βάρος) των ισοτονωτικών και σταθεροποιητικών ουσιών που προστίθενται σε οφθαλμικές σταγόνες, διαλύματα για ενέσιμα και εγχύσεις, πρέπει να αναγράφονται όχι μόνο στα διαβατήρια, αλλά και στις συνταγές.
4. Το διαβατήριο πρέπει να αναφέρει τους τύπους υπολογισμού και τους συντελεστές απορρόφησης νερού που χρησιμοποιούνται για φαρμακευτικά φυτικά υλικά, τους συντελεστές αύξησης του όγκου των διαλυμάτων κατά τη διάλυση φαρμακευτικών ουσιών, τους συντελεστές υποκατάστασης για την κατασκευή υπόθετων.
5. Η διατήρηση γραπτών διαβατηρίων ελέγχου είναι επίσης απαραίτητη εάν οι δοσολογικές μορφές κατασκευάζονται και διανέμονται από το ίδιο άτομο. Στην περίπτωση αυτή, το διαβατήριο συμπληρώνεται κατά την κατασκευή του δοσολογικού εντύπου.
6. Τα διαβατήρια γραπτού ελέγχου φυλάσσονται στο φαρμακείο για δύο μήνες από την ημερομηνία παρασκευής του φαρμακευτικού προϊόντος.
7. Τα παρασκευασμένα φάρμακα, οι συνταγές και τα συμπληρωμένα διαβατήρια υποβάλλονται για επαλήθευση σε φαρμακοποιό που ασκεί ελεγκτικές λειτουργίες στην παρασκευή και τη διανομή φαρμάκων (εφεξής «φαρμακοποιός-τεχνολόγος»). Ο έλεγχος συνίσταται στον έλεγχο της συμμόρφωσης των εγγραφών στο διαβατήριο με τον γραπτό έλεγχο της συνταγής στη συνταγή, την ορθότητα των υπολογισμών που έγιναν. Εάν διενεργείται πλήρης χημικός ποιοτικός έλεγχος του φαρμακευτικού προϊόντος από φαρμακοποιό-αναλυτή, τότε στο διαβατήριο τίθεται ο αριθμός της ανάλυσης και η υπογραφή του φαρμακοποιού-αναλυτή.
8. Στην παρασκευή συμπυκνωμάτων, ημικατεργασμένων προϊόντων, ενδοφαρμακευτικής προμήθειας και συσκευασίας φαρμάκων, γίνονται όλες οι εγγραφές στα λογιστικά βιβλία για εργαστηριακές και συσκευαστικές εργασίες.
IV. Έλεγχος δημοσκοπήσεων
1. Ο έλεγχος δημοσκόπησης εφαρμόζεται επιλεκτικά. Πραγματοποιείται μετά την παρασκευή από φαρμακοποιό όχι περισσότερες από πέντε δοσολογικές μορφές.
2. Κατά τη διεξαγωγή ενός ελέγχου έρευνας, ο φαρμακοποιός-τεχνολόγος ονομάζει την πρώτη ουσία που περιλαμβάνεται στη δοσολογική μορφή και σε δοσολογικές μορφές μιας σύνθετης σύνθεσης υποδεικνύει επίσης την ποσότητα της, μετά την οποία ο φαρμακοποιός ονομάζει όλες τις φαρμακευτικές ουσίες που λαμβάνονται και τις ποσότητες τους. Όταν χρησιμοποιούνται ημικατεργασμένα προϊόντα (συμπυκνώματα), ο φαρμακοποιός ονομάζει επίσης τη σύνθεση και τη συγκέντρωσή τους.
1. Κατ' εξαίρεση, η παρασκευή αρωματικών νερών, ενδοφαρμακευτικών παρασκευασμάτων φαρμάκων εξωτερικής χρήσης που περιέχουν πίσσα, ιχθυόλη, θείο, έλαιο Naftalan, κολλόδιο, μόλυβδο, καθώς και ομοιοπαθητικά φάρμακα των οποίων η ανάλυση δεν μπορεί να γίνει. σε φαρμακείο, πραγματοποιείται υπό την επίβλεψη φαρμακοποιού που ασχολείται με τον ποιοτικό έλεγχο φαρμάκων.
V. Οργανοληπτικός έλεγχος
1. Ο οργανοληπτικός έλεγχος συνίσταται στον έλεγχο της δοσολογικής μορφής (συμπεριλαμβανομένης της ομοιοπαθητικής) ως προς: «Περιγραφή» (εμφάνιση, χρώμα, οσμή), ομοιομορφία, απουσία ορατών μηχανικών εγκλεισμάτων (σε υγρές δοσολογικές μορφές). Η γεύση ελέγχεται επιλεκτικά σε δοσολογικές μορφές που προορίζονται για παιδιά.
2. Η ομοιογένεια σκονών, ομοιοπαθητικών κονιοποιήσεων, αλοιφών, χαπιών, υπόθετων ελέγχεται σύμφωνα με τις απαιτήσεις της Κρατικής Φαρμακοποιίας, ισχύοντα κανονιστικά έγγραφα. Ο έλεγχος πραγματοποιείται επιλεκτικά σε κάθε φαρμακοποιό κατά τη διάρκεια της εργάσιμης ημέρας, λαμβάνοντας υπόψη διάφορα είδηδοσολογικές μορφές.
3. Τα αποτελέσματα του οργανοληπτικού ελέγχου των δοσολογικών μορφών καταγράφονται στο περιοδικό σύμφωνα με το συνημμένο έντυπο (Παράρτημα 2 στο της παρούσας Οδηγίας).
VI. Φυσικός έλεγχος
1. Ο φυσικός έλεγχος συνίσταται στον έλεγχο της συνολικής μάζας ή όγκου της δοσολογικής μορφής, του αριθμού και της μάζας των μεμονωμένων δόσεων (τουλάχιστον τρεις δόσεις) που περιλαμβάνονται σε αυτήν τη δοσολογική μορφή.
2. Έλεγξε:
3. Κάθε σειρά τεμαχίων συσκευασίας και ενδοφαρμακευτικής συσκευασίας σε ποσότητα τουλάχιστον τριών συσκευασιών (συμπεριλαμβανομένων των συσκευασιών βιομηχανικών προϊόντων και ομοιοπαθητικών φαρμάκων).
4. Δοσολογικές μορφές που παρασκευάζονται σύμφωνα με μεμονωμένες συνταγές (απαιτήσεις), επιλεκτικά κατά τη διάρκεια της εργάσιμης ημέρας, λαμβάνοντας υπόψη διαφορετικούς τύπους δοσολογικών μορφών, αλλά όχι λιγότερο από το 3% του αριθμού των μορφών δοσολογίας που παρασκευάζονται ανά ημέρα.
5. Κάθε σειρά δοσολογικών μορφών που απαιτούν αποστείρωση, μετά τη συσκευασία πριν από την αποστείρωσή τους σε ποσότητα τουλάχιστον πέντε φιαλιδίων (φιαλίδια).
6. τον αριθμό των ομοιοπαθητικών κόκκων σε ένα συγκεκριμένο βάρος δείγματος σύμφωνα με τις απαιτήσεις των ισχυόντων κανονιστικών εγγράφων.
7. Αποτελέσματα σωματικός έλεγχοςκαταχωρούνται στο περιοδικό σύμφωνα με το συνημμένο έντυπο (Παράρτημα 2 της παρούσας Οδηγίας).
8. Κατά τον έλεγχο των δοσολογικών μορφών, ελέγχεται και η ποιότητα του κλεισίματος.
VII. Χημικός έλεγχος
1. Ο χημικός έλεγχος συνίσταται στην αξιολόγηση της ποιότητας παραγωγής ενός φαρμακευτικού προϊόντος σύμφωνα με τους ακόλουθους δείκτες: «Ταυτότητα», «Δοκιμές καθαρότητας και επιτρεπόμενα όρια προσμίξεων» (ποιοτική ανάλυση) και «ποσοτικός προσδιορισμός» (ποσοτική ανάλυση) φαρμακευτικών ουσιών περιλαμβάνονται στη σύνθεσή του.
2. Η ποιοτική ανάλυση είναι υποχρεωτική:
3. Καθαρισμένο νερό, νερό για ένεση καθημερινά (από κάθε φιάλη και όταν παρέχεται νερό μέσω του αγωγού σε κάθε χώρο εργασίας) για την απουσία χλωριδίων, θειικών αλάτων και αλάτων ασβεστίου. Το νερό που προορίζεται για την παρασκευή αποστειρωμένων διαλυμάτων, εκτός από τις παραπάνω δοκιμές, πρέπει να ελέγχεται για απουσία αναγωγικών ουσιών, αλάτων αμμωνίου και διοξειδίου του άνθρακα σύμφωνα με τις απαιτήσεις της ισχύουσας Κρατικής Φαρμακοποιίας. Κάθε τρίμηνο, το καθαρό νερό θα πρέπει να αποστέλλεται στο εργαστήριο εδαφικού ελέγχου και ανάλυσης για πλήρη χημική ανάλυση.
4. Όλα τα φάρμακα, τα συμπυκνώματα και τα ημικατεργασμένα προϊόντα (συμπεριλαμβανομένων ομοιοπαθητικών βαμμάτων, λειοτριβήσεων, διαλυμάτων, αραιώσεων) που προέρχονται από τις αποθήκες στο δωμάτιο του βοηθού και σε περίπτωση αμφιβολίας - φάρμακα που έρχονται στο φαρμακείο από την αποθήκη.
5. Συμπυκνώματα, ημικατεργασμένα προϊόντα και υγρά φάρμακα σε προχοΐδα και πιπέτες στο δωμάτιο του βοηθού κατά την πλήρωση.
6. Φάρμακα εργοστασιακή παραγωγή, συσκευασμένο σε φαρμακείο και κενό εντός φαρμακείου, που κατασκευάζεται και συσκευάζεται σε φαρμακείο (κάθε σειρά). *
7. . Η ποιοτική ανάλυση πραγματοποιείται επιλεκτικά:
οκτώ.. Δοσολογικές μορφές που παρασκευάζονται σύμφωνα με μεμονωμένες συνταγές και απαιτήσεις ιατρικών οργανισμών, σε κάθε φαρμακοποιό κατά τη διάρκεια της εργάσιμης ημέρας, αλλά όχι λιγότερο από το 10% του συνολικού αριθμού παρασκευασμένων δοσομετρικών μορφών. Θα πρέπει να ελέγχονται διάφοροι τύποι δοσολογικών μορφών. Ιδιαίτερη προσοχή εφιστάται στις δοσολογικές μορφές: για παιδιά; χρησιμοποιείται στην πρακτική των ματιών. που περιέχει ναρκωτικές και δηλητηριώδεις ουσίες.
9. Σειρά -- ένα ορισμένο ποσό απόομοιογενές τελικό προϊόν (φάρμακο) που παρασκευάζεται σε έναν κύκλο παραγωγής υπό σταθερές συνθήκες.
10. Η ποιοτική ανάλυση υποβάλλεται σε επιλεκτικές ομοιοπαθητικές αραιώσεις της τέταρτης δεκαδικής αραίωσης που περιέχει δηλητηριώδη και ισχυρά βιολογικά δραστικές ουσίεςή δηλητηριώδεις και ισχυρές ανόργανες και οργανικές ενώσεις.
έντεκα. . Τα αποτελέσματα της ποιοτικής ανάλυσης καταγράφονται στα περιοδικά σύμφωνα με τα συνημμένα έντυπα (Παραρτήματα 2,3,4 της παρούσας Οδηγίας).
12. Η ποιοτική και ποσοτική ανάλυση (πλήρης χημικός έλεγχος) είναι υποχρεωτική:
δεκατρία.. Όλα τα διαλύματα για ενέσιμα και εγχύσεις πριν από την αποστείρωση, συμπεριλαμβανομένου του προσδιορισμού του pH, των ισοτονιστικών και σταθεροποιητικών παραγόντων. Τα διαλύματα για ενέσιμα και εγχύσεις μετά την αποστείρωση ελέγχονται για τιμή pH, γνησιότητα και ποσοτική περιεκτικότητα ενεργά συστατικά. Οι σταθεροποιητές σε αυτά τα διαλύματα μετά την αποστείρωση ελέγχονται στις περιπτώσεις που ορίζονται από τα τρέχοντα κανονιστικά έγγραφα, συμπεριλαμβανομένων των κατευθυντήριων οδηγιών. Για έλεγχο μετά την αποστείρωση, λαμβάνεται ένα φιαλίδιο διαλύματος από κάθε σειρά.
14. Αποστειρωμένα διαλύματα εξωτερικής χρήσης (οφθαλμικά διαλύματα για άρδευση, διαλύματα για την αντιμετώπιση εγκαυμάτων επιφανειών και ανοιχτές πληγές, για ενδοκολπική χορήγηση κ.λπ.).
15. Οφθαλμικές σταγόνες και αλοιφές που περιέχουν ναρκωτικές και δηλητηριώδεις ουσίες. Κατά την ανάλυση των οφθαλμικών σταγόνων, η περιεκτικότητα σε αυτές σε ισοτονωτικές και σταθεροποιητικές ουσίες προσδιορίζεται πριν από την αποστείρωση.
16. Όλες οι δοσολογικές μορφές για νεογνά*.
17. . Διαλύματα θειικής ατροπίνης και υδροχλωρικού οξέος (για εσωτερική χρήση), διαλύματα διχλωριούχου υδραργύρου και νιτρικού αργύρου.
δεκαοκτώ.. Όλα τα συμπυκνώματα, ημικατεργασμένα προϊόντα, κονιοποιήσεις, συμπεριλαμβανομένων υγρών ομοιοπαθητικών αραιώσεων ανόργανων και οργανικών φαρμακευτικών ουσιών και οι κονιοποιήσεις τους μέχρι την τρίτη δεκαδική αραίωση**.
δεκαεννιά.. Όλες οι ενδοφαρμακευτικές προμήθειες φαρμάκων (κάθε σειρά).
20. Σταθεροποιητές που χρησιμοποιούνται για την παρασκευή ενέσιμων διαλυμάτων και ρυθμιστικών διαλυμάτων που χρησιμοποιούνται για την παρασκευή οφθαλμικών σταγόνων.
21. Η συγκέντρωση της αιθυλικής αλκοόλης όταν αραιώνεται σε φαρμακείο και, εάν χρειάζεται, όταν λαμβάνεται από αποθήκη.
22. Κατ' εξαίρεση, η κατασκευή σύνθετων δοσολογικών μορφών για νεογνά που δεν διαθέτουν μεθόδους ποιοτικής και ποσοτικής ανάλυσης γίνεται υπό την επίβλεψη φαρμακοποιού-αναλυτή ή φαρμακοποιού-τεχνολόγου.
23. Η συγκέντρωση αιθυλικής αλκοόλης σε ομοιοπαθητικά διαλύματα νερού-αλκοόλης, αραιώσεις και σταγόνες (κάθε σειρά).
24. Ομοιοπαθητικά κοκκία για διάσπαση (κάθε σειρά) σύμφωνα με τις απαιτήσεις των ισχυόντων κανονιστικών εγγράφων.
25. Η ποιοτική και ποσοτική ανάλυση (πλήρης χημικός έλεγχος) υποβάλλεται επιλεκτικά σε:
26. Οι δοσολογικές μορφές που κατασκευάζονται σε φαρμακείο σύμφωνα με μεμονωμένες συνταγές ή απαιτήσεις ιατρικών οργανισμών ελέγχονται σε ποσότητα τουλάχιστον τριών μορφών δοσολογίας όταν εργάζονται σε μία βάρδια, λαμβάνοντας υπόψη διαφορετικούς τύπους δοσολογικών μορφών. Ιδιαίτερη προσοχή δίνεται στις δοσολογικές μορφές για παιδιά: χρησιμοποιούνται στην οφθαλμολογική πρακτική. που περιέχει ναρκωτικές και δηλητηριώδεις ουσίες. λύσεις για θεραπευτικούς υποκλυσμούς.
27. Τα αποτελέσματα ενός πλήρους χημικού ελέγχου καταγράφονται στο περιοδικό σύμφωνα με το συνημμένο έντυπο (Παράρτημα 2 της παρούσας Οδηγίας). Το περιοδικό πρέπει να καταγράφει όλες τις περιπτώσεις μη ικανοποιητικής παρασκευής φαρμάκων.
