Фармакологічна дія. Фізико-хімічні та хімічні механізми дії лікарських речовин. Стратегія індивідуальної лікарської терапії
Блокатор H 1 -гістамінових рецепторів першого покоління. Дія на центральну нервову систему обумовлена \u200b\u200bблокадою H 3 -гістамінових рецепторів мозку і пригніченням центральних холінергічних структур. Знімає спазм гладкої мускулатури (безпосередня дія), зменшує проникність капілярів, попереджає і послаблює алергічні реакції, має місцевоанестезуючий, протиблювотний, седативний ефекти, помірно блокує холінорецептори вегетативних гангліїв, надає снодійну дію.
Показанія- анафілактичні та анафілактоїдні реакції (в комплексній терапії); - набряк Квінке;
Сироваткова хвороба; - інші гострі алергічні стани (в комплексній терапії та в тих випадках, коли використання таблетованої форми неможливо).
Побічні дії
Зі сторони нервової системи: Сонливість, слабкість, зниження швидкості психомоторної реакції, порушення координації рухів, запаморочення, тремор, дратівливість, ейфорія, збудження (особливо у дітей), безсоння.
Зі сторони дихальної системи: Сухість слизової оболонки порожнини рота, носа, бронхів (підвищення в'язкості мокротиння).
З боку органів кровотворення: гемолітична анемія, тромбоцитопенія, агранулоцитоз.
Зі сторони серцево-судинної системи: Зниження артеріального тиску, тахікардія, екстрасистолія.
З боку сечовидільної системи: порушення сечовипускання.
Алергічні реакції: кропив'янка, фоточутливість, шкірні висипання, свербіж.
Лоратадин (кларитин)
Фармакологічна дія
Протиалергічний препарат, селективний блокатор периферичних гістамінових H 1 -рецепторів. Лоратадин є трициклічні з'єднання з вираженим антигістамінним дією. Володіє швидким і тривалим протиалергічну дію.
Лоратадин не проникає через гематоенцефалічний бар'єр і не робить впливу на ЦНС. Не має клінічно значимого антихолинергического або седативного дії, тобто не викликає сонливості і не впливає на швидкість реакції при застосуванні в рекомендованих дозах. Прийом препарату Кларитин не призводить до подовження інтервалу QT на ЕКГ. при тривалому лікуванні не спостерігалося клінічно значущих змін показників життєво важливих функцій, даних фізикального огляду, результатів лабораторних досліджень або ЕКГ.
Лоратадин не володіє істотною селективністю відносно гістамінових Н2-рецепторів. Не пригнічує зворотне захоплення норадреналіну і практично не впливає на серцево-судинну систему або функцію водія ритму
Побічні дії
З боку нервової системи: у дітей у віці від 2 до 12 років - головний біль (2.7%), нервозність (2.3%), стомлюваність (1%); у дорослих - головний біль (0.6%), сонливість (1.2%), безсоння (0.1%).
у дорослих - підвищення апетиту (0.5%).
У постмаркетинговомуу періоді
З боку нервової системи: дуже рідко (< 1/10 000) - головокружение, утомляемость.
Зі сторони травної системи: дуже рідко (< 1/10 000) - сухость во рту, желудочно-кишечные расстройства (тошнота, гастрит), нарушение функции печени.
Алергічні реакції: дуже рідко (< 1/10 000) - сыпь, анафилаксия.
З боку серцево-судинної системи: дуже рідко (< 1/10 000) - сердцебиение, тахикардия.
Зі сторони шкірних покривів: дуже рідко (< 1/10 000) - алопеция.
показання
Сезонний (поліноз) і цілорічний алергічні риніти і алергічний кон'юнктивіт (для усунення симптомів, пов'язаних з цими захворюваннями - чхання, свербіння слизової оболонки носа, ринореї, відчуття печіння та свербежу в очах, сльозотечі); - хронічна ідіопатична кропив'янка; - шкірні захворювання алергічного походження .
33. Засоби, що усувають загальні прояви алергічних реакцій типу анафілактичного шоку. Адреналін, еуфілін, преднізоллон. Основні фармакологічні ефекти, мета призначення кожного препарату і небажані ефекти.
протиалергічний засіб (Antiallergica; син. Десенсибілізуючі засоби) - лікарські засоби, що попереджають або послаблюють прояви алергічних реакцій. Одним з можливих шляхів попередження і лікування алергічних реакцій є метод так зв. специфічної гіпосенсибілізації, т. е. зниження чутливості організму до якого-небудь антигену шляхом багаторазового введення самого антигену в низьких дозах, які не викликають проявів алергії. При цьому організм поступово втрачає чутливість до вводиться антигену.
адреналін
Фармакологічна дія Адреномиметик, надає пряму стимулюючу дію на α- і β-адренорецептори. Під дією адреналіну (адреналіну) внаслідок стимуляції α-адренорецепторів відбувається збільшення вмісту внутрішньоклітинного кальцію в гладких м'язах. підвищує активність фосфоліпази С (через стимуляцію G-білка) і освіту інозітолтріфосфат і діацілгліцерола. Має виражену дію на серцево-судинну систему. Збільшує частоту і силу серцевих скорочень, ударний і хвилинний об'єм серця. Покращує AV-провідність, підвищує автоматизм. Збільшує потребу міокарда в кисні. Викликає звуження судин органів черевної порожнини, шкіри, слизових оболонок, в меншій мірі - скелетних м'язів. Підвищує артеріальний тиск (головним чином систолічний), Епінефрин (адреналін) розслаблює гладкі м'язи бронхів, знижує тонус і моторику шлунково-кишкового тракту, розширює зіниці, сприяє зниженню внутрішньоочного тиску. Викликає гіперглікемію і підвищує вміст в плазмі вільних жирних кислот. Показання Алергічні реакції негайного типу (у т. Ч. Кропив'янка, ангіоневротичний шок, анафілактичний шок), що розвиваються при застосуванні лікарських засобів, сироваток, переливанні крові, вживанні харчових продуктів, укусах комах або введенні інших алергенів. Бронхіальна астма (купірування нападу), бронхоспазм під час наркозу. З метою зупинки кровотечі. Побічна дія З боку серцево-судинної системи: стенокардія, брадикардія або тахікардія, серцебиття, підвищення або зниження артеріального тиску; при застосуванні в високих дозах - шлуночкові аритмії; рідко - аритмія, біль у грудній клітці. З боку нервової системи: головний біль, тривожний стан, тремор, запаморочення, нервозність, втома, психоневротичні розлади
еуфілін
Фармакологічна дія
Бронхолітичну засіб, похідне ксантину; інгібує фосфодіестеразу, збільшує накопичення в тканинах циклічного аденозинмонофосфату, блокує аденозинові (пуринові) рецептори; знижує надходження іонів кальцію через канали клітинних мембран, зменшує скоротливу активність гладкої мускулатури. Розслабляє мускулатуру бронхів, збільшує мукоциліарний кліренс, стимулює скорочення діафрагми, покращує функцію дихальних і міжреберних м'язів, стимулює дихальний центр, підвищує його чутливість до вуглекислого газу і покращує альвеолярну вентиляцію, що в кінцевому підсумку призводить до зниження тяжкості та частоти епізодів апное. Нормалізує дихальну функцію, сприяє насиченню крові киснем і зниження концентрації вуглекислоти. Виявляє стимулюючий вплив на діяльність серця, збільшує силу і число серцевих скорочень, підвищує коронарний кровотік і потреба міокарда в кисні. Знижує тонус кровоносних судин (головним чином, судин мозку, шкіри і нирок). Надає периферичний веноділатірующее дію, зменшує легеневий судинний опір, знижує тиск в «малому» колі кровообігу. Збільшує нирковий кровотік, виявляє помірний діуретичний ефект. Розширює позапечінкові жовчні шляхи. Гальмує агрегацію тромбоцитів (пригнічує фактор активації тромбоцитів і PgE2 альфа), підвищує стійкість еритроцитів до деформації (поліпшує реологічні властивості крові), зменшує тромбоутворення та нормалізує мікроциркуляцію. Володіє токолітичних дією, підвищує кислотність шлункового соку. При використанні в великих дозах володіє енілептогенним дією.
Побічні дії
З боку нервової системи: Запаморочення, головний біль, безсоння, збудження, тривожність, дратівливість, тремор.
З боку серцево-судинної системи: серцебиття, тахікардія (в тому числі у плода при прийомі вагітної в III триместрі), аритмії, кардіалгія, зниження артеріального тиску, збільшення частоти нападів стенокардії.
З боку травної системи: Біль у шлунку, нудота, блювота, гастроезофагеальний рефлюкс, печія, загострення виразкової хвороби, діарея, при тривалому прийомі - зниження апетиту.
Алергічні реакції: шкірний висип, свербіж, лихоманка.
Інші: біль у грудях, тахіпное, відчуття припливів до обличчя, альбумінурія, гематурія, гіпоглікемія, посилення діурезу, підвищене потовиділення.
показання
Бронхообструктивний синдром будь-якого генезу: бронхіальна астма (препарат вибору у хворих з астмою фізичного напруження і як додатковий засіб при ін. Формах), хронічна обструктивна хвороба легень, емфізема легенів, хронічний обструктивний бронхіт, легенева гіпертензія, «легеневе» серце, нічне апное.
преднізолон
Фармакологічна дія
Синтетичний ГКС. Має виражену протизапальну дію. Препарат гальмує розвиток симптомів запалення. Гальмує накопичення макрофагів, лейкоцитів та інших клітин в зоні запалення. Пригнічує фагоцитоз, вивільнення мікросомальних ферментів, а також синтез і вивільнення медіаторів запалення. Викликає зменшення проникності капілярів, гальмування міграції лейкоцитів.
Підсилює синтез ліпомодуліна, інгібітору фосфоліпази А2, що вивільняє арахідонову кислоту з фосфоліпідних мембран з одночасним пригніченням її синтезу.
Механізм иммунодепрессивного дії преднізолону до кінця не вивчений. Препарат зменшує кількість Т-лімфоцитів, моноцитів і ацидофільних гранулоцитів, а також зв'язування імуноглобулінів з рецепторами на поверхні клітин, гальмує синтез або вивільнення інтерлейкінів шляхом зменшення бластогенеза Т-лімфоцитів; зменшує ранній імунологічний відповідь. Гальмує також проникнення імунологічних комплексів через мембрани і зменшує концентрацію компонентів комплементу і імуноглобулінів.
Преднізолон діє на дистальну частину ниркових канальців, посилюючи зворотне всмоктування натрію і води, а також збільшення виділення калію і іонів водню.
Преднізолон пригнічує секрецію АКТГ гіпофізом, що приводить до зменшення вироблення кортикостероїдів і андрогенів корою наднирників. Після тривалого застосування препарату у високих дозах функція надниркових залоз може відновлюватися протягом року, а в деяких випадках розвивається стійке придушення їх функції. Преднізолон підсилює катаболізм білків і індукує ферменти, що беруть участь у метаболізмі амінокислот. Гальмує синтез і посилює катаболізм білків в лімфатичної, сполучної, м'язової тканини. При тривалому застосуванні можливий розвиток атрофії цих тканин (а також шкіри).
Підвищує концентрацію глюкози в крові шляхом індукції ферментів глюконеогенезу в печінці, стимуляції катаболізму білків (що збільшує кількість амінокислот для глюконеогенезу) і зменшення споживання глюкози в периферичних тканинах. Це призводить до накопичення глікогену в печінці, підвищення концентрації глюкози в крові і підвищення резистентності до інсуліну.
показання
Ендокринологічні захворювання:
Недостатність кори надниркових залоз: первинна (хвороба Аддісона) та вторинна; - адреногенітальний синдром (вроджена гіперплазія наднирників); - гостра недостатність кори надниркових залоз;
Перед хірургічним втручанням і при важких захворюваннях і травмах у пацієнтів з недостатністю надниркових залоз; - підгострий тиреоїдит.
Важкі алергічні захворювання, резистентні до іншої терапії: - контактний дерматит; - атопічний дерматит; - сироваткова хвороба; - реакції підвищеної чутливості до лікарських засобів;
Постійний або сезонний алергічний риніт; - анафілактичний реакції; - ангіоневротичний набряк.
Ревматичні захворювання:
Ревматоїдний артрит, ювенільний ревматоїдний артрит (у випадках резистентний до інших методів лікування);
Дерматологічні захворювання: - ексфоліативний дерматит; - герпетиформний бульозний дерматит;
Тяжкий себорейний дерматит; - тяжка мультиформна еритема (синдром Стівенса-Джонсона);
Побічні дії
При короткочасному застосуванні преднізолону (як і інших ГКС) побічні ефекти спостерігаються рідко. При застосуванні преднізолону протягом тривалого часу можливий розвиток наступних побічних ефектів.
З боку водно-електролітного балансу: затримка в організмі натрію і рідини, гіпокаліємія.
З боку кістково-м'язової системи: м'язова слабкість, стероїдна міопатія, втрата м'язової маси, остеопороз, компресійний перелом хребта.
З боку травної системи: стероидная виразка з можливим проривом і кровотечею, панкреатит, метеоризм, виразковий езофагіт, порушення травлення, нудота, підвищений апетит.
Дерматологічні реакції: атрофія шкіри, стриї, вугри, уповільнене загоєння ран, витончення шкіри, петехії, гематоми, еритема, підвищене потовиділення, алергічний дерматит, кропив'янка, ангіоневротичний набряк.
З боку ЦНС і периферичної нервової системи: підвищення внутрішньочерепного тиску з синдромом застійного соска зорового нерва (виникає найчастіше у дітей, після занадто швидкого зниження дози, симптоми - головний біль, погіршення гостроти зору, двоїння в очах); судоми, запаморочення, головний біль, порушення сну.
З боку ендокринного статусу: вторинна надниркова та гіпоталамо-гіпофізарна недостатність (особливо під час стресових ситуацій: хвороба, травма, хірургічна операція); синдром Кушинга.
Інші: анафілактичніреакції, реакції гіперчутливості; облітеруючий артеріїт, збільшення маси тіла, непритомність.
1. Сутність фармакології як науки. Розділи і області сучасної фармакології. Основні терміни і поняття фармакології - фармакологічна активність, дія, ефективність хімічних речовин.
фармакологія - наука про ліки у всіх аспектах - теоретична основа терапії:
а) наука про взаємодію хімічних речовин з живими системами
б) наука про управління процесами життєдіяльності організму за допомогою хімічних речовин
розвиток фармакологіїйде по двох головних напрямках: фундаментальні дослідження для з'ясування принципів і механізмів дії ЛЗ та розробка ефективних препаратів як основи лікування захворювань.
Фармакологію поділяють на:
1. загальну- вивчає загальні закономірності взаємодії лікарських речовин з живими організмами.
приватну- розглядає конкретні фармакологічні групи і окремі препарати
2. Експериментальну (базисну) фармакологію - вивчає дію ліків в експерименті.
клінічну фармакологію - вивчає клінічну ефективність і безпеку
застосування ліків у пацієнтів, оптимізує програму лікування пацієнта з урахуванням
його стану.
токсикологію - вивчає токсичну дію на органи різних речовин (в тому числі
і лікарських).
Розділи сучасної фармакології:
1) фармакодинамика - вивчає а) вплив ЛЗ на організм людини, б) взаємодія різних ЛЗ в організмі при одночасному їх призначенні, в) вплив віку і різних захворювань на дію ЛЗ
2) фармакокінетика - вивчає всмоктування, розподіл, метаболізм та екскрецію ЛЗ (тобто як організм хворого реагує на ЛЗ)
3) фармакогенетика- вивчає роль генетичних факторів у формуванні фармакологічного відповіді організму на ЛЗ
4) фармакоекономіка- оцінює результати використання і вартість ЛЗ для прийняття рішення про подальше їх практичному застосуванні
5) фармакоепідеміологія - вивчає застосування ЛЗ та їх ефекти на рівні популяцій або великих груп людей для забезпечення застосування найбільш ефективних і безпечних лікарських засобів
Основні терміни і поняття:
Фармакологічна (біологічна) активність - властивість речовини викликати зміни в биосистеме (організмі людини). Фармакологічні речовини \u003d біологічно активні речовини (БАВ)
Фармакологічна дія - вплив ЛЗ на об'єкт і його мішені
фармакологічний ефект - результат дії речовини в організмі (модифікація фізіологічних, біохімічних процесів, морфологічних структур) - кількісне, але не якісна зміна в стані біосистем (клітин, тканин, органів).
ефективність ЛЗ - здатність ЛЗ викликати певні необхідні в даному випадку фармакологічні ефекти в організмі. Оцінюється на основі «істотних доказів» - адекватних добре контрольованих досліджень і клінічних випробувань, проведених експертами з відповідною науковою підготовкою та досвідом в дослідженні ліків даного типу (FDA)
2. Джерела і етапи створення ліків. Ліки - генерики, плацебо - ефекти Визначення понять лікарська речовина, лікарський засіб, лікарський препарат і лікарська форма.
Джерела створення ЛЗ:
а) натуральна сировина: рослини, тварини, мінерали, Продукти життєдіяльності мікроорганізмів (серцеві глікозиди, свинячий інсулін, АБ)
б) модифіковані природні БАР
в) продукти хімічного синтезу (методи: фармакологічний скринінг, молекулярне конструювання, відтворення біогенних амінів, цілеспрямована модифікація молекул з уже відомою активністю, синтез фармакологічно активних метаболітів, випадкові знахідки ( «серендіпітний» метод))
г) продукти генної інженерії (рекомбінантний інсулін, інтерферони)
Етапи створення ЛЗ:
1. Синтез ЛЗ в хімічній лабораторії
2. Доклінічна оцінка активності та небажаних ефектів ЛЗ МОЗ та ін. Організмаціямі
3. Клінічні випробування ЛЗ Експертиза документації Фармакологічним комітетом проводиться після завершення кожної фази. Ліки можуть бути відкликано на будь-якому етапі. (I фаза - оцінка переносимості на здорових добровольцях 20-25 років, II фаза - на хворих добровольцях чисельністю менше 100 чоловік, які страждають певним захворюванням, III фаза - мультицентрові клінічні дослідження на великих групах людей (до 1000 чоловік), IV фаза - моніторинг препарату протягом 5 років після його офіційного дозволу (виконують на великій кількості пацієнтів (не менше 1.000-5.000 чоловік). після завершення III фази клінічних випробувань документація знову надходить в Фармакологічний комітет (обсяг повного досьє може становити до 1 млн. сторінок) і протягом 1-2 років реєструється в Державному реєстрі лікарських засобів і виробів медичного призначення. Тільки після цього фармакологічний концерн має право почати промисловий випуск лікарського засобу і його поширення через аптечну мережу.
Ліки-генерик - це непанентованний лікарський препарат, який є воспризведения оригінального препарату, на діючу речовину якого закінчився термін патентного захисту. Може відрізнятися від оригінального препарату за складом допоміжних речовин. Необхідна вимога для продажу генериків - доказова фармацевтична, біологічна і терапевтична еквівалентність вихідного препарату. Генерикові ліки завжди дешевше їх брендових аналогів, тому що фірма не витрачає кошти на 10-15 річні дослідження ліки, а користується готовими даними
плацебо - будь-який компонент терапії, що не виявляє ніякого специфічного біологічного впливу на хворобу, яка є об'єктом лікування.
Застосовується з метою контролю при оцінці дії ЛЗ та для того, щоб принести користь хворому без будь-яких фармакологічних засобів в результаті тільки психологічного впливу (тобто плацебо-ефекту).
Всі види лікування мають психологічний компонент, Або доставляє задоволення ( плацебо-ефект), Або викликає занепокоєння (ноцебо-ефект). Приклад плацебо-ефекту: швидке поліпшення у хворого вірусною інфекцією при застосуванні антибіотиків. Сприятливість плацебо-ефекту пов'язана з психологічним впливом на пацієнта. Він буде максимальним лише при його використанні в поєднанні з методами лікування, Що мають виражений специфічний ефект. дорогі речовини в якості плацебо також сприяють досягненню більшої відповіді.
Показання до застосування плацебо:
1) слабкі психічні порушення
2) психологічна підтримка пацієнта з невиліковною хронічною хворобою або з підозрою на важкий діагноз
Лікарський засіб - будь-яка речовина або продукт, що використовуються, щоб модифікувати або досліджувати фізіологічні системи або патологічні стани для блага реципієнта (по ВООЗ, 1966 г.); індивідуальні речовини, суміші речовин або композиції невідомого складу, які мають доказані лікувальними властивостями.
лікарська речовина - індивідуальна хімічна сполука, що використовується в якості лікарського засобу.
Лікарська форма - зручна для практичного застосування форма, що надається лікарського засобу для отримання необхідного лікувального або профілактичного ефекту.
Лікарський засіб - лікарський засіб в певній лікарській формі, дозволене органом державного управління.
Наприклад: лікарською речовиною є антибіотик ампіцилін, лікарським засобом - ампіциліну тригідрат, який може випускатися у формі таблеток або капсул. Лікарським препаратом є таблетки ампіциліну тригідрату по 0,25 г.
Шляхи введення ліків в організм і їх характеристика. Пресистемна елімінація ліків.
а. ентеральний шлях введення: перорально, сублінгвально, трансбуккально, ректально, через зонд б. парентеральний шлях введення: внутрішньовенно, підшкірно, внутрішньом'язово, ... 2. Для місцевого впливу: накожно (епікутарно), на слизові, в порожнині (черевну, плевральну, суглобову), в тканини ...Перенесення ліків через біологічні бар'єри і його різновиди. Основні фактори, що впливають на перенесення ліків в організмі.
1) Фільтрація (водна дифузія) - пасивне переміщення молекул речовини за градієнтом концентрації через заповнені водою пори в мембрані кожної ... 2) Пасивна дифузія (ліпідна дифузія) - основний механізм перенесення ЛВ, ... 3) Транспорт за допомогою специфічних переносників - перенесення ЛВ за допомогою вбудованих в мембрану переносників (частіше ...Перенесення через мембрани лікарських речовин із змінною іонізацією (рівняння іонізації Гендерсона-Гассельбальха). Принципи управління перенесенням.
Всі ЛЗ - слабкі кислоти або слабкі підстави, що мають свої значення константи іонізації (рК). Якщо значення рН середовища дорівнює значенню рК ліки, то 50% його молекул буде знаходиться в іонізованому і 50% в неіонізованому стані і середовище для ліків буде нейтральною.
В кислому середовищі (РН менше рК), там де є надлишок протонів, слабка кислота буде перебувати в недиссоциированной формі (R-COOH), тобто буде пов'язана з протоном - протоновану. Така форма кислоти незаряжена і добре розчинна в ліпідах. Якщо рН зміститися в лужну сторону (тобто рН побільшає рК), то кислота почне диссоциировать і позбудеться протона, перейшовши при цьому в непротонірованную форму, яка має заряд і погано розчинна у ліпідах.
У лужному середовищі, там де є дефіцит протонів, слабка основа буде перебувати в недиссоциированной формі (R-NH 2), тобто буде непротоніровано і позбавлене заряду. Така форма підстави добре розчинна в ліпідах і швидко абсорбується. У кислому середовищі є надлишок протонів і слабка основа почне диссоциировать, пов'язуючи при цьому протони і утворюючи протоновану, заряджену форму підстави. Така форма погано розчинна у ліпідах і слабо абсорбується.
отже, абсорбція слабких кислот протікає переважно в кислому середовищі, а слабких основ - в лужному.
Особливості метаболізму слабких кислот (СК):
1) шлунок: СК в кислому середовищі шлунка неіонізовану, а в лужному середовищі тонкого кишечника вона буде діссоціацііровать і молекули СК придбають заряд. Тому, абсорбція слабких кислот буде найбільш інтенсивної в шлунку.
2) в крові середовище досить лужне і всосавшиеся молекули СК перейдуть в іонізовану форму. Фільтр клубочків нирок пропускає як іонізовані, так і неіонізовані молекули, тому, незважаючи на заряд молекули, СК будуть виводитися в первинну сечу
3) якщо сеча лужна, то кислота залишиться в іонізованій формі, не зможе реабсорбироваться назад в кровотік і виділиться з сечею; сечі кисла, то ліки перейде в неіонізовану форму, яка легко реабсорбується назад в кров.
Особливості метаболізму слабких основ: Протилежно СК (абсорбція краще в кишечнику; в лужній сечі піддаються реабсорбції)
т.ч., щоб прискорити виведення з організму слабкої кислоти сечу необхідно ощелачивать, а щоб прискорити виведення слабкої основи її необхідно підкислити (Детоксикація по Попову).
Кількісну залежність процесу іонізації ліки при різному рН середовища дозволяє отримати рівняння Henderson-Hasselbach:
Де pKa відповідає значенню pH, при якому концентрації іонізованої і неионизированной форм знаходяться в рівновазі .
Рівняння Гендерсона-Гассельбаха дозволяє оцінити ступінь іонізації ЛЗ при даному значенні рН і передбачити ймовірність його проникнення через клітинну мембрану.
(1)Для розведеної кислоти, A,
HA ↔ H + + A -, де HA - концентрація неионизированной (протоновану) форми кислоти і A - - концентрація іонізованої (непротонірованной) форми.
(2) Для слабкої основи, B,
BH + ↔ H + + B, де BH + - концентрація протоновану форми підстави, B - концентрація непротонірованной форми
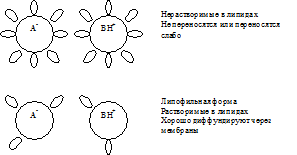
Знаючи рН середовища і рКа речовини, можна по обчисленому логарифму визначити ступінь іонізації ліки, а значить, і ступінь його всмоктування з шлунково-кишкового тракту, Реабсорбції або екскреції нирками при різних значеннях рН сечі і т. д.
Принципи управлінням переносом.
Для прискорення всмоктування
Ø слабких кислот (АСК) - рН шлункового соку повинен бути кислим;
Ø слабких заснований - рН шлункового соку повинен бути нейтральним.
Для прискорення виведення
Ø слабких кислот - сечу подщелачивают;
Ø слабких основ - сечу підкисляють.
Перенесення ліків в організмі. Водна дифузія і дифузія в ліпідах (закон Фіка). Активний транспорт.
Перенесення ЛЗ в організмі може здійснюватися водної та ліпідної дифузією, активним транспортом, ендо- та піноцитозом.
Особливості перенесення ЛЗ в організмі водної дифузією:
1. Епітеліальні покриви (слизові ШКТ, порожнини рота і ін.) - водна дифузія тільки дуже малих молекул (метанол, іони літію і т.д.)
2. Капіляри (крім мозкових) - фільтрація речовин з молекулярною масою до 20-30 тис. Так.
3. Капіляри мозку - в основному не мають водних пір, за винятком областей гіпофіза, епіфіза, зони IV шлуночка, хоріоїдного сплетення, медіанного піднесення
4. Плацента - не має водних пір (хоча питання спірне).
5. Зв'язування ЛЗ з білками крові перешкоджає їх виходу з кров'яного русла, а значить, і водної дифузії
6. Дифузія в воді залежить від розмірів молекул ЛЗ і водних пір
Особливості ліпідного дифузії:
1. Основний механізм перенесення ЛЗ через клітинні мембрани
2. Визначається липофильностью діффундіруемие речовини (тобто коефіцієнтом розподілу «масло / вода») і градієнтом концентрації, може бути обмежена дуже низьку розчинність речовини у воді (що перешкоджає проникненню ЛЗ в водну фазу мембран)
3. Легко дифундують неполярні сполуки, важко - іони.
Будь-яка дифузія (і водна, і в ліпідах) підкоряється закону дифузії Фіка:
Швидкість дифузії - кількість переносите в одиницю часу молекул ліки; З 1 - концентрація речовини зовні мембрани; С 2 - концентрація речовини зсередини мембрани.
Слідство із закону Фіка:
1) фільтрація ЛЗ тим вище, чим більше його концентрація в місці введення (S абсорбіруємой поверхні в кишечнику більше, ніж в шлунку, тому абсорбція ЛЗ в кишечнику швидша)
2) фільтрація ЛЗ тим вище, чим більше концентрація ЛЗ в місці введення
3) фільтрація ЛЗ тим вище, чим менше товщина подоланої біологічної мембрани (товщина бар'єру в альвеолах легенів значно менше, ніж шкіри, тому швидкість абсорбції вище в легких)
активний транспорт - перенесення ЛC незалежно від градієнта концентрації з використанням енергії АТФ, Характерний для гідрофільних полярних молекул, ряду неорганічних іонів, цукрів, амінокислот, піримідинів.
характеризується: а) вибірковістю до певних сполук б) можливістю конкуренції двох речовин за один транспортний механізм в) насичуваність при високих концентраціях речовини г) можливістю транспорту проти градієнта концентрації д) витратою енергії.
7. Центральний постулат фармакокінетики концентрація ліків в крові - основний параметр для управління терапевтичним ефектом. Завдання, які вирішуються на підставі знання цього постулату.
Центральний постулат (догма) фармакокінетики: Концентрація ЛВ в плазмі крові детермінує (кількісно визначає) фармакологічний ефект.
У більшості випадків швидкість всмоктування, розподілу, метаболізму та екскреції ЛЗ пропорційна їх концентрації в плазмі крові (підпорядковується закону діючих мас), тому знаючи її можливо:
1) визначити період полуелімінаціі (для ЛЗ з кінетикою першого порядку)
2) пояснити тривалість деяких токсичних ефектів ЛЗ (для ЛЗ у високих дозах з кінетикою насичення)
[C] плазма → [C] на мішені → ефект
Визначаються законами визначається з-нами фармодінамікі
розподілу
Завдання: навчитися керувати концентрацією ліки в крові.
Фармакокінетичні моделі (однокамерна і двокамерна), кількісні закони всмоктування та елімінації ліків.
Весь організм - єдиний однорідний контейнер. Допущення: 1) встановлюється швидке динамічний розвиток між вмістом препарату в ... 2) ЛЗ швидко і рівномірно розподіляється по всьому об'єму кровіРозподіл ліків в організмі. Відсіки, ліганди. Основні детермінанти розподілу.
Відсіки розподілу: 1. Позаклітинне простір (плазма, міжклітинна рідина) 2. Клітини (цитоплазма, мембрана органел)Константа елімінації, її сутність, розмірність, зв'язок з іншими фармакокинетическими параметрами.
Константа швидкості елімінації (K el, хв -1) - показує, яка частина ЛЗ елімінується з організму в одиницю часу Þ Kel \u003d A вид / А заг, де А вид - кількість ЛС, що виділяється в од. часу, А заг - загальна кількість ЛЗ в організмі.
Значення k el зазвичай знаходять шляхом вирішення фармакокинетического рівняння, що описує процес елімінації ліки з крові, тому k el називають модельним показником кінетики. Безпосереднього відношення до планування режиму дозування k el не має, але її значення використовують для розрахунку інших фармакокінетичних параметрів.
Константа елімінації прямо пропорційна кліренсу і обернено пропорційно обсягу розподілу (з визначення кліренсу): Kel \u003d CL / Vd; \u003d Годину -1 / хв -1 \u003d частка в годину.
Період напіввиведення ліків, його сутність, розмірність, взаємозв'язок з іншими фармакокинетическими параметрами.
період полуелімінаціі (T ½, хв) - це час, необхідний для зниження концентрації ЛЗ в крові рівно наполовину. При цьому не грає ролі яким шляхом досягається зниження концентрації - за допомогою біотрансформації, екскреції або ж за рахунок поєднання обох процесів.
Період полуелімінаціі визначають за формулою:
![]()
Період напіввиведення - найважливіший фармакокинетический параметр, що дозволяє:
б) визначити час повної елімінації препарату
в) передбачити концентрацію ЛЗ в будь-який момент часу (для ЛЗ з кінетикою першого порядку)
Кліренс як головний параметр фармакокінетики для управління режимом дозування. Його сутність, розмірність і зв'язок з іншими фармакокинетическими показниками.
кліренс (Cl, мл / хв) - обсяг крові, який очищається від ЛЗ за одиницю часу.
Оскільки плазма (кров) - «видима» частина обсягу розподілу, то кліренс - фракція обсягу розподілу, з якої ліки виділяється в одиницю часу. Якщо позначити загальна кількість ліки в організмі через А заг, А кількість, яка виділилася через А вид, То:
З іншого боку, з визначення обсягу розподілу випливає, що загальна кількість ліки в організмі становить А заг \u003d V d'C тер / плазма. Підставляючи це значення в формулу кліренсу, ми отримаємо:
![]() .
.
Таким чином, кліренс - відношення швидкості виведення лікарського засобу до його концентрації в плазмі крові.
У такому вигляді формулу кліренсу використовують для розрахунку підтримуючої дози ліків ( D п), Тобто тієї дози лікарського засобу, яка повинна компенсувати втрату ліки і підтримати його рівень на постійному рівні:
Швидкість введення \u003d швидкість виведення \u003d Cl'C тер (доза / хв)
D п \u003d швидкість введенія't (t - інтервал, між прийомом ліків)
кліренс аддитивен, Тобто елімінація речовини з організму може відбуватися за участю процесів, що йдуть в нирках, легенях, печінці та інших органах: Cl системний \u003d Cl нирковий. + Cl печінки + Cl ін.
кліренс пов'язаний з періодом полуелімінаціі ЛЗ і обсягом розподілу: T 1/2 \u003d 0,7 * Vd / Cl.
Доза. Види доз. Одиниці дозування лікарських засобів. Цілі дозування ліків, способи і варіанти введення, інтервал введення.
Дія ЛС на організм більшою мірою визначається їх дозою.
доза - кількість речовини, введене в організм за один прийом; виражається у вагових, об'ємних або умовних (біологічних) одиницях.
Види доз:
а) разова доза - кількість речовини на один прийом
б) добова доза - кількість препарату, яка призначається на добу в один або декілька прийомів
в) курсова доза - загальна кількість препарату на курс лікування
г) терапевтичні дози - дози, в яких препарат використовують з лікувальними або профілактичними цілями (Порогові, або мінімальні діючі, середні терапевтичні і вищі терапевтичні дози).
д) токсичні і смертельні дози - дози ЛВ, при яких вони починають надавати виражені токсичні ефекти або викликати смерть організму.
е) завантажувальна (вступна) доза - кількість введеного ЛЗ, яке заповнює весь обсяг розподілу організму в чинній (терапевтичної) концентрації: ВД \u003d (Css * Vd) / F
ж) підтримуюча доза - систематично вводиться кількість ЛЗ, яке компенсує втрати ЛЗ з кліренсом: ПД \u003d (Css * Cl * DT) / F
Одиниці дозування ЛЗ:
1) в грамах або частках грама ЛЗ
2) кількість ЛЗ в розрахунку на 1 кг маси тіла (наприклад, 1 мг / кг) Або на одиницю поверхні тіла (наприклад, 1 мг / м 2)
Цілі дозування ЛЗ:
1) визначити кількість ЛЗ, необхідне для того, щоб викликати потрібний терапевтичний ефект з певною тривалістю
2) уникнути явищ інтоксикації і побічних ефектів при введенні ЛЗ
Способи введення ЛЗ: 1) ентерально 2) парентеральний (див. Ст. 5)
Варіанти введення ЛЗ:
а) безперервний (шляхом тривалих внутрішньосудинних інфузій ЛЗ крапельно або через автоматичні дозатори). При безперервному введенні ЛЗ його концентрація в організмі змінюється плавно і не піддається значним коливанням
б) переривчасте введення (ін'єкційним або неін'єкційним способами) - введення ліків через певні проміжки часу (інтервали дозування). При переривчастому введенні ЛЗ його концентрація в організмі безперервно коливається. Після прийому певної дози вона спочатку підвищується, а потім поступово знижується, досягаючи мінімальних значень перед черговим введенням ліки. Коливання концентрації тим значніше, чим більше вводиться доза ліків і інтервал між введеннями.
інтервал введення - інтервал між вводяться дозами, що забезпечує підтримку терапевтичної концентрації речовини в крові.
15. Введення ліків з постійною швидкістю. Кінетика концентрації препарату в крові. Стаціонарна концентрація препарату в крові (C ss), час її досягнення, розрахунок і управління нею.
 Особливість введення ЛЗ з постійною швидкістю - плавну зміну його концентрації в крові при введенні, при цьому:
Особливість введення ЛЗ з постійною швидкістю - плавну зміну його концентрації в крові при введенні, при цьому:
1) час досягнення стаціонарної концентрації ліки становить 4-5t ½ і не залежить від швидкості інфузії (величини дози, що вводиться)
2) при збільшенні швидкості інфузії (дози, що вводиться) величина С SS також збільшується в пропорційне число раз
3) елімінація ліків з організму після припинення інфузії займає 4-5t ½.
Сss - рівноважна стаціонарна концентрація - концентрація ЛЗ, що досягається при швидкості введення рівної швидкості виведення, тому:
![]() (З визначення кліренсу)
(З визначення кліренсу)
За кожний наступний період напіввиведення концентрація ЛЗ приростає на половину від залишилася концентрації. Всі ЛЗ, що підкоряються закону елімінації першого порядку, досягатимуть Css через 4-5 періодів напіввиведення.
Підходи до управління рівнем Сss: Змінити вводиться дозу ЛЗ або інтервал введення
16. Переривисте введення ліків. Кінетика концентрації препарату в крові, терапевтичний і токсичний діапазон концентрацій. Розрахунок стаціонарної концентрації (C ss), кордонів її коливань і управління нею. Адекватний інтервал введення дискретних доз.
 Коливання концентрації ЛЗ в плазмі крові: 1 - при постійному внутрішньовенному краплинному введенні; 2-прі дробовому введенні тієї ж добової дози з інтервалом 8 год; 3 - при введенні добової дози з інтервалом 24 год.
Коливання концентрації ЛЗ в плазмі крові: 1 - при постійному внутрішньовенному краплинному введенні; 2-прі дробовому введенні тієї ж добової дози з інтервалом 8 год; 3 - при введенні добової дози з інтервалом 24 год.
Переривчасте введення ЛЗ - Вступ певної кількості ЛЗ через деякі проміжки часу.
Рівноважна стаціонарна концентрація досягається через 4-5 періодів полуелімінаціі, час її досягнення не залежить від дози (на початку, коли рівень концентрації ЛЗ невисокий, швидкість його елімінації також невисока; в міру збільшення кількості речовини в організмі наростає і швидкість його елімінації, тому рано чи пізно настане такий момент, коли збільшена швидкість елімінації врівноважить вводиться дозу ЛЗ і подальше зростання концентрації припинитися)
Css прямо пропорційна дозі ЛЗ і обернено пропорційна інтервалу введення і кліренсу ЛС.
Межі коливань Css: ![]() ; C ss min \u003d C ss max × (1 - ел. Фр.). Коливання концентрації ЛЗ пропорційні T / t 1/2.
; C ss min \u003d C ss max × (1 - ел. Фр.). Коливання концентрації ЛЗ пропорційні T / t 1/2.
Терапевтичний діапазон (коридор безпеки, терапевтичне вікно) - це інтервал концентрацій від мінімальної терапевтичної до викликає поява перших ознак побічних дій.
токсичний діапазон - інтервал концентрації від вищої терапевтичної до смертельної.
Адекватний режим введення дискретних доз: Такий режим введення, при якому флуктуація концентрації препарату в крові укладається в терапевтичний діапазон. Для визначення адекватного режиму введення ЛЗ необхідно розрахувати. Різниця між Css max і Css min при цьому не повинна перевищити 2Css.
Управління коливаннями Css:
Розмах коливань Css прямо пропорційний дозі ЛЗ і обернено пропорційний інтервалу його введення.
1. Змінити дозу ЛЗ: При збільшенні дози ЛЗ діапазон коливань його Css пропорційно збільшується
2. Змінити інтервал введення ЛЗ: При збільшенні інтервалу введення ЛЗ діапазон коливань його Css пропорційно зменшується
Одночасно змінити дозу і інтервал введення
Вступна (завантажувальна) доза. Терапевтичний сенс, розрахунок за фармакокінетичними параметрами, умови і обмеження її використання.
Вступна (завантажувальна) доза - доза, що вводиться за один прийом і що заповнює весь обсяг розподілу в чинній терапевтичної концентрації. ВД \u003d (Css * Vd) / F; \u003d Мг / л, \u003d л / кг
терапевтичний сенс: Вступна доза швидко забезпечує діючу терапевтичну концентрацію ЛЗ в крові, що дозволяє, наприклад, швидко зняти напад БА, аритмії і т.д.
Вступна доза може бути введена за один раз лише тоді, коли ігнорується процес розподілу речовини
Обмеження використання ВД: Якщо розподіл ЛЗ відбувається значно повільніше, ніж його надходження в кров, Введення відразу всієї завантажувальної дози (особливо внутрішньовенно) створить концентрацію значно вище терапевтичної та зумовить виникнення токсичних ефектів. Умова використання ВД: Тому введення навантажувальних доз завжди має бути повільним або дробовим.
Підтримуючі дози, їх терапевтичний сенс і розрахунок для оптимального режиму дозування.
Терапевтичний сенс: ПД компенсує втрати з кліренсом за інтервал між введеннями препарату. Розрахунок для оптимального дозування ЛЗ (для швидкого купірування нападу): ... 1. Розраховуємо ВД: ВД \u003d (Css * Vd) / FІндивідуальні, вікові і статеві відмінності фармакокінетики ліків. Поправки для розрахунку індивідуальних значень обсягу розподілу ліків.
2. Статеві відмінності в дії ліків. Для жінок характерна менша маса тіла, ніж для чоловіків, тому і величина доз ліки для них повинна ... 3. патологічні стани організму і дію ліків а) захворювання печінки: F ЛЗ через виключення пресистемного метаболізму, фракція незв'язаного ЛЗ через нестачу ...Нирковий кліренс ліків, механізми, їх кількісні та якісні характеристики.
Механізми ниркового кліренсу і їх характеристика: 1. Фільтрація: ЛЗ, виделяемоетолько фільтрацією (інсулін) матиме кліренс, ... Визначається: нирковим кровотоком, незв'язаної фракцією ЛЗ і фільтраційної здатністю нирок.Фактори, що впливають на нирковий кліренс ліків. Залежність кліренсу від фізико-хімічних властивостей лікарських засобів.
а) гломерулярна фільтрація б) швидкість ниркового кровотоку в) максимальна швидкість секреціїПечінковий кліренс ліків, його детермінанти та обмеження. Ентерогепатичній цикл лікарських засобів.
1) метаболізм (біотрансформація) шляхом окислення, відновлення, алкілування, гідролізу, коньюгации і т.д. Основна стратегія метаболізму ксенобіотиків: неполярні речовини ® полярні ... 2) секреція (виведення нетрансформованих речовин в жовч)Корекція лікарської терапії при ураженні печінки та інших патологічних станах.
Корекцію режиму дозування при захворюванні нирок см. Вище в в.26, загальні принципи корекції - в.25. Корекція режиму дозування під контролем загального кліренсу препарату: Корекція дози: Дінді. \u003d Дтіпічн. × Clінд. / Clтіпічн.Корекція режиму дозування під контролем залишкової функції нирок.
Нам відомо: а) залишкова функція нирок, що визначається кліренсом креатиніну у даного ... б) загальний кліренс даного ЛЗ (СlЛС / загальний) і частка ниркового кліренсу ЛС в загальному кліренсіСтратегія індивідуальної лікарської терапії.
визнання важливої \u200b\u200bролі концентрації як сполучної ланки фармакокінетики і фармакодинаміки сприяє створенню стратегії цільової концентрації - оптимізації дози у даного хворого на основі вимірювання концентрації ЛЗ. Вона складається з наступних етапів:
1. Вибір цільової концентрації
2. Розрахунок V d і Cl на основі типових значень і внесення поправок з урахуванням таких факторів як маса тіла і функція нирок.
3. Введення завантажувального дози або підтримуючої дози, розрахованих з урахуванням значень TC, V d і Cl.
4. Реєстрація реакції хворого і визначення концентрації ЛЗ
5. Перегляд V d і Cl на основі результатів вимірювання концентрації.
6. Повторити кроків 3-6 з метою підбору необхідної для оптимальної реакції на ліки підтримуючої дози.
Біотрансформація лікарських засобів, її біологічний сенс, основна спрямованість і вплив на активність ліків. Основні фази метаболічних перетворень ліків в організмі.
Біотрансформація ЛЗ - хімічні перетворення ЛЗ в організмі.
Біологічний сенс біотрансформації ЛЗ: створення субстрату, зручного для подальшої утилізації (в якості енергетичного або пластичного матеріалу) або в прискоренні виведення ЛЗ з організму.
Основна спрямованість метаболічних перетворень ЛЗ: неполярні ЛЗ → полярні (гідрофільні) метаболіти, що виводяться з сечею.
Виділяють дві фази метаболічних реакцій ЛЗ:
1) метаболічна трансформація (несинтетичних реакції, фаза 1) - перетворення речовин за рахунок мікросомального і внемікросомального окислення, відновлення і гідролізу
2) кон'югація (синтетичні реакції, фаза 2) - біосинтетичний процес, що супроводжується приєднанням до лікарської речовини або його метаболітів ряду хімічних угруповань або молекул ендогенних з'єднань шляхом а) освіти глюкуронидов б) ефірів гліцерину в) сульфоефіров г) ацетилювання д) метилування
Біологічна трансформація суттєво вплине на фармакологічну активність лікарських засобів:
1) найчастіше метаболіти біотрансформації є неактивними або їх активність знижена в порівнянні з вихідною речовиною
2) в деяких випадках метаболіти можуть зберігати активність і навіть перевершувати за активністю вихідна речовина (кодеїн метаболізується до більш фармакологічно активного морфіну)
3) іноді в ході біотрансформації утворюються токсичні речовини (метаболіти ізоніазиду, лідокаїну)
4) іноді в ході біотрансформації утворюються метаболіти з протилежними фармакологічними властивостями (метаболіти неселективних агоністів b 2 - адренорецепторів мають властивості блокаторів цих рецепторів)
5) ряд речовин є проліками, які початково не дають фармакологічних ефектів, але в ході біотрансформації перетворюються в БАВ (неактивна L-допа, проникаючи через гематоенцефалічний бар'єр, перетворюється в мозку в активний дофамін, при цьому немає системних ефектів дофаміну).
Клінічне значення біотрансформації ліків. Фактори, що впливають на їх бтотрансформацію. Метаболічна взаємодія ліків.
Вплив на біотрансформацію ЛЗ різних факторів: А) функціональний стан печінки: при її захворюваннях кліренс ЛЗ зазвичай ... б) вплив факторів середовища: куріння сприяє індукції цитохрому P450, в результаті чого прискорюється метаболізм ЛЗ в ...Шляхи та механізми виведення ліків з організму. Можливості управління виведенням ліків.
Шляхи та механізми виведення ЛЗ:елімінація ЛЗ печінкою і нирками і деякими іншими органами:
а) нирками шляхом фільтрації, секреції, реабсорбції
б) печінкою шляхом біотрансформації, екскреції з жовчю
в) через легені, слину, піт, молоко і т.д. шляхом секреції, випаровування
Можливості управління процесами виведення ЛЗ:
1. управління pH: в лужній сечі підвищується виведення кислих сполук, в кислому - виведення основних з'єднань
2. застосування жовчогінних препаратів (Холензим, аллохол)
3. гемодіаліз, перитонеальний діаліз, гемосорбція, лимфосорбция
4. форсований діурез (в / в NaCl або глюкоза для водного навантаження + Фуросемід або манітол)
5. промивання шлунка, застосування клізм
Концепція рецепторів в фармакології, молекулярна природа рецепторів, сигнальні механізми дії ліків (типи трансмембранної сигналізації і вторинні посередники).
рецептори -молекулярні компоненти клітини або організму, які взаємодіють з ЛЗ і індукують ряд біохімічних подій, що ведуть до розвитку фармакологічного ефекту.
Концепція рецепторів в фармакології:
1. Рецептори детермінують кількісні закономірності дії ЛЗ
2. Рецептори відповідальні за селективність дії ЛЗ
3. Рецептори посередники дії фармакологічних антагоністів
Концепція рецепторів - основа цілеспрямованого застосування лікарських засобів, що впливають на регуляторні, біохімічні процеси і комунікації.
Молекулярна природа рецепторів:
1. регуляторні білки, посередники дії різних хімічних сигналів: нейромедіаторів, гормонів, аутокоідов
2. ферменти і трансмембранні білки переносники (Na +, K + АТФази)
3. структурні білки (тубулін, білки цитоскелета, клітинна поверхня)
4. ядерні білки і нуклеїнові кислоти
Сигнальні механізми дії ліків:
1) проникнення розчинних в ліпідах лігандів через мембрану і їх дію на внутрішньоклітинні рецептори.
2) сигнальна молекула зв'язується з позаклітинним доменом трансмембранного білка і активує ферментативну активність його цитоплазматического домену.
3) сигнальна молекула зв'язується з іонним каналом і регулює його відкриття.
4) сигнальна молекула зв'язується з рецептором на поверхні клітини, який пов'язаний з еффекторним ферментом за допомогою G-білка. G-білок активує вторинний посередник.
Типи трансмембранної сигналізації:
а) через 1-TMS-рецептори, що володіють і не володіють тірозінкіназной активністю
б) через 7-ТMS-рецептори, пов'язані з G-білком
в) через іонні канали (ліганд-залежні, потенціал-залежні, щілинні контакти)
вторинні посередники: ЦАМФ, іони Ca2 +, ДАГ, ІФ3.
Фізико-хімічні та хімічні механізми дії лікарських речовин.
Основні фармакологічні ефекти: 1) наркотичну 2) загально депресивний 3) паралізує 4) місцево подразнюючу 5) мембранолитического дії. Хімічна природа речовин: хімічно інертні вуглеводні, ефіри, спирти, ... Механізм дії - оборотне деструірованіе мембран.Селективність і специфічність дії ліків. Терапевтичні, побічні та токсичні ефекти ліків, їх природа з позицій концепції рецепторів. Терапевтична стратегія боротьби з побічними і токсичними ефектами ліків.
специфічність -связиваніе ЛЗ зі строго специфічним йому типом рецептора.
селективність - здатне зв'язуватися ЛЗ з одним або декількома типами рецепторів більш точно, ніж з іншими.
Більш переважно використовувати термін селективність, тому що малоймовірно, що будь-яка молекула ЛЗ може зв'язатися тільки з одним типом рецепторних молекул, оскільки число потенційних рецепторів у кожного пацієнта має астрономічне значення.
терапевтична дія - основний бажаний фармакологічний ефект, очікуваний від даного фармакологічного препарату.
Побічні ефекти- ті ефекти, які виникають при застосуванні речовин в терапевтичних дозах і складають спектр їх фармакологічної дії.
токсичні ефекти - небажані ефекти, які проявляються у даного ЛЗ при виході з терапевтичного діапазону.
Зв'язки терапевтичного і токсичної ефектів ЛЗ на основі аналізу рецепторно-ефекторних механізмів:
1) терапевтичний і токсичний ефекти, опосередковувані одним і тим же рецепторно-ефекторних механізмом (празозин діє як альфа-селективний антагоніст на рецептори ГМК судин і має гіпотензивну дію при есенціальнійгіпертензії, але при його великій дозі у хворого може виникнути постуральна гіпотензія)
2) терапевтичний і токсичний ефекти, опосередковувані ідентичними рецепторами, але різними тканинами або різними ефекторними шляхами (серцеві глікозиди використовують для збільшення скорочувальної здатності міокарда, в той же час вони порушують функцію шлунково-кишкового тракту, зору за рахунок блокади Na + / K + -АТФази клітинної мембрани)
3) терапевтичний і токсичний ефекти, опосредуемий різними типами рецепторів (наприклад, норадреналін надає гіпертензивну дію через a 1 -АР, але при цьому викликає тахікардію через b 1 -АР)
Терапевтична стратегія боротьби з терапевтичними і побічними ефектами ЛЗ:
1. ЛЗ завжди слід вводити у найменшій дозі, яка викликає прийнятний терапевтичний ефект
2. Зниження дози одного ЛЗ за рахунок призначення іншого ЛЗ зі подібним дією, Але через інші рецептори і з іншим профілем токсичності.
3. Селективність дії ЛЗ може бути збільшена шляхом управління концентрацією ЛЗ в районі рецепторів різних відділів організму ( місцеве застосування ЛЗ - інгаляційне застосування сальбутамолу при бронхіальній астмі)
32. Терміни і поняття кількісної фармакології: ефект, ефективність, активність, агоніст (повний, частковий), антагоніст. Клінічне відмінність понять активність і ефективність ліків.
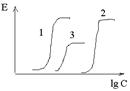 Ефект (відповідь)- кількісний вихід реакції взаємодії клітини, органу, системи або організму з фармакологічним агентом.
Ефект (відповідь)- кількісний вихід реакції взаємодії клітини, органу, системи або організму з фармакологічним агентом.
ефективність - міра реакції по осі ефекту - величина відгуку біологічної системи на фармакологічний вплив; це здатність ЛЗ надавати максимально можливе для нього дію. Тобто фактично це максимальна величина ефекту, яку можна досягти при введенні даних ліків. Чисельно характеризується величиною Е max. Чим вище Е max, тим вище ефективність ліків
активність - міра чутливості до ЛЗ по осі концентрацій, характеризує аффинность (спорідненість ліганда до рецептора), показує, яка доза (концентрація) ЛЗ здатна викликати розвиток стандартного ефекту, рівного 50% від максимально можливого для цих ліків. Чисельно характеризується величиною ЄС 50 або ED 50. Чим вище активність ЛЗ, тим менша його доза потрібна для відтворення терапевтичного ефекту.
Ефективність: 1 \u003d 2\u003e 3
Активність: 1\u003e 3\u003e 2
У клінічній діяльності важливіше знати ефективність, а не активність, тому що нас більше цікавить здатність ЛЗ викликати певну дію в організмі.
агоніст- ліганд, який зв'язується з рецептором і викликає біологічну реакція, спрацьовування фізіологічної системи. повний агонист- максимальний відгук, частковий - викликають меншу реакцію навіть при окупації всіх рецепторів.
 антагоніст - ліганди займають рецептори або змінюють їх таким чином, що вони втрачають здатність взаємодіяти з іншими лігандами, але самі не викликають біологічної реакції (блокують дію агоністів).
антагоніст - ліганди займають рецептори або змінюють їх таким чином, що вони втрачають здатність взаємодіяти з іншими лігандами, але самі не викликають біологічної реакції (блокують дію агоністів).
конкурентні антагоністи- взаємодіють з рецепторами оборотно і тим самим конкурують з агоністами. Збільшення концентрації агоніста може повністю усунути ефект антагоніста. Конкурентний антагоніст зрушує криву «доза-ефект» для агоніста, збільшує EC 50, не впливає на E max.
неконкурентні антагоністи- незворотньо змінюють спорідненість рецепторів до агоністи, зв'язування часто відбувається не з активною ділянкою рецептора, збільшення концентрації агоніста не усуває дію антагоніста. Неконкурентний антагоніст знижує Emax, не змінює EC50, крива «доза-ефект» стискається щодо вертикальної осі.
33. Кількісні закономірності дії ліків. Закон зменшення відгуку біологічних систем. Модель Кларка і її наслідки. Загальний вигляд Залежно концентрація - ефект в нормальних і логнормального координатах.
Модель Кларка-Аріенса:
1. Взаємодія між лігандом (L) і рецептором (R) оборотні.
2. Всі рецептори для даного ліганду - еквівалентні і незалежні (їх насичення не впливає на інші рецептори).
3. Ефект прямо пропорційний числу зайнятих рецепторів.
4. Ліганд існує в двох станах: вільному і пов'язаному з рецептором.
А), де Kd - константа рівноваги, Ke - внутрішня активність.
Б) Т.к. при зростанні кількості лігандів в якийсь момент часу всі рецептори виявляться зайняті, то максимально можливу кількість освічених комплексів ліганд-рецептор описується формулою:
\u003d [R] × (1)
Ефект визначається ймовірністю активації рецептора при зв'язуванні з лігандом, тобто його внутрішньої активністю (Ке), тому E \u003d Ke ×. При цьому ефект максимальний при Ке \u003d 1 і мінімальний і Ке \u003d 0. Природно, що максимальний ефект описується співвідношенням Emax \u003d Ke ×, де - загальне число рецепторів для даного ліганду
Ефект залежить і від концентрації ліганда на рецепторах [З], тому
З наведених співвідношень випливає, що EC 50 \u003d Kd
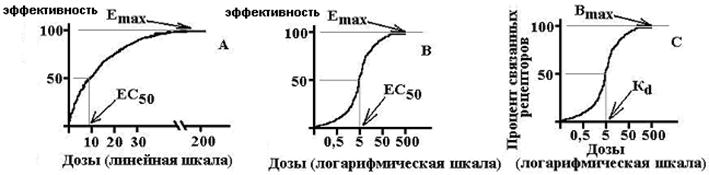
E max - максимальний ефект, B max - максимальне число пов'язаних рецепторів, EC 50 - концентрація ЛЗ, при якій виникає ефект, рівний половині від максимального, K d - константа дисоціації речовини від рецептора, при якій пов'язано 50% рецепторів.
Закону убування відгукувідповідає параболічна залежність «концентрація - ефективність». Відповідь на малі дози ЛЗ зазвичай зростає прямо пропорційно дозі. Однак при збільшенні дози приріст відповідної реакції знижується і в кінцевому рахунку може бути досягнута доза, при якій не відбувається подальшого збільшення відповіді (за рахунок окупації всіх рецепторів для даного ліганду).
Градуальная і квантова оцінка ефекту, сутність і клінічні додатки. Кількісна оцінка активності та ефективності ліків в експериментальній і клінічній практиці.
Всі фармакологічні ефекти можна умовно розділити на дві категорії:
а) градуально (безперервні, інтегральні) ефекти - такі ефекти ЛЗ, які можуть бути виміряні кількісно (дію гіпотензивних ЛЗ - за рівнем артеріального тиску). Описуються градуально «кривої доза-ефект» (див. Ст. 33), на основі якої можна оцінити: 1) індивідуальну чутливість до ЛЗ; 2) активність ЛЗ; 3) максимальну ефективність ЛЗ.
б) квантові ефекти - такі ефекти ЛЗ, які є дискретною величиною, якісною ознакою, тобто описуються всього лише кількома варіантами станів (головний біль після прийому анальгетика або є, або немає). Описується квантовою кривої доза-ефект, де відзначають залежність прояву ефекту в популяції від величини прийнятої дози ЛЗ. Графік залежності доза-ефект при цьому має куполоподібний вигляд і ідентичний кривою Гаусса нормального розподілу. На основі квантової кривої можна: 1) оцінити популяционную чутливість ЛЗ; 2) зазначити наявність ефекту при даній дозі; 3) вибрати середню терапевтичну дозу.
Відмінності між градуально і квантової характеристикою «доза-ефект»:
Кількісна оцінка активності та ефективності ЛЗ проводиться на основі побудови кривих «доза-ефект» і їх подальшій оцінці (див. В.32)
Види дії лікарських засобів. Зміна дії ліків при їх повторному застосуванні.
1. За локалізацією: · місцеве - дія, що виникає на місці додатка ЛЗ (зазвичай шкіра і ... · резорбтивное - це дія, яка ЛЗ надає, коли всмоктується в кровотік або безпосередньо вводиться в ...Залежність дії ліків від віку, статі та індивідуальних здібностей організму. Значення добових ритмів.
· Діти - область фармакології, що займається вивченням особливостей дії ЛЗ на дитячий організм, Називається педіатрична фармакологія. ... · літні люди - в літньому і старечому віці фармакокинетические ... 2. Пол - експерименти на тваринах і клінічні спостереження свідчать, що існують статеві відмінності в ...Варіабельність і мінливість дії ліків. Гіпо- і гіперреактивність, толерантність і тахифилаксия, гіперчутливість і ідіосинкразія. Причини варіабельності дії ліків і раціональна стратегія терапії.
Варіабельність дії ЛЗ - відображає відмінність фармакологічних ефектів одного ЛЗ у різних індивідуумів.
Мінливість дії ЛЗ - відображає здатність ЛЗ впливати, яке відрізняється від його типових фармакологічних ефектів.
Варіанти варіабельності і мінливості дії ЛЗ:
1. гипореактивность - зниження ефекту даної дози ЛЗ в порівнянні з тим ефектом, який спостерігається у більшості хворих.
2. Гіперреактивність - підвищення ефекту даної дози ЛЗ в порівнянні з тим ефектом, який спостерігається у більшості хворих.
3. Толерантність - зниження відповідної реакції організму на повторні введення ЛЗ; для того, щоб відновити реакцію на ЛЗ, його доводиться вводити в усі більших і більших дозах.
4. Тахіфілаксія - стан, при якому часте введення ЛЗ викликає розвиток толерантності вже через кілька годин, але при досить рідкісних введення ЛЗ його ефект зберігається в повній мірі. Розвиток тахифилаксии зазвичай пов'язане з виснаженням ефекторних систем.
5. Гіперчутливість - розвиток алергічної або іншої імунної реакції на повторне введення ЛЗ.
6. Ідіосинкразія - збочена реакція організму на ЛЗ, пов'язане з генетичними особливостями метаболізму ЛЗ або індивідуальної імунологічної реактивності.
Основні причини варіабельності дії ЛЗ:
1) зміна концентрації речовини в зоні рецептора - через відмінності в швидкості всмоктування, його розподілу, метаболізму, елімінації
2) варіації в концентрації ендогенного ліганда - рецептора - пропранолол (β-адреноблокатор) уповільнює ЧСС у людей з підвищеним рівнем катехоламінів в крові, але не впливає на фонову ЧСС у спортсменів.
3) зміна щільності або функції рецепторів.
4) зміна компонентів реакції, розташованих дистальніше рецептора.
Раціональна стратегія терапії: полягає в тому, що для призначення ЛЗ і для того, щоб воно зробило очікуваний ефект, необхідно враховувати індивідуальні фактори організму (вік, стать та ін.), Добові ритми людини, наявність у нього хронічних захворювань та інших відхилень. Також необхідно прогнозувати розвиток нехарактерних ефектів, враховуючи всі можливі варіанти мінливості дії ЛЗ.
Оцінка безпеки ліків. Терапевтичний індекс і стандартні кордону безпеки.
На створення і впровадження нового ЛЗ витрачаються величезні кошти - від 100 до 350 млн доларів і більше. Ці витрати включають працю, витрачений на ... Для того, щоб пройти всі етапи оцінки ЛЗ має відповідати основному ... Оцінка безпеки нових ЛЗ проводиться в 2 етапи:Фармакокінетична взаємодії лікарських засобів (приклади).
Фармакокінетична взаємодія ЛЗ є різновидом фармакологічного взаємодії, тобто взаємодія ліків, яке проявляється тільки при їх спільному надходженні в організм людини.
Фармакокінетична взаємодія здійснюється на етапі всмоктування, розподілу і депонування, метаболізму і виведення.
1. На етапі всмоктування - цей вид взаємодії може призводити до збільшення або зменшення їх всмоктування. Його можна уникнути, якщо робити інтервал між прийомами ЛЗ не менше 4 годин.
При введенні препарату per os його всмоктування детермінують:
· рН середовища - неіонізовані ЛЗ всмоктуються в шлунково-кишковому тракті краще іонізованих, тому підвищення рН шлункового соку підвищує всмоктування слабких основ і знижує всмоктування слабких кислот. приклад: антациди, блокатори Н2-гістамінових рецепторів гальмують всмоктування кетоконазолу та ін. протигрибкових препаратів, непрямих антикоагулянтів, ацетилсаліцилової кислоти, барбітуратів (майже повністю запобігають їх снодійну дію); підвищення рН середовища покращує всмоктування Глибутид, прискорює розчинення оболонки кишково-розчинних речовин.
· пряму взаємодію в шлунково-кишковому тракті - освіту хелатних комплексів і з'єднань, які не всмоктуються в шлунково-кишковому тракті. П рімери:активоване вугілля утворює нерозчинні сполуки з ЛЗ, запобігаючи їх всмоктування при отруєнні; тетрациклін взаємодіють з кальцієм, алюміній, залізо, магній з утворенням хелатних комплексів, тому їх всмоктування знижується при застосуванні антацидів, препаратів вісмуту; фторхінолони + антациди або сукралфат \u003d зниження ефективності антибактеріальної терапії.
· моторика шлунково-кишкового тракту - може викликати або прискорення, або уповільнення всмоктування ЛЗ. приклади: прокинетики (метоклопромід) прискорюють всмоктування швидко всмоктуються ЛЗ (етанол, парацетамол, тетрациклін) і уповільнюють у повільно всмоктуються (дігоксин, циметидин); проносні засоби знижують всмоктування та біодоступність ЛЗ; при прийомі антихолінергічних ЛЗ, блокаторів Н 2 -гістамінових рецепторів (подовження часу проходження ЛЗ по шлунково-кишкового тракту) підвищується біодоступність і всмоктування серцевих глікозидів, препаратів заліза, що може привести в прояву токсичних ефектів.
· кишкова мікрофлора - вона бере безпосередню участь у всмоктуванні ЛЗ, тому будь-який дисбактеріоз проявляється порушеннями всмоктування ЛЗ. приклади: дігоксин + еритроміцин \u003d підвищення концентрації дигоксину в крові та розвиток небажаних ефектів; пероральні конрацептіви + АБ широкого спектру \u003d зниження ефекту контрецепціі
· пошкодження СО кишечника - гальмує всмоктування деяких ЛЗ. приклади: цитостатики (циклофосфамід) гальмують всмоктування дигоксину; порушення всмоктування препаратів заліза, ціанокобаламіну, фолієвої кислоти.
На етапі розподілу і депонування
· Конкурентне витіснення із зв'язку з альбумінами плазми крові - якщо ЛЗ пов'язано з білками менше 90%, то витіснення із зв'язку з ним не призведе до ... · витіснення із зв'язку з білками в тканинах: хінідин витісняє дігоксин + ... 3. На етапі метаболізму - ЛЗ можуть підвищувати або знижувати активність ферментних систем, Що беруть участь у метаболізмі ЛЗ (...На етапі виведення
· Зміна канальцевоїсекреції - хінідин + дигоксин \u003d підвищення концентрації дигоксину в крові та розвиток токсичних ефектів (хінідин ... · зміна канальцевої реабсорбції - реабсорбції піддаються тільки ... 40.Фармакодінаміческое взаємодія лікарських речовин. Антагонізм, синергізм, їх види. Характер зміни ...Побічні і токсичні ефекти лікарських речовин. Тератогенна, ембрітоксіческое, мутагенну дію ліків. Медичні і соціальні аспекти боротьби з лікарською залежністю, наркоманії та алкоголізмом. Поняття про токсикоманіях.
Побічні ефекти - ті ефекти, які виникають при застосуванні речовин в терапевтичних дозах і складають спектр їх фармакологічної дії, можуть бути первинними і вторинними:
а) первинні побічні ефекти - як прямий наслідок впливу даного препарату на певний субстрат (гіпосалівація при застосуванні атропіну для усунення брадиаритмии)
б) вторинні побічні ефекти - побічно виникають несприятливі впливу (АБ, пригнічуючи нормальну мікрофлору, можуть привести до суперінфекції)
токсичні ефекти - небажані ефекти, які проявляються у даного ЛЗ при виході з терапевтичного діапазону (передозування ЛЗ)
Вибірковість дії ЛЗ залежить від його дози. Чим вище доза препарату, тим менше виборчим він стає.
тератогенну дію- здатність ЛЗ при призначенні його вагітній жінці викликати анатомічні аномалії розвитку плода (талідомід: фокомелия, протівобластомние ЛЗ: множинні дефекти)
ембріотоксичну дію - несприятливий вплив, не пов'язане з порушенням органогенезу в перші три місяці вагітності. на більш пізніх термінах проявляється фетотоксіческое дію.
Мутагенну дію ЛЗ - пошкодження зародкової клітини і її генетичного апарату ЛЗ, що проявляється зміною генотипу потомства (адреналін, цитостатики).
Канцерогенну дію ЛЗ - здатність деяких ЛЗ індукувати канцерогенез.
1) Лікарська залежність - стан психіки і / або фізичний стан, Яке є наслідком впливу на організм ЛЗ і характеризується специфічними поведінковими реакціями, важко переборним прагненням повторно приймати ЛЗ, щоб домогтися особливого психічного ефекту або уникнути дискомфорту при відсутності ЛЗ в організмі. Лікарська залежність характеризується:
а) психологічною залежністю - розвитком емоційного дистресу при припиненні прийому ЛЗ. Людина відчуває себе спустошеним, занурюється в депресію, відчуває почуття страху, тривоги, його поведінка стає агресивною. Всі ці психопатологічні симптоми виникають на тлі думок про необхідність ввести собі ЛЗ, що викликало залежність. Прагнення до прийому ЛЗ може коливатися від простого бажання до жагучої спраги прийому ЛЗ, яка поглинає всі інші потреби і перетворюється в сенс життя людини. Вважають, що психологічна залежність розвивається тоді, коли у людини з'являється свідомість того, що оптимального самопочуття він може досягти виключно завдяки введенню ЛЗ. основа психологічної залежності - віра людини в дію ліки (в літературі описані випадки розвитку психологічної залежності до плацебо).
б) фізичною залежністю - порушенням нормального фізіологічного стану організму, яке вимагає постійної присутності в ньому ЛЗ для підтримання стану фізіологічної рівноваги. Припинення прийому ліків викликає розвиток специфічного симптомокомплексу - абстинентного синдрому - комплексу психічних і нейровегетативних розладів у вигляді порушення функції в сторону, протилежну тій, Яка характерна для дії (морфін усуває біль, пригнічує дихальний центр, звужує зіниці, викликає запор; при абстиненції у пацієнта виникають нестерпний біль, часте гучне дихання, зіниці розширені і розвивається наполеглива діарея)
в) толерантністю. Толерантність до засобів, що викликають лікарську залежність часто носить перехресний характер, тобто виникає не тільки Вашого хімічній сполуці, але і до всіх структурно подібним з'єднанням. Наприклад, у пацієнтів з лікарською залежністю до морфіну толерантність виникає не тільки до нього, а й до інших опіоїдних анальгетиків.
Для розвитку лікарської залежності наявність всіх 3 критеріїв не є необхідною умовою.
Опіоїди, барбітурати, алкоголь викликають сильні фізичну, психологічну залежність і толерантність. Анксиолитики (діазепам, альпразолам) переважно викликають психологічну залежність.
2) Наркоманія (наркотична залежність)- це вкрай важка форма лікарської залежності, компульсивний застосування ЛЗ, що характеризується все зростаючим, непереборним потягом до введення даного ліки все збільшуючи його дози. Компульсивність потягу означає, що потреба у введенні ліки домінує у пацієнта над усіма іншими (навіть вітальними) потребами. З позицій даного визначення, Потяг до морфіну - наркоманія, тоді як потяг до нікотину - лікарська залежність.
3) Пристрасть до ліків - характеризує менш інтенсивне потяг до прийому ліків, коли відмова від ліків викликає тільки відчуття легкого дискомфорту, без розвитку фізичної залежності або розгорнутої картини психологічної залежності. Т.ч. пристрасть охоплює ту частину лікарської залежності, яка не підпадає під визначення наркоманії. Наприклад, згадана вище залежність від ліків до нікотину - форма пристрасті.
4) Зловживання лікарськими засобами - самовільне застосування лікарських засобів в таких дозах і такими способами, які відрізняються від прийнятих медичних або соціальних стандартів в даній культурі і в наразі. Т.ч. зловживання ЛЗ охоплює тільки соціальні аспекти застосування ліків. Прикладом зловживання є використання анаболічних стероїдів в спорті або для поліпшення статури молодими чоловіками.
5) алкоголізм - хронічне зловживання алкоголю (етилового спирту), що приводить до тимчасовий до поразки ряду органів (печінки, шлунково-кишкового тракту, ЦНС, серцево-судинної системи, імунної системи) І супроводжується психико-фізичною залежністю.
6) токсикоманія - хронічне зловживання різними ЛЗ (в т.ч. наркотиками, алкоголем, галюциногенами), що виявляється різноманітними психічними і соматичними розладами, порушенням поведінки, соціальною деградацією.
Лікування лікарської залежності важка і невдячна задача. До сих пір не створено ефективної методики, Яка б забезпечувала б успіх лікування більш ніж у 30-40% пацієнтів. Досягнення скільки-небудь помітних результатів можливо тільки при повній кооперації зусиль пацієнта, лікаря і того соціального оточення, В якому знаходиться хворий (принцип добровільності і індивідуальності). В основі сучасних методик лежать наступні принципи:
Психотерапевтичні та трудотерапевтических методи;
Групове лікування і реабілітація (товариства анонімних алкоголіків, наркоманів)
Поступова або різка відміна препарату на тлі детоксикаційної терапії
Проведення замісної терапії (заміна наркотичного засобу повільно і длітельнодействующіе аналогами з їх подальшим скасуванням; наприклад, т.зв. програма метадонової замісної терапії у героїновий наркоманів)
Лікування специфічними антагоністами (налоксоном і налтрексон) або сенсибилизирующими засобами (тетурамом)
Нейрохірургічний методи кріодеструкції поясної звивини і гіпокампу
42.Фармацевтіческое взаємодія лікарських засобів. Попередження і запобіжні заходи при проведенні інфузійної терапії.
Фармацевтична взаємодія -вид взаємодії, пов'язаний з фізико-хімічною реакцією між ЛЗ в процесі виготовлення лікарського препарату, ще до введення цих коштів в організм людини
а) типові помилки, Що призводять до фармацевтичної несумісності: виписування складних рецептів, неправильне зберігання, не враховується можливість адсорбції ЛЗ на поверхні пластмаси (органічні нітрати)
б) проблеми при інфузійної терапії: змішування розчинних солей, похідних нерозчинних слабких кислот або підстав призводить до їх преципітації; в рідких лікарських формах гідролізуються серцеві глікозиди і алкалоїди, руйнуються АБ; рН середовища (в лужному середовищі випадає в осад алкалоїди)
в) рекомендації: 1) Усі суміші краще готувати ex tempore 2) Найбільш надійний розчин з одним ЛЗ 3) Всі розчини перед вживанням необхідно перевірити на наявність суспензій 4) Взаємодія може відбуватися без видимих \u200b\u200bзмін розчинів 5) Не можна додавати ЛЗ в кров і розчини АК 6) При відсутності спеціальних вказівок препарати слід розчиняти в 5% -му розчині глюкози (рН 3,5-6,5), фізіологічному розчині NaCl (рН 4,5-7,0).
Розчин глюкози, стабілізований HCl, несумісний з адреналіном, бензилпенициллином, апоморфіном, канаміцин, вітаміном С, олеандоміцином, серцевимиглікозидами. Серцеві глікозиди несумісні з атропіном, папаверином, платифілін. АБ несумісні з гепарином, гідрокортизоном. Вітаміни групи В несумісні між собою, з вітамінами PP, С. Вітамін РР і С також між собою несумісні.
Не можна змішувати ні з якими іншими препаратами: фенотіазіди, хлорпромазин, барбітурати, препарати вітаміну С, амфотерицин В, фуросемід, сульфадіазин, амінофілін, адреноміметики.
Види фармакотерапії. Деонтологічні проблеми фармакотерапії.
1. Етіотропна ФТ - корекція і усунення причини захворювання (АБ при інфекційних захворюваннях) 2. патогенетична ФТ - вплив на механізм розвитку хвороби (інгібітори ... 3. симптоматична ФТ - усунення симптомів захворювання при неможливості впливу на його причину або патогенез (НПЗЗ ...Основні принципи лікування та профілактика отруєнь лікарськими речовинами. Антидотная терапія (приклади).
Класифікація отруйних речовин (ОР):
1. По приналежності до певних класів хімічних сполук: Барбітурати, бензодіазепіни, ціаніди.
2. За походженням: небиологической природи (кислоти, луги, солі важких металів), токсичні продукти життєдіяльності деяких МБ (ботулотоксин), рослинного походження (Алколоїди, глікозиди), тваринного походження (отрути змій, бджіл)
3. За ступенем токсичності: а) надзвичайно токсичні (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. За токсикологическому дії: а) нервово-паралітичного (бронхоспазм, ядуха) б) шкірно-резорбтивних в) общетоксические (гіпоксичні судоми, кома, паралічі) г) задушливі д) сльозоточиві і дратівливі е) психотропні (порушення психічної активності, свідомості)
5. В залежності від сфери переважного використання: промислові отрути, отрутохімікати, побутові отрути, бойові отруйні речовини, лікарські речовини.
6. В залежності від токсичності ЛЗ: список А - ЛЗ, призначення, застосування, дозування і зберігання яких в зв'язку з високою токсичністю повинні проводитися з високою обережністю. До цього ж списку відносяться ЛЗ, що викликають наркоманію; список В - ЛЗ, призначення, застосування, дозування і зберігання яких повинні проводитися з обережністю у зв'язку з можливими ускладненнями при їх застосуванні без медичного контролю.
Вибірково токсичну дію ЛЗ.
а) кардиотоксическое: серцеві глікозиди, препарати калію, антидепресанти
б) нейротоксическое: психофармакологічні кошти, оксихинолином, аміноглікозиди
в) гепатотоксичні: тетрациклін, левоміцетин, еритроміцин, парацетамол
г) нефротоксичний: ванкоміцин, аміноглікозиди, сульфаніламіди
д) гастроентеротоксіческое: стероїдні протизапальні засоби, нестероїдні протизапальні засоби, резерпін
е) гематотоксичних: цитостатики, левоміцетин, сульфаніламіди, нітрати, нітрити
ж) пневмотоксичних
Токсікокінетіка - вивчає всмоктування, розподіл, метаболізм і виведення ЛЗ, прийнятих в токсичних дозах.
Надходження отруйних речовин в організм можливо а) ентерально б) парентерально. Швидкість і повнота всмоктування відображає швидкість розвитку токсичного ефекту і його вираженість.
Розподіл в організмі: Vd \u003d D / Cmax - дійсний обсяг, в якому розподіляється в організмі отруйну речовину. Vd\u003e 5-10 л / кг - ОВ важко допустимо для його видалення (антидепресанти, фенотіазини). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Передозування - зміна фармакокінетичних процесів: розчинності, зв'язку з білками, метаболізму ® значне підвищення вільної фракції ЛЗ ® токсичні ефект.
Кінетика першого порядку при збільшенні концентрації ЛЗ переходить в кінетику нульового порядку.
Токсигенних стадія - дезінтоксикаційна терапія, соматогенна стадія - симптоматична терапія.
токсікодінамікі . Основні механізми токсичної дії:
а) медіаторний: прямий (по типу конкурентної блокади - ФОС, психоміметиками) і непрямий (активатори або інгібітори ферментів)
б) взаємодія з биомолекулами і внутрішньоклітинними структурами (гемолітичні речовини)
в) метаболізм за типом летального синтезу ( етиловий спирт, Тиофос)
г) ферментний (отрути змій та ін.)
Види дії: місцеве, рефлекторне, резорбтивное.
Класифікація отруєнь:
1. Етіопатогенетична:
а) випадкове (самолікування, помилковий прийом)
б) навмисне (з метою самогубства, вбивства, розвитку у потерпілого безпорадного стану)
2. Клінічна:
а) в залежності від швидкості розвитку отруєння: гостре (надходження одноразово або з коротким інтервалом часу токсичної дози речовини), підгострий (уповільнений розвиток клінічної картини після одноразового прийому), хронічне
б) в залежності від прояву основного синдрому: поразка ССС, ураження ДС і ін.
в) в залежності від тяжкості стану хворого: легкої, середньої, важкої, вкрай важкої
3. Нозологічна: враховує назва ЛЗ, назва групи речовин
Загальний механізм смерті при отруєнні:
а) ураження ССС:
1) зниження артеріального тиску, гіповолемія периферичних судин, Колапс, бради- або тахікардія (трициклічніантидепресанти, бета-блокатори, блокатори кальцієвих каналів)
2) аритмії (шлуночкова тахікардія, фібриляція - трициклічніантидепресанти, теофілін, амфетамін)
б) ураження ЦНС: ступор, кома ® пригнічення дихання (наркотики, барбітурати, алкоголь, гипно-седативні ЛЗ)
в) судоми, м'язова гіперреактивність і ригідність ® гіпертермія, міоглобінурія, ниркова недостатність, гіперкаліємія
Токсикологічна тріада:
1) тривалість застосування, доза і речовина ® анамнез.
2) оцінка стану свідомості за симптомами: дихання, артеріальний тиск, температура тіла
3) лабораторні дані
Основні принципи лікування:
I. перша невідкладна допомога : Штучне дихання, масаж серця, протишокова терапія, контроль за водно-сольовим балансом
II. Затримка всмоктування і видалення з організму не всмоктаної ОВ:
Мета: припинити контакт з ОВ
1. Парентеральний шлях:
а) через легені:
1) припинити інгаляцію
2) подразнюючі речовини (нашатирний спирт, формальдегід) ® закріпити активні рухи, зігріти, дати кисень і піногасники (у нашатирного спирту пеногаситель оцет, а у формальдегіду - розбавлений розчин нашатирного спирту)
б) через шкіру: змити великою кількістю теплої води з милом або миючим засобом, специфічні протиотрути, нейтралізація і припинення дії ОР на шкіру (ФОС: обмивають водою, видаляють за допомогою 10-15% нашатирного спирту або 5-6% розчину бікарбонату натрію з водою; фенолкрезол: рослинне масло або етиленгліколь, але не можна вазелинове масло, KMNO 4: 0,5-1% -ий розчин аскорбінової кислоти або рівні об'єми 3% перекису водню і 3% розчину оцтової кислоти, CCl 4, скипидар, бензин: тепла мильна вода)
в) при ін'єкції в кінцівку: джгут вище місця ін'єкції
г) при попаданні в очі: промивання теплим фізрозчином або молоком протягом 10-20 хвилин, закапати місцевий анестетик; при попаданні кислот і лугів не можна нейтралізувати. Обов'язкова консультація офтальмолога.
2. Ентеральний шлях: звільнити шлунок від ОВ, прискорити пасаж
а) видалення ОВ:
1) попередньо прийом води. Не можна приймати молоко (виняток - їдкі отруйні речовини) і етанол (виняток -метанол).
2) блювота - показана переважно при отруєнні великими таблетками або капсулами, які не можуть пройти через зонд. Можна спровокувати рефлекторно або блювотними засобами (NaCl: 1 столова ложка на 1 склянку води; сироп іпекакуани: дорослим 2 столові ложки, дітям 2 чайні ложки; гірчиця: 1-2 чайні ложки на склянку води; апоморфин: 5-10 мг / кг підшкірно , крім дітей до 5 років). Не можна викликати блювоту після прийому: органічних розчинників - небезпека інгаляцій, миючих засобів - піноутворення, судомних ОВ - небезпека аспірації, їдких речовин - пошкодження стравоходу)
3) зондове промивання шлунка - є екстреним і обов'язковим заходом. Шлунок промивають, якщо з моменту отруєння минуло не більше 4-6 годин, іноді до 10 годин; при отруєнні ацетилсаліциловою кислотою - через 24 години. Попередньо интубируют пацієнта трубкою з раздувной манжетою: в коматозному стані при відсутності кашльового і ларингеального рефлексу. Шлунок промивають водою або фізіологічним розчином 30 ° С, час процедури 4 години і більше. В кінці промивання - активоване вугілля і сульфат натрію.
б) зниження всмоктування з шлунково-кишкового тракту: активоване вугілля всередину після спорожнення шлунка + сульфат натрію або магнію. Особливості заходів щодо зниження всмоктуваності:
1) органічні розчинники: не можна викликати блювоту, промивання шлунка після інтубації, активоване вугілля + вазелінове масло
2) миючі засоби: Не можна викликати блювоту і промивати шлунок, необхідно давати багато води + піногасники (симетикон)
3) кислоти і луги: не можна викликати блювоту, промивання шлунка через зонд, змащений рослинним маслом після введення наркотичного анальгетика - єдине показання для дачі молока. При отруєнні кислотами - антациди, при отруєнні лугу - лимонна або оцтова кислоти.
III. Видалення з організму всмоктався ОВ
а) форсований діурез (умови: достатній нирковий кровообіг і клубочкова фільтрація; за 24 години влити-вилити 20-25 літрів)
б) перитонеальний гемодіаліз
в) гемосорбция
г) обмінне переливання крові
д) форсована гіпервентиляція
IV. Симптоматична терапія функціональних порушень.
2) токсікокінетіческіе - прискорюють біотрансформацію ОВ (трімедоксіма бромід, натрію тіосульфат, етанол, АТ) 3) фармакологічні - атропін, налоксон 4) імунологічні протиотрутиПравила виписування отруйних, наркотичних і сільнодействующіхсредств.
Рецепти на наркотичні в-ва (морфін, омнопон, промедол, фенамін, кокаїн та ін.) І прирівняні до них незалежно від лек. ф-ми виписують на спец. ... В разі, якщо лек. ср-во утримуючі. спирт, то ставиться печатка лік. уста. «Для ... У тих випадках, коли макс. дозу отруйних або сільнод. в-в перевищують, необх. вказати їх кількість прописом з додаванням ...Що будемо робити з отриманим матеріалом:
Якщо цей матеріал виявився корисним для Вас, Ви можете зберегти його на свою сторінку в соціальних мережах:
Інформація про час всмоктування, розподілу та елімінації, тобто про фармагокінетіке лікарських речовин може бути виражена математично. Це необхідно при плануванні режимів клінічного застосування лікарських препаратів. На підставі фармакокінетичних даних розробляються принципи раціонального вибору і дозування останніх. Разом з тим, поряд з цими розрахунками, потрібен постійний клінічний контроль за дією препарату, так як фармакокінетичні дослідження лише доповнюють цей контроль і дозволяють робити більш об'єктивні висновки.
Елімінація більшості лекраственних речовин відбувається відповідно до експоненційної кінетикою, а саме таким чином, що за кожен рівний проміжок часу з організму зникає постійна частина від загальної кількості введеного лікарського речовини. У більшості випадків швидкість ізчезновеніе лікарської речовини з організму відбивається у відповідній швидкості зниження рівня препарату в плазмі.
Концентрація препаратів в біологічних рідинах визначається методом рідинної або газорідинної хроматографії, радіоімунного або ферментнохіміческого аналізу, полярографически або спектрофотометрично. Повторне визначення концентрацій препарату в крові протягом курсу лікування називають терапевтичним моніторингу. Для цієї мети іноді використовують слину, що є безбілкових ультрафільтратом крові.
На підставі отриманих значень будується графік, на осі абсцис якого відзначається час відбору проб, а на осі ординат - концентрація лікарської речовини в біологічній пробі (найбільш часто - в плазмі крові) у відповідних одиницях. Отримана крива характеризує фармакокінетичні процеси, що відбуваються з препаратом. Так, після однократного в / венного введення концентрація лікарської речовини в плазмі зменшується експоненціально. Швидкість експоненціального процесу може бути охарактеризована через константу швидкості (К), що відбиває зміну концентрації за одиницю часу або через період полуекспоненціального процесу (позначається як Т 1/2 або t / 2). Цей період дорівнює часу, необхідному для завершення процесу на 50%.
Про виведення лікарських засобів з організму можна судити по періоду напіввиведення або періоду полуелімінаціі, півжиття, напівіснування, який визначають як час зниження концентрації препарату в крові на 50% від введеної кількості препарату або виведення 50% біодоступного кількості препарату.
Термін "ПЕРІОД полуелімінаціі" більш вдалий, ніж "період напіввиведення", так як ліки не тільки виводяться, а й біотрансформуються. Період полуелімінаціі можна визначити за графіком "концентраціявремя", вимірявши інтервал часу, за який будь-яка концентрація речовини на кривій зменшилася наполовину.
Практично важливо пам'ятати, що за один період напіввиведення
з організму виводиться 50% лікарського засобу, за два періоди - 75%, за три періоди - 90%, за чотири - 94%.
Оскільки для повної елімінації експоненціального типу потрібен час більш тривалий, ніж чотири (4) періоду напіввиведення, то при повторному введендіі препарату через більш короткі проміжки часу відзначається кумуляція (накопичення) його. Підраховано, що для того, щоб досягти плато концентрації, тобто постійної концентрації препарату в плазмі, потрібно близько чотирьох періодів біологічної напівжиття препарату.
Важливо, що зниження елімінації лікарського засобу призводить до подовження біологічного періоду напіврозпаду і пролонгації дії препарату.
У деяких же лікарських засобів фармакологічна дія може бути більш тривалим, ніж можна припустити на підставі їх t / 2. У зв'язку з цим такі препарати, як гормон росту, анаприлін можна вводити з проміжками більш тривалими, ніж їх Т / 2.
Щоб уникнути небезпечного підвищення рівня препарату в плазмі у хворих зі зниженою елімінацією при порушенні функції печінки, нирок або серцево-судинної системи, слід знизити підтримуючі дози його або за рахунок зменшення кожної дози, або за рахунок подовження інтервалів між введенням пропорційно подовженню періоду їх біологічної напівжиття .
БІОЛОГІЧНА ДОСТУПНІСТЬ лікарських засобів
Для надання терапевтичного ефекту лікарська речовина має бути доставлено в ті органи або тканини, в яких здійснюється його специфічну дію (в Біофаза). При внутрішньосудинному введенні ліки відразу і повністю потрапляє в кровоносне русло. При інших шляхах введення (перорально, в / м, п / к і т. Д.) Перш ніж потрапити в кровотік, лікарська речовина має пройти ряд біологічних мембран клітин (слизової шлунка, клітин печінки, м'язів і т. Д.) І тільки тоді якась частина його потрапить в системний кровотік. Ефект препарату багато в чому залежить від того, яка частина від введеної дози лікарського засобу потрапляє в системний кровотік. Цей показник характеризує біологічну доступність кошти (F). Таким чином, посуті, біодоступність ліки відображає концентрацію його у рецепторів, тобто в крові і тканинах організму після всмоктування. Природно, що біодоступність одного і того ж кошти буде різна у кожного хворого. Очевидно, що при внутівенном введенні ліків біодоступність його дорівнює приблизно 100%, а при інших шляхах введення біодоступність майже ніколи не досягає 100%.
Розрізняють абсолютну і відносну біодоступність. Абсолютна біодоступність - це частка поглиненого препарату при позасудинному введенні по відношенню до його кількості після в / венного введення.
Важливим показником є \u200b\u200bВІДНОСНА біодоступність, яка визначає відносну ступінь всмоктування лікарської речовини з випробуваного препарату і з препаратів порівняння. Іншими словами, відносна біодоступність визначається для різних серій препаратів, для лікарських засобів при зраді
ванні технології виробництва, для препаратів, випущених різними виробниками, для різних лікарських форм. Для визначення відносної біодоступності можуть використовуватися дані про рівень вмісту лікарської речовини в крові або ж його екскреції з сечею після одноразового або багаторазового введення. Цей термін важливий при порівнянні 2-х препаратів між собою.
Порівняльна біодоступність одних і тих же препаратів, зроблених різними фірмами (приклад: кокарбоксіназа польського поісхожденія і зроблена в Дніпропетровську), визначається шляхом зіставлення хімічної, біологічної та терапевтичної еквівалентності.
ХІМІЧНА ЕКВІВАЛЕНТНІСТЬ - це збіг у препаратів не тільки хімічної формули ліків, але і збіг ізомерії, просторової конфігурації атомів в молекулі лікарської речовини.
БІОЛОГІЧНА ЕКВІВАЛЕНТНІСТЬ означає одінаковоую, рівну концентрацію діючої речовини в крові при прийомі препарату різних фірм.
Нарешті, ТЕРАПЕВТИЧНА ЕКВІВАЛЕНТНІСТЬ має на увазі однаковий, рівноцінний терапевтичний ефект.
Якщо перераховані 3 характеристики збігаються, кажуть, що лікарські препарати мають рівний біодоступністю (біодоступності). В даний час є багато прикладів того, що аналогічні препарати біологічно нееквівалентний внаслідок відмінностей у біодоступності. Практикуючий лікар повинен пам'ятати про це, особливо при перекладі хворого з одного препарату на аналогічний препарат іншої фірми.
Безумовно, що на всі ці питання може дати відповідь тільки нова наука - а саме КЛІНІЧНА ФАРМАКОЛОГІЯ. Це самостійна наука зі своїм предметом і завданнями дослідження. Чому вона виділилася в самостійний предмет? Перш за все тому, що, як виявилося, не все можна вивчати в експерименті на тварин. наприклад, психічні процеси, Які надзвичайно властиві лише людині.
Бурхливий розвиток фармацевтичної промисловості привело до створення величезної кількості лікарських засобів. З'явилася лавина препаратів, які створили своєрідні лікарські джунглі. Ситуація, що склалася вельми ускладнює вибір потрібного засобу навіть в одній групі лікарських препаратів, заважає лікаря зорієнтуватися на оптимальне для конкретного хворого засіб. На всі ці питання допомагає відповісти клінічна фармакологія.
Як приклад можна привести можливості вибору препарату при колагенозах (хвороби сполучної тканини, ревматоїдний артрит, ревматизм, системний червоний вовчак і т. Д.). З однією
боку - ацетилсаліцилова кислота (аспірин), але разом з тим, є інші сучасні ненаркотичні анальгетики, що володіють, в порівнянні з аспірином, низку переваг: напроксен, піроксикам і т. д.
Що краще, який препарат даному хворому буде більш адекватний, який дає найбільш виражений терапевтичний ефект? На ці питання і допомагає відповісти клінічна фармакологія.
Основними завданнями клінічного фармаколога є:
1) Вибір лікарських засобів для лікування конкретного біль
2) Визначення найбільш підходящих для нього лікарських
форм і режиму їх застосування.
3) Вибір шляху введення препарату.
4) Моніторні спостереження за дією препарату.
Для цієї мети ставлять датчики, що дають постійну картину концентрації препарату в крові на моніторі. Вивчаються всі інші аспекти фармакокінетики.
5) Вивчення небажаних реакцій і побічних ефектів на ліки, їх усунення, а також вивчення наслідків взаємодії ліків у даного хворого.
6) Передача накопичених знань шляхом навчання.
7) Організація лабораторних та інформаційних служб, А також консультації з планування досліджень (ВООЗ, 1971).
ФАРМАКОДИНАМІКА (ФД) - це розділ фармакології, що вивчає
1) механізми дії (тобто сутність процесів взаємодії з тканинними, клітинними або субклітинному рецепторами - специфічними або неспецифічними) 1.
1 02) фармакологічні ефекти (тобто зміст і зміни впли яния препарату в залежності від віку, статі хворого, характеру та перебігу захворювання, супутньої патології), а також 3) локалізацію дії ліків. Більш коротко ФД можна визначити як розділ фармакології, що вивчає дію лікарських засобів на організм.
Зазвичай механізм дії лікарського засобу вивчається в експериментах на тваринах, так як майже завжди вони однакові у тварин і людини. Знання механізму дії лікарського засобу дозволяє лікарю осмислено вибрати необхідний препарат для лікування.
Механізмів дії лікарських засобів багато, але всі їхні умовно можна звести в 2 групи.
Перша група механізмів пов'язана з тими випадками, коли ліки діють на спеціфіцескіе рецептори, - тобто це рецепторні механізми.
Друга група механізмів пов'язана з ліками, які в силу своїх фізико-хімічних властивостей діють не через рецептори. Тут перш за все можна вказати дію лікарських засобів на специфічні ферменти їх фізико-хімічний вплив на мембрани клітин і пряме хімічну взаємодію з речовинами клітин.
Як приклад нерецепторних механізмів можна привести
випадок із засобами для наркозу, скажімо з фторотаном. Він є відмінним розчинником жирів, тому перш за все діє на мембрани нервових клітин, викликаючи фармакологічний ефект - наркоз.
Розберемо основні, найчастіше зустрічаються рецепторине механізми дії лікарських засобів.
Рецептори в фармакологічному плані є функціональні біохімічні макромолекулярні мембранні структури, вибірково чутливі до дії певних хімічних сполук, а в нашому випадку до дії лікарських засобів. дослідження останніх років показали, що фармакологічні рецептори є білки або ферменти (G-білки - одиночна пептидная ланцюг з 7 доменів) - в цьому їх принципова відмінність від морфологічних рецепторів.
Виборча чутливість ліки до рецептора означає той факт, що лікарська речовина може, по-перше, зв'язуватися з рецептором, тобто володіє аффинитетом або спорідненістю до нього. Іншими словами, спорідненість або афінітет означає здатність лікарської речовини до зв'язку з рецептором.
Спорідненість або афінітет відображає кінетичні константи, що зв'язують лікарська речовина, рецептор і реакцію на молекулярному рівні. Взаємодія лікарських речовин з рецептором призводить до виникнення ряду біохімічних і фізіологічних змін в організмі, які виражаються в тому чи іншому ефекті.
Другою характеристикою лікарського речовини є здатність його викликати фармакологічний відповідь, ефект після взаємодії з рецептором. Ця здатність позначається як внутрішня активність лікарського засобу або його ефективність. До певної міри біологічна реакція регулюється шляхом зміни числа рецепторів і їх чутливості.
В процесі еволюції утворилися рецептори, чутливі до різноманітних ендогенних регуляторів. Згідно рецепторной теорії, механізм дії лікарських засобів полягає в зміні швидкості функціонування специфічних систем організму при впливі природних медіаторів або екзогенних речовин на рецептори.
Лікарські засоби, дія яких пов'язана з прямим порушенням або підвищенням функціональних можливостей (Здібностей) рецепторів, називаються агоністами, а речовини, що перешкоджають дії специфічних агоністів, - антагоністами. Іншими словами, якщо лікарська речовина має обидві характеристики (тобто і спорідненість і внутрішню активність), то воно є агоністом. Тому, агоніст - це речовина з високим аффинитетом до рецептора і високою внутрішньою активністю. Якщо ж речовина має здатність тільки зв'язуватися з рецептором (тобто має спорідненості), але при цьому не здатне викликати фармакологічні ефекти, то воно викликає блокаду рецептора і називається антагоністом.
Препарати, які мають той же спорідненість до рецептора, що і агоніст, або більш слабке, але володіють менш вираженою внутрішньою
активністю, називаються частковими агоністами або агоністом-антагоністом. Ці препарати, які використовуються одночасно з агоністами, знижують дію останніх внаслідок їх здатності займати рецептор.
Приклад: атропін - має велику активність, ніж ацетилхолін (ендогенний медіатор). Атропін провзаимодействует з рецепторами, але так як не має внутрішньої активності, фізіологічного ефекту не викличе. З огляду на більшої спорідненості до рецептора в порівнянні з ацетилхоліном, він буде перешкоджати дії агоніста, а саме ацетилхоліну, а значить бути його антагоністом.
Лікарські речовини можуть діяти подібно або протилежно ендогенних медіаторів. Якщо лікарська речовина діє подібно до медіатора (ацетилхоліну, норадреналіну та ін.), - таку речовину називається миметики. Mim - корінь "мім", пантоміма, мімікрія. Звідси холиномиметик, адреномиметик.
Лікарська речовина, що перешкоджає взаємодії медіатора з рецептором, називається блокатором (холіноблокатор, адреноблокатор, гистаминоблокатор і т. Д.).
У літературі можна зустріти термін "литик" (лізис - розчинення, фізичний процес). Термін досить старий, проте іноді використовується (холинолитик, адренолитики). Таким чином, терміни "литик" і "блокатор" використовують як синоніми.
У медичній практиці все більш широке застосування знаходить одночасне призначення декількох лікарських засобів. При цьому вони можуть взаємодіяти один з одним, змінюючи вираженість і характер основного ефекту, його тривалість або послаблюючи побічні і токсичні впливи. У зв'язку з цим спеціальний розділ фармакодинамики присвячений ВЗАЄМОДІЇ лікарських засобів, яке класифікують наступним чином. Виділяють Фармакологічна взаємодія і ФАРМАЦЕВТИЧНЕ взаємодія.
Фармацевтична взаємодія пов'язано з фармацевтичною несумісністю ліків в процесі їх виготовлення або зберігання, а також при змішуванні в одному шприці. При цьому имевшаяся раніше фармакологічна активність у препаратів знижується або зникає, а іноді з'являються навіть нові, токсичні властивості.
Фармакологічна взаємодія ліків пов'язано зі змінами їх фармакокінетики, фармакодинаміки або засноване на хімічному і фізико-хімічній взаємодії в середовищах організму. При цьому лікарські препарати можуть взаємодіяти один з одним на будь-якому етапі проходження їх через організм хворого: при всмоктуванні, у транспортній фазі, в процесі метаболізму, а також екскреції (фармакокінетична взаємодія).
Фармакодинамічна взаємодія відображає зміну викликаються кожним препаратом окремо процесів, пов'язаних з реалізацією ефекту. Інакше кажучи, фармакодинамічний тип взаємодії заснований на особливостях змін механізмів і локалізації дії використовуваних лікарських засобів, їх основних ефектів. Якщо взаємодія здійснюється на рівні рецепторів, то воно в основному стосується агоністів і антагоністів різних типів рецепторів. При цьому одне лікарська речовина може посилювати чи послаблювати дію іншого. Якщо лікарські ве
щества діють відносно ефекту однонаправленно - це препарати синергисти (син - разом, ерго - робота). Таким чином, синергізм супроводжується посиленням кінцевого ефекту. Як правило, ці лікарські речовини діють на одні й ті ж рецептори. Виділяють 2 варіанти синергізму:
1) Ефекти збігаються за принципом простої суми. Підсумований (або адитивний, - лат. - additio - додаток). Ефект спостерігається при простому додаванні ефектів кожного з компонентів. Наприклад, так взаємодіють засоби для наркозу (закис азоту + фторотан). Аналогічний варіант адитивного ефекту при одночасному використанні аспірину і анальгіну. Навіщо це треба знати? Якщо аспірин хворий змушений приймати тривалий час, То потрібно врахувати, що Аспірин діє ульцерогенной, тобто викликає виразки слизової оболонки шлунково-кишкового тракту, а Анальгін має таким небажаним ефектом як пригнічення кровотворення. З огляду на адитивний аналгетичний ефект, можна без существнного ризику його виникнення знизити, істотно зменшити дозування обох засобів, прийнятих хворим.
2) Другий варіант синергізму - потенціювання або посилення ефекту. Даний варіант виникає тоді, коли при введенні двох речовин загальний ефект перевищує суму ефектів обох засобів. Як приклад можна привести взаємодія нейролептиків (аміназин) і засобів для наркозу, взаємодія антибіотиків і протимікробних сульфоніламідів.
Іноді виділяють третій (3) варіант синергізму, - сенситизацию. Сенситизация - коли один препарат у мінімальній дозі підсилює дію іншого в їх комбінації (застосування малих доз інсуліну в поєднанні з KCl збільшує рівень проникнення калію в клітини).
Крім синергізму існує явище антагонізму. Здатність однієї речовини в тій чи іншій мірі зменшувати ефект іншого називають антагонізмом, тобто в даному випадку одне лікарський засіб перешкоджає дії іншого.
Виділяють фізичний, хімічний і фізіологічний антагонізм. даний вид взаємодії найчастіше використовується при передозуванні або гострому отруєнні лікарськими засобами. Прикладом ФІЗИЧНОГО антагонізму може бути вказана здатність адсорбуючих засобів ускладнювати всмоктування речовин з травного тракту (Активоване вугілля, адсорбує на своїй поверхні отрута; холестирамин).
Ілюстрацією ХІМІЧНОГО взаємодії може бути освіту комплексонів (іони деяких важких металів - ртуті, свинцю - пов'язує пенициламин, ЕДТА), або так взаємодіє соляна кислота шлунка і бікарбонат натрію (луг).
ФІЗІОЛОГІЧНИЙ антагонізм пов'язаний із взаємодією ліків на рівні рецепторів, про характер якого вже говорилося вище.
За аналогією з синергізмом виділяють ПРЯМИЙ (коли обидва лікарських з'єднання діють на одні й ті ж рецептори) і ПОБІЧНІ (різна локалізація дії лікарських засобів) антагонізм. У свою чергу прямий антагонізм буває КОНКУРЕНТНИЙ і НЕ
КОНКУРЕНТНИЙ. При конкурентному антагонізмі лікарська речовина вступає в конкурентні відносини з природними регуляторами (медіаторами) за місця зв'язування в специфічних рецепторах. Блокада рецептора, викликана конкурентним антагоністом, може бути знята великими дозами речовини-агоніста або природного медіатора.
Неконкурентний антагонізм - це та ситуація, коли лікарська речовина не може витіснити природний медіатор з рецептора, але утворює з ним (медіатором) ковалентні зв'язки.
ТОЧКИ Взаємодія лікарських засобів Основна
маса рецепторів розташована на зовнішній і внутрішній стороні мембрани клітини і її органелах. До найбільш частих точках взаємодії ЛЗ відносяться: 1) медіатори і гормональні рецептори; 2) АТФ-фаза Na / K насоса, Ca, K і Na - внутрімембранние канали.
Останнє ще раз доводить, що ЛЗ діють на доступні ключові механізми білогіческіе реакцій, тобто на філогенетично детерміновані процеси, а не шляхом створення якихось нових реакцій.
Взаємодія ЛЗ з рецептором відбувається на рівні хімічних або фізико-хімічних процесів. Найбільш часто характер реакції, її сила, оборотність і тривалість обумовлені властивостями зв'язку ЛЗ з рецептором. Міцність зв'язку залежить від відстані електростатичного взаємодії між двома атомами. Як правило, характер взаємодії складний, в ньому можуть брати участь різні види зв'язку, що визначається комплементарностью ЛЗ і рецептора, ступенем зближення їх між собою.
Найслабші зв'язку - вандерваальсови (визначають специфічність взаємодії речовин з реактивними системами). У більшості випадків між ЛЗ і рецептором виникають іонні зв'язку (оборотний характер).
ВИДИ ДІЇ ЛІКІВ
1) МІСЦЕВЕ ДІЯ - дія речовини, що виникає на місці його застосування. Приклад: використання місцевих анестетиків - внесення розчину дикаїну в порожнину кон'юнктиви. Використання 1% розчину новокаїну при екстракції
зуба. Цей термін (місцеву дію) дещо умовний, так як істинно місцеве дію спостерігається вкрай рідко, в силу того, що так як речовини можуть частково всмоктуватися, або надавати рефлекторну дію.
2) рефлекторної дії - це коли лікарська речовина діє на шляхах рефлексу, тобто воно впливає на Екстер або інтерорецептори і ефект проявляється зміною стану або соотвтетствующіх нервових центрів, або виконавчих органів. Так, використання гірчичників при патології органів дихання покращує їх трофіку рефлекторно (ефірне гірчичне масло стимулює екстерорецептори шкіри). Препарат цититон (дихальний аналептик) надає збудливу дію на хеморецептори каротидного клубочка і, рефлекторно стимулюючи центр дихання, збільшує об'єм і частоту дихання. Інший приклад - використання нашатирного спирту при непритомності (аміак), рефлекторно поліпшує
мозковий кровообіг і тонізірующго життєві центри.
3) резорбтивної дії - це коли дія речовини розвивається після його всмоктування (резорбція - всмоктування; лат. - resorbeo - поглинати), надходження в загальний кровотік, потім в тканини. Резорбтивна дія залежить від шляхів введення лікарського засобу та його здатності проникати через біологічні бар'єри. Якщо речовина взаємодіє тільки з функціонально одноз почнемо рецепторами певної локалізації і не впливає на інші рецептори, дія такого речовини називається ВИБОРЧИМ. Так, деякі курареподібних речовини (міорелаксанти) досить вибірково блокують холінорецептори кінцевих пластинок, викликаючи розслаблення скелетних м'язів. Дія препарату празозину пов'язано з виборчим, блокуючим постсинаптические альфа-один адренорецептори ефектом, що веде в кінцевому результаті призведе до зниження артеріального тиску. Основою вибірковості дії ЛЗ (селективності) є спорідненість (афінітет) речовини до рецептора, що визначається наявністю в молекулі цих речовин певних функціональних угруповань і загальної структурної організацією речовини, найбільш адекватною для взаємодії з даними рецепторами, тобто комплементарності.
Загальна характеристика ДІЇ лікарських засобів НА ОРГАНІЗМ
Незважаючи на велику кількість лікарських засобів, все імзененія,
визивавемие ними в організмі, мають певну спільність і
однотипність. Виходячи з поняття норми реакції, розрізняють 5
типів змін,
викликаються фармакологічними засобами (Н. В. Вершинін):
1) тонизирование (підвищення функції до норми);
2) порушення (підвищення функції понад норму);
3) заспокійливу дію (седативну), тобто зниження підвищеній функції до норми;
4) пригнічення (зниження функції нижче норми);
5) параліч (припинення функції). Сума тонізуючого і віз
спонукає ефектів називаетсярующім дією.
ОСНОВНІ дія ЛІКІВ
Перш за все, розрізняють:
1) фізіологічні ефекти, коли ліки викликають такі зміни, як підвищення або зниження артеріального тиску, частоти серцевих скорочень і т. Д .;
2) біохімічні (підвищення рівня ферментів в крові, глюко
зи і т. д.). Крім того, виділяють ОСНОВНІ (або головні) і
Неосновних (другорядні) ефекти ліків. ОСНОВНИЙ ЕФ
Фекта - це той, на якому лікар будує свої розрахунки при лікуванні даного (!) Хворого (анальгетики - для знеболюючого ефекту, гіпотензивні - для зниження артеріального тиску і т. П.).
Неосновних, або неголовні ефекти, додаткові інакше, ті, які притаманні даного засобу, Але розвиток яких у даного хворого необов'язково (анальгетики ненаркотичні - крім знеболюючого ефекту викликають жарознижувальний ефект і т. П.). Серед неосновних ефектів можуть бути бажаних і небажаних (або Побічна) ефекти.
Приклад. Атропін - розслаблює гладку мускулатуру внутрішніх
органів. Однак при цьому він одночасно поліпшує провідність в АВузле серця (при блокаді серця), збільшує діаметр зіниці і т. Д. Всі ці ефекти потрібно розглядати індивідуально в кожному конкретному випадку.
ФАКТОРИ, ЩО ВПЛИВАЮТЬ НА ВЕЛИЧИНУ ЕФЕКТУ лікарських
1) Перш за все, потрібно пам'ятати про фармакокінетичні факторах, властивих кожному препарату. Про це вже говорилося вище, нагадаю лише, що мова йде про свою швидкості всмоктування або абсорбції, біотрансформації, екскреції (препарату, лікарського засобу).
2) Друга група чинників - фізіологічні.
а) Вік. Дійсно, всі добре знають про те, що з віком змінюється чутливість хворого до лікарських засобів. Виділилися навіть в зв'язку з цим:
Перинатальна фармакологія;
Педіатрична фармакологія;
Геріатричний фармакологія;
Репродуктивна фармакологія;
б) Маса хворого. Відомо, що чим більше маса, тим вище
доза. Тому ЛЗ дозують в (мг / кг).
у підлогу. Виявляється різна чутливість у чоловіків і жінок
до деяких речовин, наприклад, до нікотину, алкоголю і т. п.,
що пояснюється відмінністю метаболізму, різницею питомої
ваги жирового прошарку і т. п
в) Стан організму. Дія ЛС на організм після су
щественной фізичного навантаження буде іншим, ніж без такої.
д) біологічні ритми (Добові, місячні, сезонні, годо
ші, а зараз навіть популяційні) надають найсерйозніше
вплив на дію ЛЗ в організмі. 3) Патологічні факто
ри (наприклад рівень гормональної активності). Так при ба
зедовой хвороби легше переносять токсичні дози морфіну, але підвищується чутливість міокарда до адреналіну. 1 0Еффект серцевихглікозидів на кровообіг проявляється тільки на тлі серцевої недостатності. Дія ЛС істотно змінюється при гіпо- та гіпертермії, при інфекційних захворюваннях, при зміні функціонального стану центральної нервової системи і т. Д.).
4) Генетичні чинники. Відомо, що відсутність ферменту глюкозо-6-фосфатдегідрогенази (Г-6-ФДГ) при талассеніі, унеможливлює призначення антималярійних препаратів типу примахин. Недостатність ферменту БУТИРИЛХОЛІНЕСТЕРАЗИ в крові, що зустрічається у одного з 2500 чоловік, є причиною тривалої миорелаксации на введення дитилина.
5) Внушабельность хворих або плацебо ефект. В цьому плані антиангінальний ефект ліків плацебо, наприклад, досягає 40% і до 81% ефект-плацебо виникає від ін'єкційного шляху введення препаратів. Ймовірно тому використання вітамінних препаратів, Тонізуючих засобів, транквілізаторів багато в чому обумовлені цим ефектом.
6) Доза ліки. Дія ЛС в дуже великій мірі визначається їх дозою. Дозою називають кількість лікарського ве
щества, призначене на один прийом (зазвичай позначається як разова доза). Від дози лікарського засобу залежить не тільки ефективність лікування, але і безпеку хворого. Ще в кінці ХУШ століття Вільям Візерінг писав: "Яд в малих дозах - найкращі ліки; корисні ліки в занадто великій дозі - отрута". Це тим більш правильно в наш час, коли в медичну практику введені надзвичайно активні лікарські засоби, дозування яких вимірюються частками міліграма.
Позначають дозу в грамах або в долях грама. Для більш точної дозуванні препаратів розраховують їх кількість на 1 кг маси тіла (або на 1 кв. М площі тіла), наприклад, 1 мг / кг; 1 мкг / кг і т. Д. Лікарю необхідно бути орієнтованим не тільки в дозі, розрахованої на одноразовий прийом (pro dosi), але і в добовій дозі (pro die).
Мінімальні дози, в яких лікарські засоби викликають початковий біологічний (терапевтичний) ефект, називаються граничними, або мінімально діючими (терапевтичними) дозами. У практичній медицині найчастіше використовують середні терапевтичні дози, в яких лікарські засоби надають необхідне оптимальне Фармакотерапевтична дія. Якщо при їх призначенні хворому ефект недостатньо виражений, дозу підвищують до вищої терапевтичної дози. Вищі терапевтичні дози можуть бути разовими і добовими. Вища разова доза - це максимальна кількість лікарського препарату, яке без шкоди для хворого може бути введено одноразово. Цими дозами користуються рідко, в крайніх випадках (в ургентної, невідкладної ситуації). Середні терапевтичні дози становлять зазвичай 1 / 3-1 / 2 від вищої разової дози.
Вищі терапевтичні дози отруйних і сильнодіючих речовин наведені в Державній фармакопеї СРСР. У деяких випадках, наприклад, при використанні хіміотерапевтичних засобів, вказується доза препарату на курс лікування (курсова доза). Якщо виникає необхідність швидко створити високу концентрацію лікарського засобу в організмі (сепсис, серцево-судинна недостатність), то користуються першою дозою, так званої ударною дозою, яка перевищує всі наступні. Розрізняють також токсичні (надають небезпечні ефекти) і смертельні дози.
Лікарю важливо знати ще одну характеристику, - а саме поняття про широту терапевтичної дії препарату. Під широтою терапевтичної дії розуміють відстань, діапазон від мінімально терапевтичної до мінімальнотоксіческой дози. Природно, що чим більше ця дистанція, тим більш безпечний цей препарат.
1/20 дози х кількість років дитині.
Для кількісної характеристики і оцінки ефективності нового фармакологічного засобу застосовують, як правило, два стандартних порівняння - або з плацебо, або з препаратом анало
гічного типу дії, що є одним з найбільш ефективних у цій групі засобів.
Плацебо (пустушка) - це індиферентне речовина в лікарській формі, що імітує певний фармакологічний або лікарський засіб. Застосування плацебо необхідно при наявності: а) ефекту предположительности, впливу особистості, очікування і упередженого ставлення з боку хворого або дослідника; б) спонтанних змін в перебігу хвороби, симптомів, а також явищ, які пов'язані з лікуванням.
Плацебо - латинський термін, що означає: "Я можу доставити вам задоволення".
Ефект плацебо - це ефект, викликаний над специфічними фармакодинамічні властивості препарату при даній патології, а ФАКТОМ ЗАСТОСУВАННЯ препаратів, який впливає психологічно. Препарати плацебо зазвичай фармакологічно інертні, вони містять неактивні речовини, подібні до крохмалю або лактози. Плацебо використовують в клінічних дослідженнях для того, щоб встановити ефект навіювання з боку як хворого, так і лікаря, особливо якщо вивченню підлягають кошти, призначені для лікування бронхіальної астми, Гіпертонічної хвороби, стенокардії, ІХС. У таких випадках препарат плацебо не повинен за кольором і іншим фізичними властивостями (Запах, смак, форма) відрізнятися від активного препарату. Плацебо більш ефективно, коли і лікар, і хворий мало поінформовані про нього.
ПРИКЛАД. при ішемічної хвороби серця (ІХС) якщо одній групі хворих на ішемічну хворобу серця призначаємо активну ліки, а інший - плацебо, то у 40% хворих другої групи напади стенокардії купіруються.
найбільш виражений ефект плацебо (до 81%) спостерігають при ін'єкційних шляху введення його. Мікстури і таблетки менш ефективні.
У літературі, присвяченій лікарського впливу на хворого, часто звучить термін ФАРМАКОТЕРАПІЯ (ФТ). Фармакотерапія - розділ фармакології, що вивчає терапію хворого лікарськими препаратами.
розрізняють наступні види фармакотерапії:
1) етіотропне - ідеальний вид фармакотерапії. Цей вид ФТ спрямований на усунення причини хвороби. Прикладами етіотропної ФТ можуть бути лікування протимікробними засобами інфекційних хворих (бензилпеніцилін при стрептококової пневмонії), застосування антидотів при лікуванні хворих з отруєннями токсичними
речовинами. 2) патогенетичних ФАРМАКОТЕРАПІЯ - спрямована
на усунення або
придушення механізмів розвитку хвороби. Більшість вживаних в даний час ліків відноситься саме до групи препаратів патогенетичної ФТ. Антигіпертензивні засоби, серцеві глікозиди, антиаритмічні, протизапальні, психотропні та багато інших лікарські препарати надають терапевтичну дію шляхом пригнічення відповідних механізмів розвитку захворювання.
3) симптоматична терапія - спрямована на усунення або
обмеження окремих проявів хвороби. До симптоматичним лікарських засобів можна віднести знеболюючі препарати, які не впливають на причину або механізм розвитку хвороби. Протикашльові засоби - також хороший приклад симптоматичних засобів. Іноді ці кошти (усунення больового синдрому при інфаркті міокарда) можуть робити істотний вплив на перебіг основного патологічного процесу і при цьому грати роль засобів патогенетичної терапії.
4) ЗАМІСНА ФАРМАКОТЕРАПІЯ використовується при дефіциті природних біогенних речовин. До засобів замісної терапії відносяться ферментні препарати (панкреатин, панзинорм та т. Д.), Гормональні лікарські засоби (інсулін при цукровому діабеті, тиреоидин при мікседемі), препарати вітамінів (вітамін Д, наприклад, при рахіті). Препарати замісної терапії, не усуваючи причини захворювання, можуть забезпечувати нормальне існування організму протягом багатьох років. Не випадково така важка патологія як цукровий діабет - вважається особливим стилем життя у американців.
5) ПРОФІЛАКТИЧНА ТЕРАПІЯ проводиться з метою попередження захворювань. До профілактичних належать деякі противірусні засоби (Наприклад, при епідемії грипу - ремантадин), дезінфікуючі препарати та ряд інших. Застосування протитуберкульозних препаратів типу ізонізіда також можна вважати профілактичної ФТ. хорошим прикладом проведення профілактичної терапії є використання вакцин.
Від фармакотерапії слід відрізняти хіміотерапії. Якщо ФТ має справу з двома учасниками патологічного процесу, а саме - ліками і макроорганизмом, то при хіміотерапії є вже 3 учасники: ліки, макроорганизм (хворий) і збудник хвороби.
Говорячи про дозах, ми перш за все мали вказували на аллопатические дози, на відміну від гомеопатичних. Тому кілька слів про ГОМЕОПАТІЇ. Термін "гомеопатія" утворений від двох грецьких слів: homois - подібний і pathos - страждання, хвороба. Дослівно гомеопатія перекладається як подібна, подібна хвороба. Засновник гомеопатії німецький вчений Самуель Ганеман у своїй знаменитій книзі "Органон лікарського мистецтва або основна теорія гомеопатичного лікування" ще в початку XIX століття (1810 рік) виклав основні принципи цієї науки. Принципів цих кілька, але 2 з них є основними:
1) Це закон подібності, який свідчить, що лікування хвороб необхідно здійснювати подібним, схожим засобом. Згідно з цим принципом Ганеман радить "наслідувати природі, яка іноді виліковує хронічну хворобу за допомогою іншої країни, що приєднується хвороби". Тому "проти хвороби, що підлягає лікуванню (переважно хронічної), слід застосовувати такий лікарський речовина, яке в змозі викликати іншу, щонайможливої \u200b\u200bподібну штучну хворобу, і перша буде вилікувана". Similia
similibus (подібне подібним). Наример, жовтяницю слід лікувати жовтим і т. П.
2) Другий принцип - лікувати супермалий дозами. Розведення лікарських засобів, що використовуються гомеопатами обчислюються декількома порядками, іноді доходячи до їх десятків: 10 в п'ятій; 10 в десятій; 10 в вісімнадцятої і більш ступеня (тобто мільйонні
і більше частки грамів). Щоб пояснити ефект застосування ле
карственних речовин в
високих розведеннях Ганеман висунув умоглядну концепцію: "Малі дози відрізняються особливою духовною силою, більшою активністю, здатністю проникати в уражені органи і тканини".
Не відомо, чи як щодо особливої \u200b\u200bдуховної сили, але наукове життя в останнє десятиліття пред'явила дуже серйозні докази для справедливості твердження Ганемана. Так, наприклад, досліди француза Жака Беквеніста, зроблені ним з розведенням речовин в 10 в вісімдесятої ступеня раз показали, що молекули води мають "пам'яттю" на присутність даної речовини, викликаючи певний фізіологічний ефект. Якщо зазначений даний факт знайде в найближчому майбутньому підтвердження, тобто якщо встановлять, чи не є молекули води джерелом інформації, безумовно ми стоятиме біля основ найбільшого відкриття, смогущего пояснити і терапевтичну ефективність гомеопатичних засобів.
Далі розглянемо розділ, що стосується ФАРМАКОЛОГІЧНИХ АСПЕКТІВ ТОКСИЧНОГО ДІЇ ЛІКІВ, а саме токсикології ЛІКІВ. Токсикологія ліків - розділ фармакології, який вивчає токсичні ефекти цих засобів. Однак зараз більш правильно говорити про небажаних реакціях організму людини на ліки. Даний факт відомий давно, накопичений багатий фактичний матеріал, який свідчить про те, що небажані реакції різного ступеня можуть виникати при прийомі майже всіх лікарських препаратів.
Існує багато класифікацій побічних ефектів лікарських засобів і ускладнень фармакотерапії, хоча жодна з них не досконала. Разом з тим, виходячи з патогенетичного принципу, все небажані ефекти або реакції можна поділити на 2 типи:
1) небажані реакції, пов'язані з
а) передозуванням ліків
б) отруєннями;
2) токсичні реакції, пов'язані з фармакологічними властивостями ліків.
Передозування виникає зазвичай при використанні високих доз препаратів. Особливо часто передозування виникає при прийомі лікарських засобів, що мають малу широту терапевтичної дії. Наприклад, проявів токсичності важко уникнути при використанні антибіотиків аміноглікозидів (стрептоміцину, канаміцину, неоміцину). Названі препарати викликають вестибулярні порушення і глухоту при лікуванні в дозах, які не набагато перевищують терапевтичні. Для деяких ліків просто неможливо уникнути токсичних ускладнень (протипухлинні, цитотоксичні препарати), які пошкоджують все швидко діляться клітини і уг
нета відсталий мозок при одночасному ефективному впливі на ріст пухлинних клітин.
Крім того, передозування може бути пов'язана не тільки з використанням високих доз, а й з явищем кумуляції (серцеві глікозиди).
Отруєння можуть бути випадкові і навмисні. Навмисні отруєння зазвичай відбуваються з суіціідальной метою (з метою самогубства). За Омської області найбільш часто в загальній структурі отруєнь займають отруєння прижигающими рідинами, на другому місці стоять лікарські отруєння. Це, перш за все, отруєння снодійними, транквілізаторами, ФОС, алкоголями, чадним газом.
Незважаючи на відмінність етіологічних факторів, заходи допомоги на етапах лікарського допомоги прнціпіально схожі.
Ці принципи наступні:
1) БОРОТЬБА З невсосавшихся отрутою З ШКТ. Найчастіше це потрібно при пероральному отруєнні отрутою. Найбільш часто гострі отруєння викликані прийомом речовин всередину. Обов'язковою і екстреним заходом в цьому плані є промивання шлунка через зонд навіть через 10-12 годин після отруєння. Якщо хворий у свідомості, промивання шлунка здійснюється за допомогою великої кількості води і подальшого викликання блювоти. блювоту викликають механічним шляхом. У несвідомому стані промивання шлунка хворому здійснюють через зонд. Необхідно спрямувати зусилля на адсорбцію знаходиться в шлунку отрути, для чого використовують активоване вугілля (по 1 столовій ложці всередину, або 20-30 таблеток одночасно, до і після промивання шлунка). Шлунок промивають кілька разів через 3-4 години до повного очищення від речовини.
Блювота протипоказана в наступних випадках:
При коматозних станах;
При отруєнні коррозівного рідинами;
При отруєнні гасом, бензином (можливість гідрокарбонатної пневмонії з некрозом тканини легені і т.д.).
Якщо потерпілий є маленькою дитиною, то для промивання краще використовувати сольові розчини в малих обсягах (100-150 мл).
З кишечника отрута найкраще видаляти за допомогою сольових проносних. Тому після закінчення промивання можна ввести в шлунок 100-150 мл 30% розчину сульфату натрію, а ще краще сульфату магнію. Сольові проносні є найпотужнішими, швидко чинними протягом усього кишечника. Дія їх підпорядковується законам осмосу, тому вони протягом короткого періоду часу припиняють дію отрути.
Добре дати в'яжучі (розчини таніну, чай, хліб), а також обволікаючі (молоко, білок яєць, рослинне масло).
При нашкірному попаданні отрути необхідно ретельно промити шкірні покриви, найкраще заторної водою. При попаданні токсичних речовин через легені слід припинити їх інгаляцію, видаливши потерпілого з отруєної атмосфери.
При підшкірному введенні токсичної речовини всмоктування його з місця введення можна уповільнити ін'єкціями розчину адреналіну
навколо місця введення речовини, а також охолодженням цій галузі (лід на шкіру в місці ін'єкції).
2) Другий принцип допомоги при гострому отруєнні полягає в ДІЇ НА всмоктатися ЯД, ВИДАЛЕННЯ ЙОГО З ОРГАНІЗМУ.
З метою якнайшвидшого виведення токсичної речовини з організму застосовують перш за все, форсований діурез. Суть цього методу полягає в поєднанні посиленою водного навантаження з введенням активних, сильних сечогінних засобів. Повінь організму здійснюємо шляхом рясного пиття хворому або введення в / в різних розчинів (кровезамещающие розчини, глюкоза і т. п.). З сечогінних найбільш часто використовують фуросемід (лазикс) або маніту. Методом форсованого діурезу ми як би "промиваємо" тканини хворого, звільняючи їх від токсичної речовини. Цим способом вдається лише вивести тільки вільні речовини, не пов'язані з білками і ліпідами крові. Слід враховувати електролітний баланс, який при використанні даного методу може бути порушений внаслідок виведення з організму значної кількості іонів.
При гострій серцево-судинній недостатності, тяжких порушеннях функції нирок і небезпеки розвитку набряку мозку та легень форсований діурез протипоказаний.
Крім форсованого діурезу використовують гемодіаліз і перитонеальний діаліз, коли кров (гемодіаліз, або штучна нирка) проходить через напівпроникну мембрану, звільняючись від токсичних речовин, або здійснюється "промивання" порожнини очеревини розчином електролітів.
МЕТОДИ ЕКСТРАКОРПОРАЛЬНОЇ ДЕТОКСИКАЦІЇ. Вдалим методом детоксикації, який отримав широке поширення, є метод гемосорбції (лімфосорбції). В даному випадку токсичні речовини, що знаходяться в крові, адсорбуються на спеціальних сорбентах (гранульований вугілля з покриттям білками крові, аллоселезенка). Цей метод дозволяє успішно проводити детоксикацію організму при отруєннях нейролептиками, транквілізаторами, ФОС і ін. Методом гемосорбції виводяться речовини, погано віддаляються гемодіалізом і перитонеальним діалізом.
Використовують ЗАМІЩЕННЯ КРОВІ, коли поєднують кровопускання з переливанням донорської крові.
3) Третій принцип боротьби з гострим отруєнням полягає в знешкодженні всмоктатися ОТРУТИ шляхом введення АНТАГОНІСТІВ і антидот.
Антагоністи широко використовують при гострих отруєннях. Наприклад, атропін при отруєннях антіхолінестеразнимі засобами, ФОС; налорфин - при отруєнні морфіном та т. д. Зазвичай фармакологічні антагоністи конкурентно взаємодіють з тими ж рецепторами, що і речовини, що викликали отруєння. В цьому плані дуже цікавим виглядає створення СПЕЦИФІЧНИХ АНТИТІЛ (моноклональних) щодо речовин, які особливо часто є причиною гострих отруєнь (моноклональні антитіла проти серцевихглікозидів).
Для специфічного лікування хворих з отруєннями хімічними речовинами ефективна антидотною терапією. Антидот називають засоби, що застосовуються для специфічного зв'язування отрути, нейтра
лізующіе, инактивирующие отрути або за допомогою хімічного або фізичного взаємодії.
Так, при отруєнні важкими металами застосовують з'єднання, які утворюють з ними нетоксичні комплекси (наприклад, унітіол при отруєннях миш'яком, Д-пеніциламін, десфералом при отруєннях препаратами заліза і т. Д.).
4) Четвертий принцип полягає в проведенні СИМПТОМАТИЧНОЮ ТЕРАПІЇ. особливо велике значення симптоматична терапія набуває при отруєннях речовинами, які не мають спеціальних антидотів.
Симптоматичною терапією підтримують життєво важливі функції: кровообіг і ДИХАННЯ. Використовують серцеві глікозиди, вазотонікі, засоби, що поліпшують мікроциркуляцію, оксигенотерапію, стимулятори дихання. Судоми усувають ін'єкціями сибазона. При набряку мозку проводять дегідратаційних терапію (фуросемід, маніт). застосовують анальгетики, проводять корекцію кислотно-лужного стану крові. При зупинці дихання переводять хворого на штучну вентиляцію легких з комплексом реанімаційних заходів.
Далі зупинимося на ДРУГОМУ типі НЕБАЖАНИХ РЕАКЦИЙ, тобто небажані реакції, пов'язаних з фармакологічними властивостями ліків. Побічні ефекти ліків виявляються у 10-20% амбулаторних хворих, а 0, 5-5% хворих потребують госпіталізації для корекції порушень від ЛЗ. Ці небажані, з точки зору патогенезу, реакції можуть бути: а) ПРЯМИМИ і б) пов'язані з зміною чутливості організму хворого.
Розберемо ПРЯМІ ТОКСИЧНІ РЕАКЦІЇ. Вони називаються прямими тому, що ліки прямо, безпосередньо токсично діють на функціональну систему. Наприклад, антибіотики аминогликозидного ряду (стрептоміцин, канаміцин, гентаміцин) виявляють НЕЙРОТОКСИЧНІСТЬ, надаючи токсичний вплив на орган слуху (ототоксичність) і вестибулярний апарат. До того ж даний клас антибіотиків надає токсичність по відношенню до поведінкових реакцій, що проявляються млявістю, апатія, загальмованістю, сонливістю.
Ліки можуть надавати ПРЯМІ ГЕЛАТОТОКСІЧЕСКІЕ РЕАКЦІЇ. Наприклад, фторотан (засіб для наркозу) при повторних застосуваннях в стислі терміни може надавати виражений токсичний ефект аж до гострої жовтої дистрофії печінки.
Прямі токсичні ефекти можуть реалізуватися нефротоксичності. Таким ефектом володіють міціновие антибіотики-аміноглікозиди. При призначенні препаратів цього ряду хворому потрібен постійний контроль за станом аналізів сечі (білок, кров у сечі і т. П.).
Наступний прямий токсичний ефект - ульцерогенной (язвообразующій). Наприклад, призначення саліцилатів, глюкокортикоїдів, антигіпертензивного засобу резерпина - веде до виразки слизової оболонки шлунка, що необхідно враховувати при призначенні зазначених класів засобів, особливо хворим, які вже страждають на виразкову хворобу.
Прямі токсичні ефекти можуть виражатися в ембріотоксичність. Нагадаю, що ембріотоксичним називають несприятливий
дію ліків, не пов'язане з порушенням органогенезу, що виникає до 12 тижнів вагітності. А токсичну дію ліків в більш пізній період вагітності називають фетотоксичні. Необхідно пам'ятати про даний ефект при призначенні лікарських засобів вагітним жінкам, проводячи їм фармакотерапию тільки за суворими показаннями.
Приклади: 1) призначення вагітним стрептоміцину може привести до глухоти у плода (ураження VIII пари черепно-мозкових нервів); 2) тетрациклін негативно впливають на розвиток кісток у плода; 3) у матері, яка страждає морфінізмом, новонароджений також може страждати фізичною залежністю до морфіну.
Лікарські засоби можуть володіти тератогенні, тобто таким, що ушкоджує впливом на диференціювання тканин і клітин, що призводить до народження дітей з різними аномаліями. Наприклад, використання в якості заспокійливого і снодійного кошти талідомід, що володіє вираженим тератогенним ефектом, призвело до народження в країнах Західної Європи декількох тисяч дітей з різними каліцтвами (фокомелия - ластоподобние кінцівки; Амелія - \u200b\u200bВІДСУТНІСТЬ кінцівок; гемангіони особи, аномалії шлунково-кишкового тракту).
Для вивчення тератогенної дії речовин досліджують вплив препаратів на тварин, хоча прямої кореляції про вплив лікарських речовин на тварин і людини немає. Наприклад, у того ж талідоміду тератогенность в експерименті на мишах було виявлено в дозі 250-500 мг / кг маси, а у людини вона виявилася рівною 1-2 мг / кг.
Найбільш небезпечним щодо тератогенної дії вважається перший триместр (особливо період 3-8 тижнів вагітності), тобто період органогенезу. У ці терміни особливо легко викликати важку аномалію розвитку ембріона.
При створенні нових лікарських засобів слід мати також на увазі можливість таких серйозних негативних ефектів, як хімічних мутагенів і канцерогенів. Мутагенні - це здатність речовин викликати стійке пошкодження зародкової клітини, але особливо її генетичного апарату, що проявляється в зміні генотипу потомства. Канцерогенні - це здатність речовин викликати розвиток злоякісних пухлин. Естрагени сприяють розвитку раку молочної залози у жінок в дітородному віці.
Мутагенний і тератогенний ефекти можуть проявитися через місяці і навіть роки, що ускладнює виявлення їх справжньої активності. Тератогенність властива антинеопластичних засобів, кортикостероїдів, андрогенів, алкоголю. Канцерогенну дію мають циклофосфамід, деякі гормональні засоби.
Небажані реакції при використанні лікарських засобів можуть виражатися розвитком ЛЕКАРСТВЕННОЙ ЗАЛЕЖНО або якщо більш глобально - НАРКОМАНІЄЮ. Існує кілька основних ознак наркоманії.
1) Це наявність психічної ЗАЛЕЖНО, тобто такого стану, коли у хворого розвивається непереборне психічний потяг до повторного введення лікарського речовини, наприклад,
наркотику.
2) Фізична ЗАЛЕЖНІСТЬ - цим терміном позначають наявність у хворого найсильнішого фізичного нездужання без повторної ін'єкції лікарського речовини, зокрема наркотику. При різкому припиненні введення препарату, що викликав лікарську залежність, розвивається явище ПОЗБАВЛЕННЯ або абстиненції. З'являються страх, тривога, туга, безсоння. Можливо рухове занепокоєння, виникає агресивність. Порушуються багато фізіологічні функції. У важких випадках абстиненція може бути причиною смертельного результату.
3) Розвиток ТОЛЕРАНТНОСТІ, тобто звикання. іншими виду
ми небажаних ефектів, обумовлених властивостями самих ліків, є порушення, пов'язані зі зрушеннями в імунобіологічної системі хворого при прийомі високоактивних лікарських засобів. Наприклад, використання антибіотиків широкого спектру дії може проявитися зміною нормальної бактеріальної флори організму (кишечника), що реалізовується розвитком суперинфекции, дисбактеріозом, кандидозом. Найчастіше в зазначені процеси залучаються легені і кишечник.
Кортікостероідотерапія і імуносупресивної терапії послаблюють імунітет, в результаті чого підвищується ризик розвитку інфекційних захворювань, Перш за все, опортуністичної природи (пневмоцистоз, цитомегаловірус і т. П.).
Ця підгрупа реакцій буває 2-х видів:
1) АЛЕРГІЧНІ РЕАКЦІЇ;
2) ідіосинкразія. Слід сказати, що негативні впливав
ня, пов'язані з
тичними реакціями, зустрічаються дуже часто в медичній практиці. Їх частота весь час збільшується. Виникають вони незалежно від дози введеного лікарського засобу, а в їх формуванні беруть участь імунні механізми. Алергічні реакції можуть бути 2-х видів: ГІПЕРЧУТЛИВІСТЬ НЕГАЙНОГО ТИПУ, ГНТ - связанноя з утворенням антитіл класів IgE і IgG4) і УПОВІЛЬНЕНОЇ (накопичення сенсибілізованих T-лімфоцитів і макрофагів) типів.
Клінічна картина дуже різноманітна: кропив'янка, шкірні висипи, ангіоневротичний набряк, сироваткова хвороба, бронхіальна астма, лихоманка, гепатит і т. Д. Але головне - можливість розвитку анафілактичного шоку. Якщо для розвитку алергічних реакцій потрібно як мінімум дворазовий контакт хворого з лікарською речовиною, то розвиток ідіосинкразії - непереносимості лікарських речовин при первинному контакті з ксенобіотиком, завжди пов'язане з будь-яким генетичним дефектом, як правило виражається відсутністю або вкрай низькою активністю ферменту. Наприклад, використання противомалярийного препарату примахина у осіб з генетичною ензимопатіях (недостатність акт. Г-6-ФДГ) викликає утворення хинона, який володіє гемолітичним дією. При наявності даної ферментопатии небезпечно призначення ЛЗ, що є окислювачами, так як це може призводити до гемолізу
еритроцитів, до лікарської гемолітичної анемії (аспірин, левоміцетин, хінідин, примахин, фурадонін).
КІЛЬКА СЛІВ ПРО СТВОРЕННЯ НОВИХ ЛІКАРСЬКИХ ЗАСОБІВ, ОЦІНКИ ЛІКІВ ТА ЇХ номенклатури. Прогрес фармакології характеризується безперервним пошуком і створенням нових препаратів. Створення ліків починається з досліджень хіміків і фармакологів, творча співпраця яких абсолютно необхідно при відкритті нових препаратів. При цьому пошук нових засобів розвивається за кількома напрямками.
Основним шляхом є ХІМІЧНИЙ синтез препаратів, який може реалізуватися у вигляді спрямованого синтезу або мати емпіричного шлях. Якщо спрямований синтез пов'язаний з відтворенням біогенних речовин (інсулін, адреналін, норадреналін), створенням антиметаболітів (ПАБК-сульфаніламіди), модифікацією молекул сполук з відомою біологічною активністю (зміна структури ацетилхоліну - гонгліоблекатор гігроній) і т. Д., То емпіричний шлях полягає або з випадкових знахідок, або пошуку шляхом скринінгу, тобто просіювання різних хімічних сполук на фармакологічну активність.
Одним із прикладів емпіричних знахідок може бути наведений випадок обрануженія гіпоглікемічного ефекту при використанні сульфаніламідів, що згодом призвело до створення сульфаніламідних синтетичних перфоральних протидіабетичнихзасобів (бутамид, хлорпропамид).
Досить трудомісткий і інший варіант емпіричного шляху створення ліків - МЕТОД СКРИНІНГУ. Однак він неминучий, особливо якщо досліджується новий клас хімічних сполук, властивості яких, виходячи з їх структури, важко прогнозувати (малоефективний шлях). І тут величезну роль в даний час грає комп'ютеризація наукового пошуку.
В даний час лікарські засоби отримують головним чином за допомогою спрямованого хімічного синтезу, який може здійснюватися а) шляхом подібності (введення додаткових ланцюжків, радикалів) б) шляхом комплементарності, тобто відповідності будь-яким рецепторів тканин і органів.
В арсеналі лікарських засобів, крім синтетичних препаратів, значне місце займають препарати та індивідуальні речовини з ЛІКАРСЬКОГО СИРОВИНИ рослинного або тваринного походження, а також з різних мінералів. Це перш за все галенові, новогаленові препарати, алкалоїди, глікозиди. Так з опію отримують морфін, кодеїн, папаверин, з рауфльфіі змієподібній - резерпін, з наперстянки - серцеві глікозиди - дигітоксин, дигоксин; з ряду ендокринних залоз великої рогатої худоби - гормони, імуноактивний препарати (інсулін, тиреоидин, тактовно і т. д.).
Деякі лікарські засоби є продуктами життєдіяльності грибів і мікроорганізмів. Приклад - антибіотики. Лікарські речовини рослинного, тваринного, мікробного, грибкового походження часто служать основою для їх синтезу, а також подальших хімічних перетворень і отримання напівсинтетичних і синтетичних препаратів.
Набирають темпи створення лікарських засобів шляхом викорис
тання методів генної інженерії (інсулін і т. п.).
Новий лікарський засіб, пройшовши через усі ці "сита" (дослідження фармактівності, фармакодинаміки, фармакокінетики, вивчення побічних ефектів, токсичності і т. Д.) Допускається на клінічні випробування. Тут використовується метод "сліпого контролю", ефект плацебо, метод подвійного «сліпого контролю", коли ні лікар, ні хворий не знає, коли це плацебо використовується. Знає тільки спеціальна комісія. Клінічні випробування проводяться на людях, і в багатьох країнах це здійснюється на добровольцях. Тут, безумовно, виникає маса юридичних, деонтологічних, етичних аспектів проблеми, які вимагають свого чіткої розробки, регламентації і затвердження законів на даний рахунок.
НОМЕНКЛАТУРА ЛІКАРСЬКИХ ЗАСОБІВ
Багато лікарські засоби, що складаються з одного активної речовини, можуть бути названі по їх хімічною будовою. Але в зв'язку з великою складністю їх запам'ятовування і незручністю застосування хімічні назви в медичній практиці не використовуються.
В даний час для позначення лікарських засобів використовують 2 види назв:
1) непатентованих міжнародні, які затверджуються офіційними органами охорони здоров'я і використовуються в національних і міжнародних фармакопеях;
2) КОМЕРЦІЙНІ, або фірмові назви, що є комерційною власністю фармфірм. При цьому один і той же препарат може мати безліч назв. Транквілізатор діазенам має фірмові назви "седуксен", "сибазон", "реланиум" і т. Д. Деякі ЛЗ мають понад 100 найменувань (наприклад, вітамін В12). Зазвичай на упаковці лікарського препарату є як фірмове, так і міжнародна непатентована назва.
Кращим є виписування ліків під їх непатентованими назвами, що знижує можливість лікарських помилок. Такі препарати дешевше, ніж медикаменти з фірмовою назвою. Крім того, виписування ліків під їх непатентованими назвою дає можливість аптеці надати хворому препарат будь-якої фірми, що виробляє дані ліки.
Для клініцистів найбільш зручною класифікацією ліків є та, що будується по нозологічних ПРИНЦИПОМ (наприклад, кошти для лікування бронхіальної астми, інфаркту міокарда, антидіабетичні препарати і т. П.). але кращі класифікації враховують такі ознаки препаратів, як локалізація дії, фармакологічна дія, терапевтичне застосування. Однією з таких класифікацій, які є найбільш досконалою, є класифікація академіка М. Д. Машковська, згідно з якою викладено і його відомий довідник.
1. Поняття про лікування як спрямованої корекції фізіологічних порушень в організмі. Користь і ризик при використанні ліків. Підстави для їх застосування. Оцінка безпеки.
фармакологія - теоретична основа фармакотерапії.
Підстави для застосування ліків:
1) для корекції і усунення причини захворювання
2) при недостатності профілактичних засобів
3) за життєвими показаннями
4) очевидна необхідність, заснована на рівні знань і досвіді
5) прагнення до підвищення якості життя
Користь при призначенні ліків:
1) корекція або усунення причини захворювання
2) полегшення симптомів захворювання при неможливості його лікування
3) заміщення лікарськими речовинами природних БАР, які не виробляються організмів в достатній кількості
4) здійснення профілактики захворювань (вакцини і ін.)
ризик - ймовірність того, що результатом впливу буде шкода чи збитки; дорівнює відношенню числа несприятливих (аверсівних) подій до чисельності групи ризику.
А) неприйнятний (шкода\u003e користі)
Б) прийнятний (користь\u003e шкоди)
В) незначний (105 - рівень безпеки)
Г) усвідомлений
Оцінка безпеки ЛЗ починається на рівні хімічних лабораторій, Що синтезують ЛЗ. Доклінічну оцінку безпеки ЛЗ проводить МОЗ, FDA і т. Д. Якщо ЛЗ успішно проходить даний етап, Починається його клінічна оцінка, що складається з чотирьох фаз: I фаза - оцінка переносимості на здорових добровольцях 20-25 років, II фаза - на хворих добровольцях чисельністю менше 100 чоловік, які страждають певним захворюванням, III фаза - мультицентрові клінічні дослідження на великих групах людей ( до 1000 осіб), IV фаза - моніторинг препарату протягом 5 років після його офіційного дозволу. Якщо ЛЗ успішно проходить всі ці фази, воно вважається безпечним.
2. Сутність фармакології як науки. Розділи і області сучасної фармакології. Основні терміни і поняття фармакології - фармакологічна активність, дія, ефективність хімічних речовин.
фармакологія - наука про ліки у всіх аспектах - теоретична основа терапії:
А) наука про взаємодію хімічних речовин з живими системами
Б) наука про управління процесами життєдіяльності організму за допомогою хімічних речовин.
Розділи сучасної фармакології:
1) Фармакодинаміка - вивчає а) вплив ЛЗ на організм людини, б) взаємодія різних ЛЗ в організмі при одночасному їх призначенні, в) вплив віку і різних захворювань на дію ЛЗ
2) Фармакокінетика - вивчає всмоктування, розподіл, метаболізм та екскрецію ЛЗ (т. Е. Як організм хворого реагує на ЛЗ)
3) фармакогенетика- вивчає роль генетичних факторів у формуванні фармакологічного відповіді організму на ЛЗ
4) Фармакоекономіка- оцінює результати використання і вартість ЛЗ для прийняття рішення про подальше їх практичному застосуванні
5) фармакоепідеміологія - вивчає застосування ЛЗ та їх ефекти на рівні популяцій або великих груп людей для забезпечення застосування найбільш ефективних і безпечних лікарських засобів
Фармакологічна (біологічна) активність - властивість речовини викликати зміни в биосистеме (організмі людини). Фармакологічні речовини \u003d біологічно активні речовини (БАР)
Фармакологічна дія - вплив ЛЗ на об'єкт і його мішені
фармакологічний ефект - результат дії речовини в організмі (модифікація фізіологічних, біохімічних процесів, морфологічних структур) - кількісне, але не якісна зміна в стані біосистем (клітин, тканин, органів).
ефективність ЛЗ - здатність ЛЗ викликати певні необхідні в даному випадку фармакологічні ефекти в організмі. Оцінюється на основі «істотних доказів» - адекватних добре контрольованих досліджень і клінічних випробувань, проведених експертами з відповідною науковою підготовкою та досвідом в дослідженні ліків даного типу (FDA)
3. Хімічна природа ліків. Фактори, що забезпечують терапевтичний ефект лікарських засобів - фармакологічна дія і плацебо-ефекти.
ЛЗ бувають 1) рослинного 2) тваринного 3) мікробного 4) мінерального 5) синтетичного
Синтетичні ЛЗ представлені практично всіма класами хімічних сполук.
Фармакологічна дія - вплив ЛЗ на об'єкт і його мішені.
плацебо - будь-який компонент терапії, що не виявляє ніякого специфічного біологічного впливу на хворобу, яка є об'єктом лікування.
Застосовується з метою контролю при оцінці дії ЛЗ та для того, щоб принести користь хворому без будь-яких фармакологічних засобів в результаті тільки психологічного впливу (т. Е. Плацебо-ефекту).
Всі види лікування мають психологічний компонент, або доставляє задоволення ( Плацебо-ефект), Або викликає занепокоєння ( Ноцебо-ефект). Приклад плацебо-ефекту: швидке поліпшення у хворого вірусною інфекцією при застосуванні антибіотиків, які не впливають на віруси.
Сприятливість плацебо-ефекту пов'язана з психологічним впливом на пацієнта. Він буде максимальним лише при його використанні У поєднанні з методами лікування, Що мають виражений специфічний ефект. дорогі речовини в якості плацебо також сприяють досягненню більшої відповіді.
Показання до застосування плацебо:
1) слабкі психічні порушення
2) психологічна підтримка пацієнта з невиліковною хронічною хворобою або з підозрою на важкий діагноз
4. Джерела і етапи створення ліків. Визначення понять лікарська речовина, лікарський засіб, лікарський препарат і лікарська форма. Назва ліків.
Джерела створення ЛЗ:
А) натуральна сировина: рослини, тварини, мінерали і т. Д. (Серцеві глікозиди, свинячий інсулін)
Б) модифіковані природні БАР
В) синтетичні сполуки
Г) продукти генної інженерії (рекомбінантний інсулін, інтерферони)
Етапи створення ЛЗ:
1. Синтез ЛЗ в хімічній лабораторії
2. Доклінічна оцінка активності та небажаних ефектів ЛЗ МОЗ та ін. Організмаціямі
3. Клінічні випробування ЛЗ (докладніше див. Ст. 1)
Лікарський засіб - будь-яка речовина або продукт, що використовуються, щоб модифікувати або досліджувати фізіологічні системи або патологічні стани для блага реципієнта (по ВООЗ, 1966 г.); індивідуальні речовини, суміші речовин або композиції невідомого складу, які мають доказані лікувальними властивостями.
лікарська речовина - індивідуальна хімічна сполука, що використовується в якості лікарського засобу.
Лікарська форма - зручна для практичного застосування форма, що надається лікарського засобу для отримання необхідного лікувального або профілактичного ефекту.
Лікарський засіб - лікарський засіб в певній лікарській формі, дозволене органом державного управління.
5. Шляхи введення ліків в організм і їх характеристика. Пресистемна елімінація ліків.
1. Для системної дії
А. Ентеральний шлях введення: Перорально, сублінгвально, трансбуккально, ректально, через зонд
Б. Парентеральний шлях введення: Внутрішньовенно, підшкірно, внутрішньом'язово, інгаляційно, субарахноїдальний, трансдермально
2. Для місцевого впливу: накожно (епікутарно), на слизові, в порожнині (черевну, плевральну, суглобову), в тканини (інфільтрація)
|
Шлях введення ЛЗ |
переваги |
недоліки |
|
Перорально - через рот |
1. Зручний і простий для пацієнта 2. Не потрібно стерильності препаратів |
1. Абсорбція багатьох ЛЗ залежить від прийому їжі, функціонального стану шлунково-кишкового тракту та ін. Чинників, насилу враховуються на практиці 2. Не всі ЛЗ добре всмоктуються в шлунково-кишковому тракті 3. Деякі ЛЗ руйнуються в шлунку (інсулін, пеніцилін) 4. Частина ЛС надає НЛР на слизову шлунково-кишкового тракту (НПЗЗ - виявлення слизової, антациди - пригнічують моторику) 5. Не можна застосовувати у пацієнтів в несвідомому стані і при порушенні ковтанні |
|
Сублінгвально і трансбуккально |
1. Зручне і швидке введення 2. Швидке всмоктування ЛЗ 3. ЛЗ не береться пресистемної елімінації 4. Дія препарату можна швидко перервати |
1. Незручність, створюване частим регулярним використанням таблеток 2. Роздратування слизової рота, надлишкове виділення слини, що сприяє заковтування ЛЗ і зменшення його ефективності 3. Неприємний смак |
|
ректально |
1. Половина ЛВ не береться пресистемному метаболізму 2. Не дратується слизова шлунково-кишкового тракту 3. Зручно, коли інші шляхи введення неприйнятні (блювота, морська хвороба, Немовлята) 4. Місцева дія |
1. Неприємні для пацієнта психологічні моменти 2. Всмоктування ЛЗ значно сповільнюється при неопорожненіе прямій кишці. |
|
Внутрішньосудинно (зазвичай внутрішньовенно |
1. швидке надходження в кров (невідкладні стани) 2. Швидке створення високої системної концентрації і можливість нею управляти 3. Дозволяє вводити ЛЗ, що руйнуються в шлунково-кишковому тракті |
1. Технічні складності внутрішньосудинного доступу 2. Ризик розвитку інфекції у місці ін'єкції 3. Тромбози вен в місці введення ЛЗ (еритроміцин) і больові відчуття (Калію хлорид) 4. Деякі ЛЗ адсорбуються на стінках крапельниць (інсулін) |
|
внутрішньом'язово |
Досить швидке всмоктування препарату в кров (10-30 хв) |
Ризик місцевих ускладнень |
|
підшкірно |
1. Хворий може робити ін'єкції самостійно після навчання 2. Тривалий ефект ЛЗ |
1. Повільне всмоктування і прояв ефекту ЛЗ 2. Атрофія жирової тканини в місці введення і зменшення швидкості всмоктування ЛЗ |
|
інгаляційно |
1. швидкий початок дії і висока концентрація в місці введення при лікуванні захворювань дих. шляхів 2. Хороша контрольованість дії 3. Зменшення токсичних системних ефектів |
1. Необхідність спеціального пристрою (інгалятора) 2. Складність використання аерозолів під тиском для деяких хворих |
|
місцевий ЛЗ |
1. Висока діюча концентрація ЛЗ в місці введення 2. Уникайте небажані системні ефекти даного ЛЗ |
При порушенні цілісності шкірних покривів препарат може потрапити в системний кровотік - прояв небажаних системних ефектів. |
Пресистемна елімінація ЛЗ (ефект першого проходження) - процес біотрансформації ліків до потрапляння ЛЗ в системний кровотік. У пресистемної елімінації при пероральному введенні ліків беруть участь ферментативні системи кишечника, крові ворітної вени і гепатоцити.
При внутрішньовенному введенні пресистемній елімінації відсутня.
Для того, щоб перорально приймається ЛЗ зробило корисну дію, Потрібно збільшити його дозу для компенсації втрат.
6. Перенесення ліків через біологічні бар'єри і його різновиди. Основні фактори, що впливають на перенесення ліків в організмі.
Способи абсорбції (транспорту) ЛЗ через біологічні мембрани:
1) Фільтрація (водна дифузія) - пасивне переміщення молекул речовини за градієнтом концентрації через заповнені водою пори в мембрані кожної клітини і між сусідніми клітинами, характерний для води, деяких іонів, дрібних гідрофільних молекул (сечовина).
2) Пасивна дифузія (ліпідна дифузія) - основний механізм перенесення ЛВ, процес розчинення ліки в ліпідах мембрани і рух через них.
3) Транспорт за допомогою специфічних переносників - перенесення ЛВ за допомогою вбудованих в мембрану переносників (частіше білків), характерний для гідрофільних полярних молекул, ряду неорганічних іонів, цукрів, амінокислот, піримідинів:
а) полегшена дифузія - здійснюється за градієнтом концентрації без витрати АТФ
б) активний транспорт - проти градієнта концентрації з витратами АТФ
Насичується процес - т. Е. Швидкість абсорбції збільшується лише до тих пір, поки кількість молекул лікарського речовини не зрівняється з кількістю переносників.
4) Ендоцитоз і пиноцитоз - ліки зв'язується зі спеціальним розпізнає компонентом мембрани клітини, виникає інвагінація мембрани і формується пухирець, що містить молекули ліки. Згодом ліки виділяється із пляшечки в клітку або транспортується з клітки. Характерний для високомолекулярних поліпептидів.
Фактори, що впливають на перенесення ліків в організмі:
1) фізико-хімічні властивості речовини (гідро- і липофильность, іонізація, поляризованість, розмір молекул, концентрація)
2) структура бар'єрів перенесення
3) кровотік
7. Перенесення через мембрани лікарських речовин із змінною іонізацією (рівняння іонізації Гендерсона-Гассельбальха). Принципи управління перенесенням.
Всі ЛЗ - слабкі кислоти або слабкі підстави, що мають свої значення константи іонізації (рК). Якщо значення рН середовища дорівнює значенню рК ліки, то 50% його молекул буде знаходиться в іонізованому і 50% в неіонізованому стані і середовище для ліків буде нейтральною.
У кислому середовищі (рН менше рК), там де є надлишок протонів, слабка кислота буде перебувати в недиссоциированной формі (R-COOH), т. Е. Буде пов'язана з протоном - протоновану. Така форма кислоти незаряжена і добре розчинна в ліпідах. Якщо рН зміститися в лужну сторону (т. Е. РН побільшає рК), то кислота почне диссоциировать і позбудеться протона, перейшовши при цьому в непротонірованную форму, яка має заряд і погано розчинна у ліпідах.
У лужному середовищі, там де є дефіцит протонів, слабка основа буде перебувати в недиссоциированной формі (R-NH2), т. Е. Буде непротоніровано і позбавлене заряду. Така форма підстави добре розчинна в ліпідах і швидко абсорбується. У кислому середовищі є надлишок протонів і слабка основа почне диссоциировать, пов'язуючи при цьому протони і утворюючи протоновану, заряджену форму підстави. Така форма погано розчинна у ліпідах і слабо абсорбується.
отже, Абсорбція слабких кислот протікає переважно в кислому середовищі, а слабких основ - в лужному.
Особливості метаболізму слабких кислот (СК):
1) шлунок: СК в кислому середовищі шлунка неіонізовану, а в лужному середовищі тонкого кишечника вона буде діссоціацііровать і молекули СК придбають заряд. Тому, абсорбція слабких кислот буде найбільш інтенсивної в шлунку.
2) в крові середовище досить лужне і всосавшиеся молекули СК перейдуть в іонізовану форму. Фільтр клубочків нирок пропускає як іонізовані, так і неіонізовані молекули, тому, незважаючи на заряд молекули, СК будуть виводитися в первинну сечу
3) якщо сеча лужна, то кислота залишиться в іонізованій формі, не зможе реабсорбироваться назад в кровотік і виділиться з сечею; сечі кисла, то ліки перейде в неіонізовану форму, яка легко реабсорбується назад в кров.
Особливості метаболізму слабких основ: Протилежно СК (абсорбція краще в кишечнику; в лужній сечі піддаються реабсорбції)
Т. о., Щоб прискорити виведення з організму слабкої кислоти сечу необхідно ощелачивать, а щоб прискорити виведення слабкої основи її необхідно підкислити (Детоксикація по Попову).
Кількісну залежність процесу іонізації ліки при різному рН середовища дозволяє отримати рівняння Henderson— Hasselbach:
Де pKa відповідає значенню pH, при якому концентрації іонізованої і неионизированной форм знаходяться в рівновазі .
Рівняння Гендерсона-Гассельбаха дозволяє оцінити ступінь іонізації ЛЗ при даному значенні рН і передбачити ймовірність його проникнення через клітинну мембрану.
(1) Для розведеної кислоти, A,
HA ↔ H + + A -, де HA - концентрація неионизированной (протоновану) форми кислоти і A - - концентрація іонізованої (непротонірованной) форми.
(2) Для слабкої основи, B,
BH + ↔ H + + B, де BH + - концентрація протоновану форми підстави, B - концентрація непротонірованной форми
Знаючи рН середовища і рКа речовини, можна по обчисленому логарифму визначити ступінь іонізації ліки, а значить, і ступінь його всмоктування з шлунково-кишкового тракту, реабсорбції або екскреції нирками при різних значеннях рН сечі і т. Д.
8. Перенесення ліків в організмі. Водна дифузія і дифузія в ліпідах (закон Фіка). Активний транспорт.
Перенесення ЛЗ в організмі може здійснюватися водної та ліпідної дифузією, активним транспортом, ендо- - і піноцитозом.
Особливості перенесення ЛЗ в організмі водної дифузією:
1. Епітеліальні покриви (слизові ШКТ, порожнини рота і ін.) - водна дифузія тільки дуже малих молекул (метанол, іони літію і т. Д.)
2. Капіляри (крім мозкових) - фільтрація речовин з молекулярною масою до 20-30 тис. Так.
3. Капіляри мозку - в основному не мають водних пір, за винятком областей гіпофіза, епіфіза, зони IV шлуночка, хоріоїдного сплетення, медіанного піднесення
4. Плацента - не має водних пір (хоча питання спірне).
5. Зв'язування ЛЗ з білками крові перешкоджає їх виходу з кров'яного русла, а значить, і водної дифузії
6. Дифузія в воді залежить від розмірів молекул ЛЗ і водних пір
Особливості ліпідного дифузії:
1. Основний механізм перенесення ЛЗ через клітинні мембрани
2. Визначається липофильностью діффундіруемие речовини (т. Е. Коефіцієнтом розподілу «масло / вода») і градієнтом концентрації, може бути обмежена дуже низьку розчинність речовини у воді (що перешкоджає проникненню ЛЗ в водну фазу мембран)
3. Легко дифундують неполярні сполуки, важко - іони.
Будь-яка дифузія (і водна, і в ліпідах) підкоряється закону дифузії Фіка:
Швидкість дифузії - кількість переносите в одиницю часу молекул ліки; С1 - концентрація речовини зовні мембрани; С2 - концентрація речовини зсередини мембрани.
Слідство із закону Фіка:
1) фільтрація ЛЗ тим вище, чим більше його концентрація в місці введення (S абсорбіруємой поверхні в кишечнику більше, ніж в шлунку, тому абсорбція ЛЗ в кишечнику швидша)
2) фільтрація ЛЗ тим вище, чим більше концентрація ЛЗ в місці введення
3) фільтрація ЛЗ тим вище, чим менше товщина подоланої біологічної мембрани (товщина бар'єру в альвеолах легенів значно менше, ніж шкіри, тому швидкість абсорбції вище в легких)
активний транспорт - перенесення ЛC незалежно від градієнта концентрації з використанням енергії АТФ, характерний для гідрофільних полярних молекул, ряду неорганічних іонів, цукрів, амінокислот, піримідинів. характеризується: а) вибірковістю до певних сполук б) можливістю конкуренції двох речовин за один транспортний механізм в) насичуваність при високих концентраціях речовини г) можливістю транспорту проти градієнта концентрації д) витратою енергії.
9. Центральний постулат фармакокінетики концентрація ліків в крові - основний параметр для управління терапевтичним ефектом. Завдання, які вирішуються на підставі знання цього постулату.
Центральний постулат (догма) фармакокінетики: концентрація ЛВ в плазмі крові детермінує (кількісно визначає) фармакологічний ефект.
У більшості випадків швидкість всмоктування, розподілу, метаболізму та екскреції ЛЗ пропорційна їх концентрації в плазмі крові (підпорядковується закону діючих мас), тому знаючи її можливо:
1) визначити період полуелімінаціі (для ЛЗ з кінетикою першого порядку)
2) пояснити тривалість деяких токсичних ефектів ЛЗ (для ЛЗ у високих дозах з кінетикою насичення)
10. Біодоступність ліків - визначення, сутність, кількісне вираження, детермінанти. Поняття про біодоступність
Біодоступність (F) - характеризує повноту і швидкість всмоктування ЛЗ при позасистемних шляхах введення - відображає кількість незміненої речовини, яка досягла системного кровотоку, щодо вихідної дози препарату.
F становить 100% для ЛЗ, які вводять внутрішньовенно. При введенні іншими шляхами F зазвичай менше через неповну абсорбції і часткового метаболізму в периферичних тканинах. F дорівнює 0, якщо ЛЗ не всмоктується з просвіту шлунково-кишкового тракту.
Для оцінки F будують криву залежності концентрації ЛЗ в крові від часу після його введення внутрішньовенно, а також після введення досліджуваним шляхом. Це т. Зв. фармакокінетичні криві залежності «час-концентрація». Шляхом інтегрування знаходять значення площі під фармакокінетичною кривою і розраховують F як відношення:
![]() ≤ 1, де AUC - площа під фармакокінетичною кривою (Area Under Curve)
≤ 1, де AUC - площа під фармакокінетичною кривою (Area Under Curve)
Біодоступність\u003e 70% вважається високою, нижче 30% - низькою.
Детермінанти біодоступності:
1) швидкість всмоктування
2) повнота всмоктування - недостатня абсорбція ЛЗ внаслідок його дуже високою гидрофильности або ліпофільності, метаболізму бактеріями кишечника при ентеральному введенні і т. Д.
3) пресистемній елімінації - при високій биотрансформация в печінці F ЛЗ низька (нітрогліцерин при пероральному введенні).
4) лікарська форма - сублінгвальниє таблетки і ректальні супозиторії допомагають ЛЗ уникнути пресистемної елімінації.
11. Розподіл ліків в організмі. Відсіки, ліганди. Основні детермінанти розподілу.
розподіл ЛЗ - процес поширення ЛЗ по органам і тканинам після того, як вони надійдуть в системний кровотік.
Відсіки розподілу:
1. Позаклітинне простір (плазма, міжклітинна рідина)
2. Клітини (цитоплазма, мембрана органел)
3. Жирова і кісткова тканина (депонування ЛЗ)
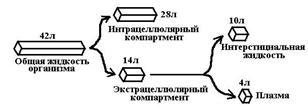 У людини масою 70 кг обсяги рідких середовищ становлять в цілому 42 л, тоді якщо:
У людини масою 70 кг обсяги рідких середовищ становлять в цілому 42 л, тоді якщо:
[Vd \u003d 3-4 л, то все ліки розподілено в крові;
[Vd \u003d 4-14 л, то все ліки розподілено в позаклітинній рідині;
[Vd \u003d 14-42 л, то все ліки приблизно рівномірно розподілено в організмі;
[Vd\u003e 42 л, то все ліки знаходиться переважно в позаклітинному просторі.
Молекулярні ліганди ЛЗ:
А) специфічні і неспецифічні рецептори
Б) білки крові (альбумін, глікопротеїн) і тканин
В) полісахариди сполучної тканини
Г) нуклеопротеїни (ДНК, РНК)
Детермінанти розподілу:
· природа ЛЗ - ніж менше розміри молекули і ліпофільних ЛЗ, тим швидше і рівномірніше його розподіл.
· Розмір органів - ніж більше розмір органу, тим більше лікарського засобу може надійти в нього без істотної зміни градієнтаконцентрацій
· Кровотік в органі - в добре перфузіруемих тканинах (мозок, серце, нирки) терапевтична концентрація речовини створюється значно раніше, ніж в тканинах погано перфузіруемих (жирова, кісткова)
· Наявність гистогематических бар'єрів- ЛЗ легко проникають в тканини з погано вираженим ГГБ
· Зв'язування ліків з білками плазми - чим більше пов'язана фракція ЛЗ, тим гірше його розподіл в тканини, т. К. Залишати капіляр можуть лише вільні молекули.
· Депонування ліки в тканинах - зв'язування ЛЗ з білками тканин сприяє його накопиченню в них, т. К. Знижується концентрація вільного ЛЗ в периваскулярном просторі і постійно підтримується високий градієнт концентрацій між кров'ю і тканинами.
Кількісною характеристикою розподілу ліки є уявний об'єм розподілу (Vd).
Уявний об'єм розподілуVd - це гіпотетичний об'єм рідини, в якому може розподілитися вся введена доза ліків, щоб створилася концентрація, що дорівнює концентрації в плазмі крові.
Vd дорівнює відношенню введеної дози (загальної кількості ліків в організмі) до його концентрації в плазмі крові:
 .
.
Чим більше уявний об'єм розподілу, тим більша частина ліків розподіляється в тканини.
12. Константа елімінації, її сутність, розмірність, зв'язок з іншими фармакокинетическими параметрами.
Константа швидкості елімінації (Kel, хв-1) - показує, яка частина ЛЗ елімінується з організму в одиницю часу Þ Kel \u003d Aвид / Азаг, де Авид - кількість ЛС, що виділяється в од. часу, Азаг - загальна кількість ЛЗ в організмі.
Значення kel зазвичай знаходять шляхом вирішення фармакокинетического рівняння, що описує процес елімінації ліки з крові, тому kel називають модельним показником кінетики. Безпосереднього відношення до планування режиму дозування kel не має, але її значення використовують для розрахунку інших фармакокінетичних параметрів.
Константа елімінації прямо пропорційна кліренсу і обернено пропорційно обсягу розподілу (з визначення кліренсу): Kel \u003d CL / Vd; \u003d Годину-1 / хв-1 \u003d частка в годину.
13. Період напіввиведення ліків, його сутність, розмірність, взаємозв'язок з іншими фармакокинетическими параметрами.
період полуелімінаціі (T½, хв) - це час, необхідний для зниження концентрації ЛЗ в крові рівно наполовину. При цьому не грає ролі яким шляхом досягається зниження концентрації - за допомогою біотрансформації, екскреції або ж за рахунок поєднання обох процесів.
Період полуелімінаціі визначають за формулою:
![]()
Період напіввиведення - найважливіший фармакокинетический параметр, що дозволяє:
Б) визначити час повної елімінації препарату
В) передбачити концентрацію ЛЗ в будь-який момент часу (для ЛЗ з кінетикою першого порядку)
14. Кліренс як головний параметр фармакокінетики для управління режимом дозування. Його сутність, розмірність і зв'язок з іншими фармакокинетическими показниками.
кліренс (Cl, мл / хв) - обсяг крові, який очищається від ЛЗ за одиницю часу.
Т. к. Плазма (кров) - «видима» частина обсягу розподілу, то кліренс - фракція обсягу розподілу, з якої ліки виділяється в одиницю часу. Якщо позначити загальна кількість ліки в організмі через Азаг, А кількість, яка виділилася через Авид, То:
![]() З іншого боку, з визначення обсягу розподілу випливає, що загальна кількість ліки в організмі становить Азаг \u003dVd´
CТер / плазма. Підставляючи це значення в формулу кліренсу, ми отримаємо:
З іншого боку, з визначення обсягу розподілу випливає, що загальна кількість ліки в організмі становить Азаг \u003dVd´
CТер / плазма. Підставляючи це значення в формулу кліренсу, ми отримаємо:
![]() .
.
Таким чином, кліренс - відношення швидкості виведення лікарського засобу до його концентрації в плазмі крові.
У такому вигляді формулу кліренсу використовують для розрахунку підтримуючої дози ліків ( DП), Т. Е тієї дози лікарського засобу, яка повинна компенсувати втрату ліки і підтримати його рівень на постійному рівні:
Швидкість введення \u003d швидкість виведення \u003dCl´ CТер (Доза / хв)
DП \u003d Швидкість введення´ T (T - інтервал, між прийомом ліків)
кліренс аддитивен, Т. Е. Елімінація речовини з організму може відбуватися за участю процесів, що йдуть в нирках, легенях, печінці та інших органах: Clсістемний \u003d Clпочечн. + Clпечені + Clдр.
кліренс пов'язаний З періодом полуелімінаціі ЛЗ і обсягом розподілу: T1 / 2 \u003d 0,7 * Vd / Cl.
15. Доза. Види доз. Одиниці дозування лікарських засобів. Цілі дозування ліків, способи і варіанти введення, інтервал введення.
Дія ЛС на організм більшою мірою визначається їх дозою.
доза - кількість речовини, введене в організм за один прийом; виражається у вагових, об'ємних або умовних (біологічних) одиницях.
Види доз:
А) разова доза - кількість речовини на один прийом
Б) добова доза - кількість препарату, яка призначається на добу в один або декілька прийомів
В) курсова доза - загальна кількість препарату на курс лікування
Г) терапевтичні дози - дози, в яких препарат використовують з лікувальними або профілактичними цілями (порогові, або мінімальні діючі, середні терапевтичні і вищі терапевтичні дози).
Д) токсичні і смертельні дози - дози ЛВ, при яких вони починають надавати виражені токсичні ефекти або викликати смерть організму.
Е) завантажувальна (вступна) доза - кількість введеного ЛЗ, яке заповнює весь обсяг розподілу організму в чинній (терапевтичної) концентрації: ВД \u003d (Css * Vd) / F
Ж) підтримуюча доза - систематично вводиться кількість ЛЗ, яке компенсує втрати ЛЗ з кліренсом: ПД \u003d (Css * Cl * DT) / F
Одиниці дозування ЛЗ:
1) в грамах або частках грама ЛЗ
2) кількість ЛЗ в розрахунку на 1 кг маси тіла (наприклад, 1 Мг / кг) Або на одиницю поверхні тіла (наприклад, 1 Мг / м2)
Цілі дозування ЛЗ:
1) визначити кількість ЛЗ, необхідне для того, щоб викликати потрібний терапевтичний ефект з певною тривалістю
2) уникнути явищ інтоксикації і побічних ефектів при введенні ЛЗ
Способи введення ЛЗ: 1) ентерально 2) парентеральний (див. Ст. 5)
Варіанти введення ЛЗ:
А) безперервний (шляхом тривалих внутрішньосудинних інфузій ЛЗ крапельно або через автоматичні дозатори). При безперервному введенні ЛЗ його концентрація в організмі змінюється плавно і не піддається значним коливанням
Б) переривчасте введення (ін'єкційним або неін'єкційним способами) - введення ліків через певні проміжки часу (інтервали дозування). При переривчастому введенні ЛЗ його концентрація в організмі безперервно коливається. Після прийому певної дози вона спочатку підвищується, а потім поступово знижується, досягаючи мінімальних значень перед черговим введенням ліки. Коливання концентрації тим значніше, чим більше вводиться доза ліків і інтервал між введеннями.
інтервал введення - інтервал між вводяться дозами, що забезпечує підтримку терапевтичної концентрації речовини в крові.
16. Введення ліків з постійною швидкістю. Кінетика концентрації препарату в крові. Стаціонарна концентрація препарату в крові ( Css), Час її досягнення, розрахунок і управління нею.
 Особливість введення ЛЗ з постійною швидкістю - плавну зміну його концентрації в крові при введенні, при цьому:
Особливість введення ЛЗ з постійною швидкістю - плавну зміну його концентрації в крові при введенні, при цьому:
1) час досягнення стаціонарної концентрації ліки становить 4-5t½ і не залежить від швидкості інфузії (величини дози, що вводиться)
2) при збільшенні швидкості інфузії (дози, що вводиться) величина СSS також збільшується в пропорційне число раз
3) елімінація ліків з організму після припинення інфузії займає 4-5t½.
ЗSs - рівноважна стаціонарна концентрація - концентрація ЛЗ, що досягається при швидкості введення рівної швидкості виведення, тому:
![]() (З визначення кліренсу)
(З визначення кліренсу)
За кожний наступний період напіввиведення концентрація ЛЗ приростає на половину від залишилася концентрації. Всі ЛЗ, що підкоряються закону елімінації першого порядку, досягатимутьCss через 4-5 періодів напіввиведення.
Підходи до управління рівнем СSs: Змінити вводиться дозу ЛЗ або інтервал введення
17. Переривисте введення ліків. Кінетика концентрації препарату в крові, терапевтичний і токсичний діапазон концентрацій. Розрахунок стаціонарної концентрації ( CSs), Кордонів її коливань і управління нею. Адекватний інтервал введення дискретних доз.
 Коливання концентрації ЛЗ в плазмі крові: 1 - при постійному внутрішньовенному краплинному введенні; 2-прі дробовому введенні тієї ж добової дози з інтервалом 8 год; 3 - при введенні добової дози з інтервалом 24 год.
Коливання концентрації ЛЗ в плазмі крові: 1 - при постійному внутрішньовенному краплинному введенні; 2-прі дробовому введенні тієї ж добової дози з інтервалом 8 год; 3 - при введенні добової дози з інтервалом 24 год.
Переривчасте введення ЛЗ - введення певної кількості ЛЗ через деякі проміжки часу.
Рівноважна стаціонарна концентрація досягається через 4-5 періодів полуелімінаціі, час її досягнення не залежить від дози (на початку, коли рівень концентрації ЛЗ невисокий, швидкість його елімінації також невисока; в міру збільшення кількості речовини в організмі наростає і швидкість його елімінації, тому рано чи пізно настане такий момент, коли збільшена швидкість елімінації врівноважить вводиться дозу ЛЗ і подальше зростання концентрації припинитися)
Css прямо пропорційна дозі ЛЗ і обернено пропорційна інтервалу введення і кліренсу ЛС.
Межі коливань Css: ![]() ; Cssmin \u003d Cssmax × (1 - ел. Фр.). Коливання концентрації ЛЗ пропорційні T / t1 / 2.
; Cssmin \u003d Cssmax × (1 - ел. Фр.). Коливання концентрації ЛЗ пропорційні T / t1 / 2.
Терапевтичний діапазон (коридор безпеки, терапевтичне вікно) - це інтервал концентрацій від мінімальної терапевтичної до викликає поява перших ознак побічних дій.
токсичний діапазон - інтервал концентрації від вищої терапевтичної до смертельної.
Адекватний режим введення дискретних доз: Такий режим введення, при якому флуктуація концентрації препарату в крові укладається в терапевтичний діапазон. Для визначення адекватного режиму введення ЛЗ необхідно розрахувати. Різниця між Cssmax і Cssmin при цьому не повинна перевищити 2Css.
управління коливаннямиCss:
розмах коливаньCss прямо пропорційний дозі ЛЗ і обернено пропорційний інтервалу його введення.
1. Змінити дозу ЛЗ: При збільшенні дози ЛЗ діапазон коливань його Css пропорційно збільшується
2. Змінити інтервал введення ЛЗ: При збільшенні інтервалу введення ЛЗ діапазон коливань його Css пропорційно зменшується
3. Одночасно змінити дозу і інтервал введення
18. Вступна (завантажувальна) доза. Терапевтичний сенс, розрахунок за фармакокінетичними параметрами, умови і обмеження її використання.
Вступна (завантажувальна) доза - доза, що вводиться за один прийом і що заповнює весь обсяг розподілу в чинній терапевтичної концентрації. ВД \u003d (Css * Vd) / F; \u003d Мг / л, \u003d л / кг
терапевтичний сенс: Вступна доза швидко забезпечує діючу терапевтичну концентрацію ЛЗ в крові, що дозволяє, наприклад, швидко зняти напад БА, аритмії і т. Д.
Вступна доза може бути введена за один раз лише тоді, коли Ігнорується процес розподілу речовини
Обмеження використання ВД: Якщо розподіл ЛЗ відбувається Значно повільніше, ніж його надходження в кров, Введення відразу всієї завантажувальної дози (особливо внутрішньовенно) створить концентрацію значно вище терапевтичної та зумовить виникнення токсичних ефектів. Умова використання ВД: Тому введення навантажувальних доз Завжди має бути повільним або дробовим.
19. Підтримуючі дози, їх терапевтичний сенс і розрахунок для оптимального режиму дозування.
підтримуюча доза - доза ЛЗ, що вводиться систематично, яка заповнює об'єм кліренсу, т. Е. Той фрагмент Vd, який очищається від ЛЗ за інтервал DT: ПД \u003d (Css * Cl * DT) / F.
терапевтичний сенс: ПД компенсує втрати з кліренсом за інтервал між введеннями препарату.
Розрахунок для оптимального дозування ЛЗ (для швидкого купірування нападу):
1. Розраховуємо ВД: ВД \u003d (Css * Vd) / F
2. Вибираємо інтервал введення DT (зазвичай більшість ЛЗ призначається з інтервалом, близьким до t1 / 2) і розраховуємо ПД: ПД \u003d (Css * Cl * DT) / F
3. Перевіряємо, чи не виходять коливання ЛЗ в крові за межі терапевтичного діапазону шляхом розрахунку Cssmax і Сssmin: ![]() ; Cssmin \u003d Cssmax × (1 - ел. Фр.). Різниця між Cssmax і Сssmin не повинна перевищувати двох Css.
; Cssmin \u003d Cssmax × (1 - ел. Фр.). Різниця між Cssmax і Сssmin не повинна перевищувати двох Css.
Елімініруемая фракція знаходиться за графіком (див. В.16) або за формулою: ![]()
4. Якщо при обраному нами інтервалі введення ЛЗ його коливання виходять за межі терапевтичного діапазону, міняємо DT і повторюємо розрахунок (пункт 2 - пункт 4)
NB! Якщо ЛЗ не призначене для купірування невідкладних станів або приймається в таблетках, ВД не розраховується.
20. Індивідуальні, вікові і статеві відмінності фармакокінетики ліків. Поправки для розрахунку індивідуальних значень обсягу розподілу ліків.
1. вікові відмінності фармакокінеткікі ліків.
|
1. Роговий шар шкіри тонше, тому при нашкірному застосуванні ЛЗ всмоктуються краще. Абсорбція ЛЗ при ректальному застосуванні також краще. 2. Обсяг рідини в організмі дітей 70-80%, тоді як у дорослих тільки »60%, тому Vd гідрофільних ЛЗ у них більше і потрібні більш високі дози. 3. У новонародженого рівень альбуміну в плазмі нижче, ніж у дорослих, тому зв'язування ЛЗ з білком у них менш інтенсивне 4. У новонароджених низька інтенсивність систем Р450 і кон'югується ферментів, але висока активність метилирующих систем. 5. Швидкість клубочкової фільтрації в нирках дітей до 6 міс становить 30-40% швидкості дорослих, тому ниркова ексркеція ліків знижена. |
1. Відзначається зниження концентрації альбуміну в плазмі крові і фракція ліки, пов'язана з білком 2. Зменшується вміст води в організмі з 60% до 45%, тому збільшується кумуляція ліпофільних ліків. 3. Швидкість клубочкової фільтрації може падати до 50-60% від швидкості зрілого пацієнта, тому ниркова елімінація ліків різко обмежується. |
2. Статеві відмінності в дії ліків. Для жінок характерна менша маса тіла, ніж для чоловіків, тому і величина доз ліки для них повинна знаходитися, як правило, біля нижньої межі діапазону терапевтичних доз.
3. Патологічні стану організму і дію ліків
А) захворювання печінки: F ЛЗ через виключення пресистемного метаболізму, фракція незв'язаного ЛЗ через нестачу синтезу альбумінів, пролонгируются ефекти ЛЗ через ¯ їх біотрансформації.
Б) патологія нирок: сповільнюється елімінація ЛЗ, які виводяться через нирки
4. Генетичні чинники - дефіцит тих чи інших ферментів метаболізму ЛЗ може сприяти пролонгації їх дії (псевдохолінестеразой і т. Д.)
Поправки для розрахунку індивідуальних значень обсягу розподілу ЛЗ:
А) при ожирінні ліпофобних ЛЗ не розчинний в жировій тканині Þ необхідно обчислити ідеальна вага по зростанню (формула Брока: ідеальна вага \u003d зріст (в см) - 100) і перерахувати Vd на ідеальну вагу по росту.
Б) при набряках потрібно обчислити надлишковий обсяг води \u003d зайва вага - ідеальний, Vd треба збільшувати на літр кожного надлишкового кілограма води.
Залежність основних фармакокінетичних параметрів від різних чинників:
1. Всмоктування ЛЗ: при віку ¯ абсорбція ЛЗ, його метаболізм в ході пресистемної елімінації, змінюється біодоступність ЛЗ.
2. Обсяг розподілу Vd: ¯ з віком і при ожирінні, при набряках
3. Період напіввиведення: змінюється з віком і при ожирінні (т. К. Зменшується Vd)
4. Кліренс: визначається функціональним станом нирок та печінки
21. Нирковийкліренс ліків, механізми, їх кількісні та якісні характеристики.
Нирковий кліренс - це міра об'єму плазми крові, яка очищається від лікарського речовини в одиницю часу нирками: Cl (мл / хв) \u003d U × V / P, де U - концентрація ЛЗ в мл сечі, V - об'єм сечі, що виділяється в хв і P \u003d концентрація ЛЗ в мл плазми.
Механізми ниркового кліренсу і їх характеристика:
1. фільтраціяЛЗ, що виділяється тільки фільтрацією (Інсулін) матиме кліренс, рівний СКФ (125-130 мл / хв)
Визначається: нирковим кровотоком, незв'язаної фракцією ЛЗ і фільтраційної здатністю нирок.
Більшість препаратів має низькі молекулярні маси і тому вільно фільтрується від плазми в клубочке.
2. активна секреціяЛЗ, що виділяється Фільтрацією і повної секрецією (Парааміногіппуріевая кислота), буде мати кліренс, рівний почечному плазмовому кліренсу (650 мл / хв)
Нирковий каналець містить дві транспортних системи, Які можуть виділити препарати в ультрафильтрат, одна для органічних кислот і інша для органічних підстав. Ці системи вимагають енергії для активного транспорту проти градієнта концентрацій; вони - місце конкуренції за переносника одних лікарських речовин з іншими.
Визначається: максимальною швидкістю секреції, об'ємом сечі
3. реабсорбція: Значення кліренсу між 130 і 650 мл / хв припускають, що ЛЗ Фільтрується, виділяється, і частково повторно реабсорбируется
Реабсорбція відбувається протягом усього ниркового каналу і залежить від полярності ЛЗ, реабсорбируются неполярні, ліпофільні.
Визначається: величиною рН первинної та іонізацією ЛЗ
Ряд таких показників як Вік, спільне вживання декількох лікарських препаратів, хвороби значно впливають на нирковий кліренс:
А) ниркова недостатність ® зменшення кліренсу ЛС® високий рівень ЛЗ в крові
Б) гломерулонефрит ® втрата сироваткового білка, який зазвичай був доступний і пов'язував ЛЗ ® збільшення рівня вільної фракції ЛЗ в плазмі
22. Фактори, що впливають на нирковий кліренс ліків. Залежність кліренсу від фізико-хімічних властивостей лікарських засобів.
Фактори, що впливають на нирковийCl:
А) гломерулярна фільтрація
Б) швидкість ниркового кровотоку
В) максимальна швидкість секреції
Г) обсяг сечі
Д) фракція незв'язана в крові
Залежність ниркового кліренсу від фізико-хімічних властивостей ЛВ:
Загальні закономірності:1) полярні ЛЗ НЕ реабсорбируются, неполярні - реабсорбируются 2) іонні ЛЗ секретируются, що не іонні - НЕ секретируются.
I. Неполярні неіоногенні речовини: фільтруються тільки в незв'язаних формах, які не секретуються, реабсорбируются
Нирковий кліренс малий і визначається: а) фракцією ЛЗ, незв'язаної в крові б) обсягом сечі
II. Полярні неіоногенні речовини: фільтруються в незв'язаної формі, не секретують, що не реабсорбуються
Нирковий кліренс високий, визначається: а) фракцією ЛЗ, незв'язаної в крові б) швидкістю гломерулярної фільтрації
III. Іонізовані в сечі неполярні в неіонної формі: фільтруються, активно секретуються, неполярні реабсорбируются
Нирковий кліренс визначається: а) фракцією ЛЗ, незв'язаної в крові б) фракцією ЛЗ, іонізованої в сечі в) обсягом сечі
IV. Іонізовані в сечі полярні в неіонізованому вигляді: фільтруються, активно секретуються, що не реабсорбуються
Нирковий кліренс визначається: а) нирковим кровотоком і швидкістю гломерулярної фільтрації б) максимальною швидкістю секреції
23. Печінковий кліренс ліків, його детермінанти та обмеження. Ентерогепатичній цикл лікарських засобів.
Механізми печінкового кліренсу:
1) метаболізм (біотрансформація) шляхом окислення, відновлення, алкілування, гідролізу, коньюгации і т. Д.
Основна стратегія метаболізму ксенобіотиків: неполярні речовини ® полярні (гідрофільні) метаболіти, що виводяться з сечею.
2) секреція (виведення нетрансформованих речовин в жовч)
Тільки полярні речовини з молекулярною масою\u003e 250 активної транспортуються в жовч (органічні кислоти, підстави).
Детермінанти печінкового кліренсу:
А) Швидкість кровотоку в печінці
Б) максимальна швидкість екскреції або метаболічних перетворень
В) Km - константа Міхаеліса
Г) Незв'язана з білком фракція
Обмеження печінкового кліренсу:
1. Якщо Vmax / Km велике → Cl печ \u003d швидкості кровотоку в печінці
2. Якщо Vmax / Km середні величини → Cl \u003d сума всіх факторів
3. Якщо Vmax / Km мало → Cl печ малий, обмежений
Ентерогепатичній цикл ЛС -Ряд препаратів і продуктів їх перетворення в значній кількості виводиться з жовчю в кишечник, звідки частково виводиться з екскрементами, а частково - Повторно всмоктується в кров, Знову потрапляє в печінку і виводиться в кишечник.
Печінкова елімінація препаратів може бути значно змінена Хворобою печінки, віком, дієтою, генетикою, тривалість призначення лікарських засобів (Наприклад, внаслідок індукція печінкових ферментів), та інших факторів.
24. Фактори, що змінюють кліренс лікарських речовин.
1. Взаємодії ЛЗ на рівні: ниркової секреції, біохімічної трансформації, явищ ферментативної індукції
2. Хвороби нирок: порушення кровотоку, гострі і хронічні ураження нирок, результати тривалих ниркових захворювань
3. Хвороби печінки: алкогольний цироз, первинний цироз, гепатити, гепатоми
4. Хвороби шлунково-кишкового тракту і ендокринних органів
5. Індивідуальна непереносимість (відсутність ферментів ацетилювання - непереносимість аспірину)
25. Корекція лікарської терапії при захворюваннях печінки і нирок. Загальні підходи. Корекція режиму дозування під контролем загального кліренсу препарату.
1. Скасувати препарати, які не є необхідними
2. При захворюваннях нирок використовувати препарати, що виділяються з печінкою і навпаки.
3. Знизити дозу або збільшити інтервал між введеннями
4. Ретельний моніторинг за побічними і токсичними ефектами
5. При відсутності фармакологічного ефекту підвищувати дозу необхідно повільно і під контролем фармакологічних і токсичних ефектів
6. При можливості визначити концентрацію речовини в плазмі і коригувати терапію по Сl препарату індивідуально
7. Використовувати непрямий спосіб оцінки Cl.
Корекція режиму дозування під контролем загального кліренсу препарату:
корекція дози : Дінді. \u003d Дтіпічн. × Clінд. / Clтіпічн.
При безперервному внутрішньовенному введенні препарату: Швидкість введення індивідуальна \u003d Швидкість введення типова × Cl інд. / Cl стандартний.
При переривчастому введенні: 1) змінити дозу 2) змінити інтервал 3) змінити обидва параметри. Наприклад, при зменшенні кліренсу на 50% можна зменшити на 50% дозу і зберегти інтервал або збільшити в два рази інтервал і зберегти дозу. Переважно зменшувати дозу і зберігати інтервал введення.
26. Корекція режиму дозування під контролем залишкової функції нирок.
кліренс креатиніну - найважливіший кількісний індикатор функції нирок, на основі якого можна скоректировать режим дозування
Нам відомо:
А) залишкова функція нирок, що визначається кліренсом креатиніну у даного хворого Clкр / хворого
Б) загальний кліренс даного ЛЗ (СlЛС / загальний) і частка ниркового кліренсу ЛС в загальному кліренсі
В) нормальний кліренс креатиніну Clкр / норма по нормограми
3) Css і F для даного ЛЗ (з довідника)
знайтиДозу ЛЗ для даного хворого
ClЛС / нирковий норма \u003d ClЛС / загальний Х частку ниркового кліренсу ЛС в загальному кліренсі
СlЛС / нирковий хворого \u003d Clкр / хворого / Сlкр / норма * ClЛС / нирковий норма
ClЛС / НЕ нирковий норма \u003d ClЛС / загальний - ClЛС / нирковий норма
ClЛС / загальний хворого \u003d СlЛС / нирковий хворого + ClЛС / НЕ нирковий норма
Доза даного ЛЗ всередину при нормальній функції нирок дорівнює: ПДнорма \u003d Css X Cl / F
Доза даного ЛЗ всередину для нашого хворого дорівнює: ПДбольного \u003d ПДнорма Х СlЛС / загальний хворого / СlЛС / загальний
відповідь: ПДбольного
27. Корекція лікарської терапії при ураженні печінки та інших патологічних станах.
Захворювання печінки можуть знижувати кліренс і подовжувати період напіввиведення багатьох ЛЗ. Однак у деяких препаратів, які елімінуються печінкою, не відбувається зміни цих показників при порушеннях функції печінки, тому Захворювання печінки не завжди впливають на власний печінковий кліренс. В даний час немає надійного маркера, який можна було б використовувати для передбачення печінкового кліренсу подібного кліренсу креатиніну.
Корекцію режиму дозування при захворюванні нирок см. Вище в в.26, загальні принципи корекції - в.25.
28. Стратегія індивідуальної лікарської терапії.
Визнання важливої \u200b\u200bролі концентрації як сполучної ланки фармакокінетики і фармакодинаміки сприяє створенню стратегії цільової концентрації - оптимізації дози у даного хворого на основі вимірювання концентрації ЛЗ. Вона складається з наступних етапів:
1. Вибір цільової концентрації
2. Розрахунок Vd і Cl на основі типових значень і внесення поправок з урахуванням таких факторів як маса тіла і функція нирок.
3. Введення завантажувального дози або підтримуючої дози, розрахованих з урахуванням значень TC, Vd і Cl.
4. Реєстрація реакції хворого і визначення концентрації ЛЗ
5. Перегляд Vd і Cl на основі результатів вимірювання концентрації.
6. Повторити кроків 3-6 з метою підбору необхідної для оптимальної реакції на ліки підтримуючої дози.
29. Біотрансформація лікарських засобів, її біологічний сенс, основна спрямованість і вплив на активність ліків. Основні фази метаболічних перетворень ліків в організмі.
Біотрансформація ЛЗ - хімічні перетворення ЛЗ в організмі.
Біологічний сенс біотрансформації ЛЗ: Створення субстрату, зручного для подальшої утилізації (в якості енергетичного або пластичного матеріалу) або в прискоренні виведення ЛЗ з організму.
Основна спрямованість метаболічних перетворень ЛЗ: Неполярні ЛЗ → полярні (гідрофільні) метаболіти, що виводяться з сечею.
Виділяють дві фази метаболічних реакцій ЛЗ:
1) метаболічна трансформація (Несинтетичних реакції, фаза 1) - перетворення речовин за рахунок мікросомального і внемікросомального окислення, відновлення і гідролізу
2) Кон'югація (синтетичні реакції, фаза 2) - біосинтетичний процес, що супроводжується приєднанням до лікарської речовини або його метаболітів ряду хімічних угруповань або молекул ендогенних з'єднань шляхом а) освіти глюкуронидов б) ефірів гліцерину в) сульфоефіров г) ацетилювання д) метилування
Біологічна трансформація суттєво вплине на фармакологічну активність лікарських засобів:
1) найчастіше метаболіти біотрансформації є неактивними або їх активність знижена в порівнянні з вихідною речовиною
2) в деяких випадках метаболіти можуть зберігати активність і навіть перевершувати за активністю вихідна речовина (кодеїн метаболізується до більш фармакологічно активного морфіну)
3) іноді в ході біотрансформації утворюються токсичні речовини (метаболіти ізоніазиду, лідокаїну)
4) іноді в ході біотрансформації утворюються метаболіти з протилежними фармакологічними властивостями (метаболіти неселективних агоністів b2- адренорецепторов мають властивості блокаторів цих рецепторів)
5) ряд речовин є проліками, які початково не дають фармакологічних ефектів, але в ході біотрансформації перетворюються в БАВ (неактивна L-допа, проникаючи через гематоенцефалічний бар'єр, перетворюється в мозку в активний дофамін, при цьому немає системних ефектів дофаміну).
30. Клінічне значення біотрансформації ліків. Вплив статі, віку, маси тіла, екологічних чинників, Куріння, алкоголю на біотрансформацію ліків.
Клінічне значення біотрансформації ЛЗ: Т. К. Доза і частота прийому, необхідні для досягнення ефективної концентрації в крові і тканинах, можуть варіювати у хворих через індивідуальних відмінностей в розподілі, швидкості метаболізму та елімінації ЛЗ, важливий їх облік в клінічній практиці.
Вплив на біотрансформацію ЛЗ різних чинників:
А) функціональний стан печінки: При її захворюваннях кліренс ЛЗ зазвичай зменшується, а період полуелімінаціі зростає.
Б) Вплив факторів середовища: Куріння сприяє індукції цитохрому P450, в результаті чого прискорюється метаболізм ЛЗ в ході мікросомального окислення
В) У вегетаріанців біотрансформація ЛЗ уповільнена
Г) у літніх і молодих пацієнтів характерна підвищена чутливість до фармакологічному або токсичної дії ЛЗ (у осіб похилого віку та у дітей до 6 міс активність мікросомального окислення знижена)
Д) у чоловіків метаболізм деяких лікарських засобів відбувається швидше, ніж у жінок, т. К. Андрогени стимулюють синтез ферментів печінки (етанол)
Е) Високий вміст в їжі білків і інтенсивна фізичне навантаження : Прискорення метаболізму ЛЗ.
Ж) Алкоголь і ожиріння уповільнюють метаболізм ЛЗ
31. Метаболічний взаємодія ліків. Хвороби, що впливають на їх біотрансформацію.
Метаболічна взаємодія ЛЗ:
1) індукція ферментів метаболізму ЛЗ - абсолютне збільшення їх кількості та активності внаслідок впливу на них певних ЛЗ. Індукція веде до прискорення метаболізму ЛЗ і (як правило, але не завжди) до зниження їх фармакологічної активності (рифампіцин, барбітурати - індуктори цитохрому P450)
2) інгібування ферментів метаболізму ЛЗ - пригнічення активності ферментів метаболізму під дією деяких ксенобіотиків:
А) конкурентну метаболічна взаємодія - ЛЗ з високим аффинитетом до певних ферментів знижують метаболізм ЛЗ з більш низьким аффинитетом до цих ферментам (верапаміл)
Б) зв'язування з геном, що індукують синтез певних ізоферментів цитохрому P450 (цімедін)
В) пряма інактивація ізоферментів цитохрому P450 (флавоноїди)
Хвороби, що впливають на метаболізм ЛЗ:
А) хвороби нирок (порушення ниркового кровотоку, гострі і хронічне захворювання нирок, результати тривалих ниркових захворювань)
Б) хвороби печінки (первинний і алкогольний цироз, гепатити, гепатоми)
В) хвороби шлунково-кишкового тракту і ендокринних органів
В) індивідуальна непереносимість деяких ЛЗ (відсутність ферментів ацетилювання - непереносимість аспірину)
32. Шляхи та механізми виведення ліків з організму. Можливості управління виведенням ліків.
Шляхи та механізми виведення ЛЗ: елімінація ЛЗ печінкою і нирками і деякими іншими органами:
А) нирками шляхом фільтрації, секреції, реабсорбції
Б) печінкою шляхом біотрансформації, екскреції з жовчю
В) через легені, слину, піт, молоко і т. Д. Шляхом секреції, випаровування
Можливості управління процесами виведення ЛЗ:
1. управління pH: в лужній сечі підвищується виведення кислих сполук, в кислому - виведення основних з'єднань
2. застосування жовчогінних препаратів (холензим, аллохол)
3. гемодіаліз, перитонеальний діаліз, гемосорбція, лимфосорбция
4. форсований діурез (в / в NaCl або глюкоза для водного навантаження + фуросемід або манітол)
5. промивання шлунка, застосування клізм
33. Концепція рецепторів в фармакології, молекулярна природа рецепторів, сигнальні механізми дії ліків (типи трансмембранної сигналізації і вторинні посередники).
рецептори -Молекулярні компоненти клітини або організму, які взаємодіють з ЛЗ і індукують ряд біохімічних подій, що ведуть до розвитку фармакологічного ефекту.
Концепція рецепторів в фармакології:
1. Рецептори детермінують кількісні закономірності дії ЛЗ
2. Рецептори відповідальні за селективність дії ЛЗ
3. Рецептори посередники дії фармакологічних антагоністів
Концепція рецепторів - основа цілеспрямованого застосування лікарських засобів, що впливають на регуляторні, біохімічні процеси і комунікації.
Молекулярна природа рецепторів:
1. регуляторні білки, посередники дії різних хімічних сигналів: нейромедіаторів, гормонів, аутокоідов
2. ферменти і трансмембранні білки переносники (Na +, K + АТФази)
3. структурні білки (тубулін, білки цитоскелета, клітинна поверхня)
4. ядерні білки і нуклеїнові кислоти
Сигнальні механізми дії ліків:
1) проникнення розчинних в ліпідах лігандів через мембрану і їх дію на внутрішньоклітинні рецептори.
2) сигнальна молекула зв'язується з позаклітинним доменом трансмембранного білка і активує ферментативну активність його цитоплазматического домену.
3) сигнальна молекула зв'язується з іонним каналом і регулює його відкриття.
4) сигнальна молекула зв'язується з рецептором на поверхні клітини, який пов'язаний з еффекторним ферментом за допомогою G-білка. G-білок активує вторинний посередник.
Типи трансмембранної сигналізації:
А) через 1-TMS-рецептори, що володіють і не володіють тірозінкіназной активністю
Б) через 7-ТMS-рецептори, пов'язані з G-білком
В) через іонні канали (ліганд-залежні, потенціал-залежні, щілинні контакти)
вторинні посередники: ЦАМФ, іони Ca2 +, ДАГ, ІФ3.
34. Фізико-хімічні та хімічні механізми дії лікарських речовин.
А) Фізико-хімічна взаємодія з біосубстратами - неелектролітное дію.
Основні фармакологічні ефекти: 1) наркотичну 2) загально депресивний 3) паралізує 4) місцево подразнюючу 5) мембранолитического дії.
Хімічна природа речовин: хімічно інертні вуглеводні, ефіри, спирти, альдегіди, барбітурати, газові наркотичні засоби
Механізм дії - оборотне деструірованіе мембран.
Б) хімічний (Молекулярно-біохімічний) механізм дії лікарських засобів.
Основні типи хімічної взаємодії з біосубстратами:
- Слабкі (Нековалентні, оборотні взаємодії) (водневі, іонні, монодіпольние, гідрофобні).
- Ковалентні зв'язки (алкілування).
Значення нековалентних взаємодій ЛЗ: Дія неспецифічно, не залежить від хімічної будови речовини.
Значення ковалентних взаємодій ЛЗ: Дія специфічно, критично залежить від хімічних будови, Реалізується за допомогою впливу на рецептори.
35. Терміни і поняття кількісної фармакології: ефект, ефективність, активність, агоніст (повний, частковий), антагоніст. Клінічне відмінність понять активність і ефективність ліків.
 Ефект (відповідь)- кількісний вихід реакції взаємодії клітини, органу, системи або організму з фармакологічним агентом.
Ефект (відповідь)- кількісний вихід реакції взаємодії клітини, органу, системи або організму з фармакологічним агентом.
ефективність - міра реакції по осі ефекту - величина відгуку біологічної системи на фармакологічний вплив; Це здатність ЛЗ надавати максимально можливе для нього дію. Т. е. Фактично це максимальна величина ефекту, яку можна досягти при введенні даних ліків. Чисельно характеризується величиною Еmax. Чим вище Еmax, тим вище ефективність ліків
активність - міра чутливості до ЛЗ по осі концентрацій, характеризує аффинность (спорідненість ліганда до рецептора), Показує, яка доза (концентрація) ЛЗ здатна викликати розвиток стандартного ефекту, рівного 50% від максимально можливого для цих ліків. Чисельно характеризується величиною ЕС50 або ED50. Чим вище активність ЛЗ, тим менша його доза потрібна для відтворення терапевтичного ефекту.
Ефективність: 1 \u003d 2\u003e 3
Активність: 1\u003e 3\u003e 2
У клінічній діяльності важливіше знати ефективність, а не активність, т. К. Нас більше цікавить здатність ЛЗ викликати певну дію в організмі.
агоніст- ліганд, який зв'язується з рецептором і викликає біологічну реакція, спрацьовування фізіологічної системи. повний агонист- максимальний відгук, частковий - викликають меншу реакцію навіть при окупації всіх рецепторів.
антагоніст - ліганди займають рецептори або змінюють їх таким чином, що вони втрачають здатність взаємодіяти з іншими лігандами, але самі не викликають біологічної реакції (блокують дію агоністів).
 конкурентні антагоністи- взаємодіють з рецепторами оборотно і тим самим конкурують з агоністами. Збільшення концентрації агоніста може повністю усунути ефект антагоніста. Конкурентний антагоніст зрушує криву «доза-ефект» для агоніста, збільшує EC50, не впливає на Emax.
конкурентні антагоністи- взаємодіють з рецепторами оборотно і тим самим конкурують з агоністами. Збільшення концентрації агоніста може повністю усунути ефект антагоніста. Конкурентний антагоніст зрушує криву «доза-ефект» для агоніста, збільшує EC50, не впливає на Emax.
неконкурентні антагоністи- незворотньо змінюють спорідненість рецепторів до агоністи, зв'язування часто відбувається не з активною ділянкою рецептора, збільшення концентрації агоніста не усуває дію антагоніста. Неконкурентний антагоніст знижує Emax, не змінює EC50, крива «доза-ефект» стискається щодо вертикальної осі.
36. Кількісні закономірності дії ліків. Закон зменшення відгуку біологічних систем. Модель Кларка і її наслідки. Загальний вид залежності концентрація - ефект в нормальних і логнормального координатах.
Модель Кларка-Аріенса:
1. Взаємодія між лігандом (L) і рецептором (R) оборотні.
2. Всі рецептори для даного ліганду - еквівалентні і незалежні (їх насичення не впливає на інші рецептори).
3. Ефект прямо пропорційний числу зайнятих рецепторів.
4. Ліганд існує в двох станах: вільному і пов'язаному з рецептором.
А) ![]() , Де Kd - константа рівноваги, Ke - внутрішня активність.
, Де Kd - константа рівноваги, Ke - внутрішня активність.
Б) Т. к. При зростанні кількості лігандів в якийсь момент часу всі рецептори виявляться зайняті, то максимально можливу кількість освічених комплексів ліганд-рецептор описується формулою:
\u003d [R] × ![]() (1)
(1)
Ефект визначається ймовірністю активації рецептора при зв'язуванні з лігандом, т. Е. Його внутрішньої активністю (Ке), тому E \u003d Ke ×. При цьому ефект максимальний при Ке \u003d 1 і мінімальний і Ке \u003d 0. Природно, що максимальний ефект описується співвідношенням Emax \u003d Ke ×, де - загальне число рецепторів для даного ліганду
Ефект залежить і від концентрації ліганда на рецепторах [З], тому
E \u003d Emax ![]() (2)
(2)
З наведених співвідношень випливає, що EC50 \u003d Kd
![]()
Emax - максимальний ефект, Bmax - максимальне число пов'язаних рецепторів, EC50 - концентрація ЛЗ, при якій виникає ефект, рівний половині від максимального, Kd - константа дисоціації речовини від рецептора, при якій пов'язано 50% рецепторів.
Закону убування відгуку відповідає параболічна залежність «концентрація - ефективність». Відповідь на малі дози ЛЗ зазвичай зростає прямо пропорційно дозі. Однак при збільшенні дози приріст відповідної реакції знижується і в кінцевому рахунку може бути досягнута доза, при якій не відбувається подальшого збільшення відповіді (за рахунок окупації всіх рецепторів для даного ліганду).
37. Зміна ефекту ліків. Градуальная і квантова оцінка ефекту, сутність і клінічні додатки. заходи кількісної оцінки активності і ефективності ліків в експериментальній і клінічній практиці.
Всі фармакологічні ефекти можна умовно розділити на дві категорії:
А) Градуально (безперервні, інтегральні) ефекти - такі ефекти ЛЗ, які можуть бути виміряні кількісно (дію гіпотензивних ЛЗ - за рівнем артеріального тиску). Описуються градуально «кривої доза-ефект» (див. Ст. 36), на основі якої можна оцінити: 1) індивідуальну чутливість до ЛЗ 2) активність ЛЗ 3) максимальну ефективність ЛЗ
Б) квантові ефекти - такі ефекти ЛЗ, які є дискретною величиною, якісною ознакою, т. Е. Описуються всього лише кількома варіантами станів (головний біль після прийому анальгетика або є, або немає). Описується квантовою кривої доза-ефект, де відзначають залежність прояву ефекту в популяції від величини прийнятої дози ЛЗ. Графік залежності доза-ефект при цьому має куполоподібний вигляд і ідентичний кривою Гаусса нормального розподілу. На основі квантової кривої можна: 1) оцінити популяционную чутливість ЛЗ 2) зазначити наявність ефекту при даній дозі 3) вибрати середню терапевтичну дозу.
Відмінності між градуально і квантової характеристикою «доза-ефект»:
Кількісна оцінка активності та ефективності ЛЗ проводиться на основі побудови кривих «доза-ефект» і їх подальшій оцінці (див. В.35)
38. Види дії лікарських засобів. Зміна дії ліків при їх повторному введенні.
Види дії ЛЗ:
1. Місцева дія - дія речовини, що виникає на місці його застосування (анестетик - на слизову оболонку)
2. Резорбтивна (системне) дію - дія речовини, розвивається після його всмоктування, надходження в загальний кровотік, а потім в тканини. Залежить від шляхів введення ЛЗ і їх здатності проникати через біологічні бар'єри.
Як при місцевому, так і резорбтивном дії лікарські засоби можуть надавати або пряме, або рефлекторне вплив:
А) прямий вплив - безпосередній контакт з органом-мішенню (адреналін на серце).
Б) рефлекторне - зміна функції органів або нервових центрів шляхом впливу на Екстер - і інтерорецептори (гірчичники при патології органів дихання рефлекторно поліпшують їх трофіку)
Зміни дії ЛЗ при їх повторному введенні:
1. Кумуляция- збільшення ефекту внаслідок накопичення в організмі ЛЗ:
а) матеріальна кумуляція - накопичення діючої речовини в організмі (серцеві глікозиди)
б) функціональна кумуляція - наростаючі зміни функції систем організму (зміни функції ЦНС при хронічному алкоголізмі).
2. Толерантність (звикання) -Зниження відповідної реакції організму на повторні введення ЛЗ; для того, щоб відновити реакцію на ЛЗ, його доводиться вводити в усі більших і більших дозах (діазепам):
А) справжня толерантність - спостерігається як при ентеральному, так і при парентеральному введенні ЛЗ, не залежить від ступеня його всмоктування в кров. В її основі - фармакодинамические механізми звикання:
1) десенситизация - зниження чутливості рецептора до лікарського засобу (b-адреноміметики при тривалому застосуванні призводять до фосфорилированию b-блокатори, які не здатні відповісти на b-адреноміметики)
2) Down-регуляція - зниження числа рецепторів до лікарського засобу (при повторних введеннях наркотичних анальгетиків кількість опіоїдних рецепторів знижується і потрібні все більші і більші дози ліків, щоб викликати бажану відповідь). Якщо ЛЗ блокує рецептори, то механізм толерантності до нього може бути пов'язаний з up-регуляцією - збільшенням числа рецепторів до лікарського засобу (b-адреноблокатори)
3) включення компенсаторних механізмів регуляції (при повторних введеннях гіпотензивних препаратів колапс виникає значно рідше, ніж при першому введенні за рахунок адаптації барорецепторів)
Б) відносна толерантність (псевдотолерантності) - розвивається тільки при введенні ЛЗ всередину і пов'язаний зі зниженням швидкості і повноти всмоктування ліки
3. Тахіфілаксія - стан, при якому часте введення ЛЗ викликає розвиток толерантності вже через кілька годин, але при досить рідкісних введениях ЛЗ його ефект зберігається в повній мірі. Розвиток толерантності пов'язано зазвичай з виснаженням ефекторних систем.
4. Лікарська залежність - непереборне прагнення до прийому речовини, що вводиться раніше. Виділяють психічну (кокаїн) та фізичну (морфін) лікарську залежності.
5. Гіперчутливість - алергічна або інша імунологічна реакція на ЛЗ при повторному введенні.
39. Залежність дії ліків від віку, статі та індивідуальних особливостей організму. Значення добових ритмів.
А) від віку: У дітей і у літніх чутливість до ЛЗ підвищена (т. К. У дітей існує недостатність багатьох ферментів, функції нирок, підвищена проникність ГЕБ, в літньому віці загальмовано всмоктування ЛЗ, менш ефективно протікає метаболізм, знижена швидкість екскреції препаратів нирками):
|
1. У новонароджених знижена чутливість до серцевих глікозидів, т. К. У них на одиницю площі кардиомиоцита більше Na + / K + -АТФази (мішеней дії глікозидів). 2. У дітей нижче чутливість до сукцинілхоліну і атракурій, але підвищена чутливість до всіх інших миорелаксантам. 3. Психотропні засоби можуть викликати у дітей аномальні реакції: психостимулятори - можуть підвищувати концентрацію уваги і знижувати моторну гіперактивність, транквілізатори - навпаки, здатні викликати т. Н. атиповий збудження. |
1. Різко зростає чутливість до серцевих глікозидів в зв'язку зі зниженням числа Na + / K + -АТФази. 2. Знижується чутливість до b-адреноблокатори. 3. Підвищується чутливість до блокаторів кальцієвих каналів, т. К. Послаблюється барорефлексов. 4. Відзначається атипова реакція на психотропні лікарські засоби, подібна реакції дітей. |
Б) Від статі:
1) гіпотензивні засоби - клонідин, b-адреноблокатори, діуретики можуть викликати порушення сексуальних функцій у чоловіків, але не впливають на роботу репродуктивної системи жінок.
2) анаболічні стероїди викликають бóльшій ефект в організмі жінок, ніж в організмі чоловіків.
В) Від індивідуальних особливостей організму: Дефіцит або надлишок тих чи інших ферментів метаболізму ЛЗ призводить до збільшення або зменшення їх дії (дефіцит псевдохолінестерази крові - аномально тривала миорелаксация при застосуванні сукцинілхоліну)
Г) Від добових ритмів: Зміна дії ЛЗ на організм кількісно і якісно в залежності від часу доби (максимальна дія при максимальній активності).
40. Варіабельність і мінливість дії ліків. Гіпо - і гіперреактивність, толерантність і тахифилаксия, гіперчутливість і ідіосинкразія. Причини варіабельності дії ліків і раціональна стратегія терапії.
варіабельність відображає різниці між індивідуумами у відповідь на даний лікарський засіб.
Причини варіабельності дії ЛЗ:
1) зміна концентрації речовини в зоні рецептора - через відмінності в швидкості всмоктування, його розподілу, метаболізму, елімінації
2) варіації в концентрації ендогенного ліганда рецептора - пропранолол (β-адреноблокатор) уповільнює ЧСС у людей з підвищеним рівнем катехоламінів в крові, але не впливає на фонову ЧСС у спортсменів.
3) зміна щільності або функції рецепторів.
4) зміна компонентів реакції, розташованих дистальніше рецептора.
Раціональна стратегія терапії: Призначення і дозування ЛЗ з урахуванням перерахованих вище причин варіабельності дії ЛЗ.
гипореактивность - зниження ефекту даної дози ЛЗ в порівнянні з тим ефектом, який спостерігається у більшості пацієнтів. Гіперреакцівность - підвищення ефекту даної дози ЛЗ в порівнянні з тим ефектом, який спостерігається у більшості пацієнтів.
Толерантність, тахифилаксия, гіперчутливість - см. В.38
ідіосинкразія - збочена реакція організму на дане ЛЗ, пов'язана з генетичними особливостями метаболізму ЛЗ або з індивідуальною імунологічної реактивності, в т. Ч. З алергічними реакціями.
41. Оцінка безпеки ліків. Терапевтичний індекс і стандартні кордону безпеки.
Оцінка безпеки здійснюється на двох рівнях:
А) доклінічному (отримання відомостей про токсичність ЛЗ, впливу на репродуктивні функції, Ембріотоксичність і тератогенність, віддалені ефекти)
Б) клінічному (подальша оцінка ефективності та безпеки ЛЗ)
Якщо після того, як досягається плато ефекту, доза ЛЗ буде продовжувати рости, то через певний проміжок часу почне проявлятися його токсичну дію. Залежність токсичної дії від дози (концентрації) ЛЗ носить такий же характер, як і його корисний ефект і може бути описана градуально або квантової кривими. На цих кривих також може бути визначена величина TD50 або ТС50 - токсична доза (концентрація) ЛЗ, яка викликає токсичний ефект, рівний 50% від максимального (для квантової кривої - токсичний ефект у 50% осіб в популяції). Іноді, замість TD50 користуються показником LD50 - летальна доза, Яка викликає загибель 50% об'єктів в популяції.
Оцінка безпеки ЛЗ характеризується на основі градульних або квантових кривих «доза-ефект» і наступних показників:
А) терапевтичний індекс - це співвідношення між токсичної і ефективної дозами ліків, які викликають появу напівмаксимального ефекту: ТИ \u003d TD50 / ED50. Чим більше величина терапевтичного індексу, тим більш безпечним є ліки.
Б) Терапевтична широта (терапевтичне вікно) - це діапазон доз між мінімальною терапевтичною і мінімальною токсичною дозами ЛЗ. Є більш коректним показником безпеки ЛЗ, оскільки дозволяє враховувати ступінь наростання небажаних ефектів на кривій «доза-ефект».
В) Фактор надійної безпеки - це відношення мінімальної токсичної дози до максимальної ефективної (ФНБ \u003d TD1 / ED99), показує, у скільки разів може бути перевищена терапевтична доза ліків без ризику розвитку інтоксикації (небажаних ефектів).
Г) терапевтичний коридор - це діапазон ефективних концентрацій лікарського речовини в крові, які необхідно створити і підтримувати в організмі, щоб забезпечити досягнення бажаного терапевтичного дії.
42.46. Взаємодія ліків. Несумісність ЛЗ (т. К. Питання взаємопов'язані, вибирайте за обставинами)
взаємодія ЛЗ - це зміна вираженості і характеру ефектів при одночасному або попередньому застосуванні декількох ліків.
Причини небажаних взаємодій:
1) полипрагмазия - 6 і більше ЛЗ дають побічних ефектів в 7 разів більше, ніж якщо ЛЗ менше 6.
2) помилки лікарів
3) порушення режиму дозування
Обгрунтування комбінованої терапії:
1. Монотерапія недостатньо ефективна.
2. Відсутність при більшості хвороб етіотропної терапії Þ необхідність лікарського впливу на різні ланки патогенезу
3. поліморбідних - чим старша людина, Тим більше у нього захворювань, що протікають одночасно
4. Потреба у регулюванні небажаних ефектів ЛЗ
5. Зниження кількості прийомів і введення ЛЗ (зручність для пацієнта, економія праці медпрацівників)
Види взаємодії:
I. Фармацевтична взаємодія -Вид взаємодії, пов'язаний з фізико-хімічною реакцією між ЛЗ в процесі виготовлення лікарського препарату, ще до введення цих коштів в організм людини
А) типові помилки, що призводять до фармацевтичної несумісності: виписування складних рецептів, неправильне зберігання, не враховується можливість адсорбції ЛЗ на поверхні пластмаси (органічні нітрати)
Б) проблеми при інфузійної терапії: змішування розчинних солей, похідних нерозчинних слабких кислот або підстав призводить до їх преципітації; в рідких лікарських формах гідролізуються серцеві глікозиди і алкалоїди, руйнуються АБ; рН середовища (в лужному середовищі випадає в осад алкалоїди)
В) рекомендації: 1) Усі суміші краще готувати ex tempore 2) Найбільш надійний розчин з одним ЛЗ 3) Всі розчини перед вживанням необхідно перевірити на наявність суспензій 4) Взаємодія може відбуватися без видимих \u200b\u200bзмін розчинів 5) Не можна додавати ЛЗ в кров і розчини АК 6) При відсутності спеціальних вказівок препарати слід розчиняти в 5% -му розчині глюкози (рН 3,5-6,5), фізіологічному розчині NaCl (рН 4,5-7,0).
Розчин глюкози, стабілізований HCl, несумісний з адреналіном, бензилпенициллином, апоморфіном, канаміцин, вітаміном С, олеандоміцином, серцевимиглікозидами. Серцеві глікозиди несумісні з атропіном, папаверином, платифілін. АБ несумісні з гепарином, гідрокортизоном. Вітаміни групи В несумісні між собою, з вітамінами PP, С. Вітамін РР і С також між собою несумісні.
Не можна змішувати ні з якими іншими препаратами: фенотіазіди, хлорпромазин, барбітурати, препарати вітаміну С, амфотерицин В, фуросемід, сульфадіазин, амінофілін, адреноміметики.
II. Фармакологічна- взаємодія ліків, яке проявляється тільки в організмі людини після їх спільного застосування
А) фармакокинетическое
1) на етапі всмоктування.
при введенніPer Os взаємодія детермінують:
1. кислотність середовища
2. пряму взаємодію в шлунково-кишковому тракті
Тетрацикліни взаємодіють з кальцієм, алюміній, залізо, магній з утворенням хелатних комплексів. Холестирамін порушує всмоктування похідних кислот, препаратів кальцію, Варварина, дигоксину, дигітоксин, жиророзчинних вітамінів, триметоприму, кліндаміцину, цефалексин, тетрацикліну. Препарати заліза краще всмоктуються з вітаміном С. Препарати заліза з карбонатами, тетрациклінами погано всмоктуються.
3. моторика шлунково-кишкового тракту
Уповільнюють перистальтику: деякі антидепресанти, протигістамінні ЛЗ, фенотіазинові антипсихотичні, наркотичні ЛЗ, підвищують абсорбцію дигоксину, кортикостероїдів, антикоагулянтів, знижують всмоктування леводопи. Посилюють перистальтику і збільшують евакуацію з шлунково-кишкового тракту: метоклопрамід, проносні. Знижують всмоктування ЛЗ: фенобарбітал - гризеофульвина, аспірин - індометацину та диклофенаку, ПАСК - рифампіцину.
Способи контролю всмоктування при парентеральному введенні: місцеві анестетики + адреналін + фенілефрин - знижується всмоктування місцевих анестетиків
4. кишкова флора
5. зміна механізму всмоктування
2) при розподілі і депонування:
1. пряму взаємодію в плазмі крові: гентаміцин + ампіцилін або карбенициллин - знижують активність гентаміцину
2. конкурентне витіснення із зв'язку з альбумінами в плазмі крові: індометацин, дигітоксин, варфарин пов'язані з білками крові на 90-98%, отже, підвищення вільної фракції ЛЗ в два рази - різке зростання токсичних ефектів; НПЗЗ витісняють: варфарин, фенітоїн, метотрексат.
Детермінати, що визначають клінічне значення такої взаємодії:
ü величина Vd (велика - немає проблем, мала - можливі)
ü вплив одного ЛЗ речовини на активність механізмів транспорту через механізми інших ЛЗ: дозозависимо підвищується транспорт ЛЗ - інсулін, АКТГ, ангіотензин, кініни та ін .; інсулін підвищує концентрацію ізоніазиду тільки в легких, а концентрацію хлопромазін - тільки в ГМК.
3. витіснення із зв'язку з білками тканини: хінідин витісняє дігоксин + знижує екскрецію нирками, тому підвищується ризик токсичності дигоксину
3) в процесі метаболізму
ЛЗ можуть підвищувати або знижувати активність Р450 і його ферментів (етанол підвищує активність певних ізоферментів цитохрому)
Інгібітори ферментів, часто вступають у взаємодію:
1. АБ: ципрофлоксацин, еритроміцин, ізоніазид, метронідазол
2. Серцево-судинні препарати: аміодарон, дилтіазем, хінідин, верапаміл
3. Антидепресанти: флуоксетин, сертрален
4. Антисекреторні препарати: циметидин, омепразол
5. антиревматичні препарати: аллопуринол
6. Фунгіциди: флуконазол, інтраканазол, кетоконазол, міконазол
7. Противірусні: індинавір, ретонавір, саквінавір
8. Інші: дисульфірам, вальпроат натрію
Препарати, що дають токсичні ефекти при інгібуванні МАО: адреноміметики, симпатоміметики, антипаркинсонические, наркотичні анальгетики, фенотіазини, седативні, антигіпертензивні діуретики, гіпоглікемічні ЛС
4) У процесі виведення - більше 90% ЛЗ виводяться з сечею.
Вплив на рН сечі і на ступінь іонізації ЛЗ, на їх ліпофільність і їх реабсорбцію
1. взаємодія під час пасивної дифузії: частина ЛЗ виводиться в незмінному вигляді, частина ЛЗ іонізується при рН сечі 4,6-8,2. Олужнення сечі клінічно важливо: отруєння ацетилсаліциловою кислотою або фенобарбіталом, при прийомі сульфаніламідів (зниження ризику кристалурії), прийомі хінідину. Підвищення кислотності сечі: підвищується екскреція амфетаміну (має практичне значення для виявлення цього ЛЗ у спортсменів)
2. взаємодія в період активного транспорту: пробенезід + пеніцилін підвищує тривалість руху пеніциліну, пробенецид + саліцилати - усунення урикозуричного дії пробенециду, пеніцилін + СА - зниження екскреції пеніциліну
Вплив складу сечі на екскрецію ЛВ:
Збільшення цукру в сечі - збільшення екскреції: вітаміну С, хлорамфеніколу, морфіну, ізоніазиду, глутатіону і їх метаболітів.
Б) фармакодинамическое це взаємодія ЛЗ, пов'язане зі зміною фармакодинамики одного з них під впливом іншого (під впливом тиреоїдних гормонів посилюється синтез b-блокатори в міокарді і посилюється вплив адреналіну на міокард).
Приклади клінічно значущих небажаних синергічних взаємодій:
НПЗЗ + Варварин - збільшення ризику кровотечі
Алкоголь + бензодіазепіни - потенціювання седативного ефекту
Інгібітори АПФ + К + -сберегающіе діуретики - збільшення ризику гіперкаліємії
Верапаміл + b-адреноблокатори - брадикардія і асистолія
Алкоголь є сильним індуктором ферментів, призводить до розвитку толерантності до лікарських засобів (особливо до наркозних і снодійних засобів), збільшує ризик розвитку лікарської залежності.
43. Взаємодія лікарських засобів. Антагонізм, синергізм, їх види. Характер зміни ефекту ліків (активності, ефективності) в залежності від типу антагонізму.
При взаємодії ЛЗ можливий розвиток таких станів: а) посилення ефектів комбінації ЛЗ б) ослаблення ефектів комбінації ЛЗ в) лікарська несумісність
Посилення ефектів комбінації ЛЗ реалізується в трьох варіантах:
1) Підсумовування ефектів або аддитивное взаємодія - вид лікарської взаємодії при якому ефект комбінації дорівнює простий сумі ефектів кожного з ЛЗ окремо. Т. е. 1+1=2 . Характерний для ЛЗ з однієї фармакологічної групи, які мають спільну мету дії (кислотонейтралізуюча активність комбінації гідроксиду алюмінію і магнію дорівнює сумі їх Кислотонейтралізуючої здібностей окремо)
2) синергізм - вид взаємодії, при якому ефект комбінації перевищує суму ефектів кожного з речовин взятих окремо. Т. е. 1+1=3 . Синергізм може стосуватися як бажаних (терапевтичних), так і небажаних ефектів ліків. Одночасне введення гідрохлортіазиду діхлотіазіда і інгібітору АПФ еналаприлу призводить до посилення гіпотензивної дії кожного із засобів, що застосовується при лікуванні АГ. Однак одночасне призначення аміноглікозиднихантибіотиків (гентаміцину) і петлевого діуретика фуросеміду викликає різке зростання ризику ототоксического дії і розвитку глухоти.
3) потенціювання - вид лікарської взаємодії, при якому одне з ЛЗ, яка сама по собі не робить цього ефекту, може призводити до різкого посилення дії інших ліків. Т. е. 1+0=3 (Клавулановая кислота не має протимікробну дію, але здатна підсилювати ефект b-лактами амоксициліну за рахунок того, що вона блокує b-лактамазу; адреналін не робить місцевоанестезуючого дії, але при додаванні до розчину Ультракаїн він різко подовжує його анестезуючий ефект за рахунок уповільнення всмоктування анестетика з місця ін'єкції).
ослаблення ефектів ЛЗ при їх спільному застосуванні називають антагонізмом:
1) Хімічний антагонізм або антідотізм - хімічну взаємодію речовин між собою з утворенням неактивних продуктів (хімічний антагоніст іонів заліза дефероксамін, який пов'язує їх в неактивні комплекси; протаміну сульфат, молекула якого має надлишковий позитивний заряд - хімічний антагоніст гепарину, молекула якого має надлишковий негативний заряд). Хімічний антагонізм лежить в основі дії антидотів (протиотрут).
2) Фармакологічний (прямий) антагонізм - антагонізм, викликаний різноспрямованим дією 2 лікарських речовин на одні й ті ж рецептори в тканинах. Фармакологічний антагонізм може бути конкурентним (оборотним) і неконкурентним (необоротним):
А) конкурентний антагонізм: конкурентний антагоніст оборотно зв'язується з активним центром рецептора, т. Е. Екранує його від дії агоніста. Т. к. Ступіньзв'язування речовини з рецептором пропорційна концентрації цієї речовини, то дія конкурентного антагоніста можна подолати якщо збільшити концентрацію агоністу. Він буде витісняти антагоніст з активного центру рецептора і викличе відповідну реакцію тканини в повному обсязі. Т. о. конкурентний антагоніст не змінює максимальний ефект агоніста, але для взаємодії агоніста з рецептором потрібно його більш висока концентрація. Конкурентний антагоніст Зрушує криву «доза-ефект» для агоніста вправо щодо вихідних значень і збільшує ЕС50 для агоніста, не впливаючи на величину Е Max.
У медичній практиці досить часто використовують конкурентний антагонізм. Оскільки ефект конкурентного антагоніста може бути подолана, якщо його концентрація впаде нижче рівня агоніста, при лікуванні конкурентними антагоністами необхідно постійно підтримувати його рівень досить високим. Іншими словами, клінічний ефект конкурентного антагоніста буде залежати від періоду його полуелімінаціі і концентрації повного агоніста.
Б) неконкурентний антагонізм: неконкурентний антагоніст зв'язується практично необоротно з активним центром рецептора або ж взаємодіє взагалі з його аллостерическим центром. Тому, як би не підвищувалася концентрація агоніста - він не в змозі витіснити антагоніст з зв'язку з рецептором. Оскільки, частина рецепторів, яка пов'язана з неконкурентним антагоністом вже не здатна активуватися , Значення ЕMax знижується, спорідненість же рецептора до агоністи не змінюється, тому значення ЕС50 залишається колишнім. На кривій залежності «доза-ефект» дію неконкурентного антагоніста проявляється у вигляді стиснення кривої щодо вертикальної осі без її зміщення вправо.
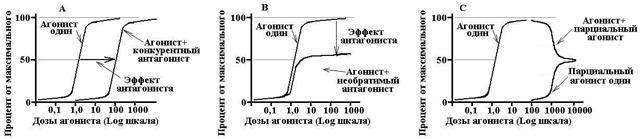
Схема 9. Види антагонізму.
А - конкурентний антагоніст зміщує криву «доза-ефект» вправо, т. Е. Знижує чутливість тканини до агоністи, не змінюючи його ефект. В - неконкурентний антагоніст знижує величину відповіді тканини (ефект), але не впливає на її чутливість до агоністи. З - варіант застосування парціального агоніста на фоні повного агоніста. У міру підвищення концентрації парціальний агоніст витісняє повний з рецепторів і в підсумку відповідь тканини знижується від максимальної відповіді на повний агоніст, до максимального відповіді на агоніст парціальний.
Неконкурентні антагоністи застосовуються в медичній практиці рідше. З одного боку вони мають незаперечну перевагу, т. К. Дію їх не може бути подолане після зв'язування з рецептором, а значить не залежить ні від періоду полуелімінаціі антагоніста, ні від рівня агоніста в організмі. Ефект неконкурентного антагоніста буде визначатися лише швидкістю синтезу нових рецепторів. Але з іншого боку, якщо відбувається передозування цих ліків, усунути його ефект буде надзвичайно складно.
|
конкурентний антагоніст |
неконкурентний антагоніст |
|
Схожий за будовою на агонист |
За будовою відрізняється від агоніста |
|
Зв'язується з активним центром рецептора |
Зв'язується з аллостерическим ділянкою рецептора |
|
Зміщує криву «доза-ефект» вправо |
Зміщує криву «доза-ефект» по вертикалі |
|
Антагоніст знижує чутливість тканини до агоністи (ЕС50), але не впливає на максимальний ефект (Еmax), який може бути досягнутий при більш високій концентрації. |
Антагоніст не змінює чутливість тканини до агоністи (ЕС50), але зменшує внутрішню активність агоніста і максимальну реакцію тканини на нього (Еmax). |
|
Дія антагоніста може бути усунуто високою дозою агоніста |
Дія антагоніста не може бути усунуто високою дозою агоніста. |
|
Ефект антагоніста залежить від співвідношення доз агоніста і антагоніста |
Ефект антагоніста залежить тільки від його дози. |
Конкурентним антагоністом відносно АТ 1 рецепторів ангіотензину є лозартан, він порушує взаємодію ангіотензину II з рецепторами і сприяє зниженню артеріального тиску. Дія лозартану можна подолати, якщо ввести високу дозу ангіотензину II. Неконкурентним антагоністом по відношенню до цих же АТ 1 рецепторів є валсартан. Його дія не можна подолати навіть при введенні високих доз ангіотензину II.
Цікавим є взаємодія, яке має місце між повним і парціальним агоністами рецепторів. Якщо концентрація повного агоніста перевищує рівень парціального, то в тканини спостерігається максимальний відповідь. Якщо рівень парціального агоніста починає підвищуватися, він витісняє повний агоніст з зв'язку з рецептором і відповідь тканини починає зменшуватися від максимального для повного агоніста, до максимального для парціального агоніста (т. Е. Такого рівня, при якому він займе все рецептори).
3) Фізіологічний (непрямий) антагонізм- антагонізм, пов'язаний з впливом 2 лікарських речовин на різні рецептори (мішені) в тканинах, що призводить до взаємного ослаблення їх ефекту. Наприклад, фізіологічний антагонізм спостерігається між інсуліном і адреналіном. Інсулін активує інсулінові рецептори в результаті чого збільшується транспорт глюкози в клітину і рівень глікемії знижується. Адреналін активує b2-адренорецептори печінки, скелетних м'язів і стимулює розпад глікогену, що в підсумку призводить до підвищення рівня глюкози. Даний вид антагонізму часто використовується при наданні невідкладної допомоги пацієнтам з передозуванням інсуліну, яка привела до гіпоглікемічної коми.
44. Побічні і токсичні ефекти лікарських речовин. Тератогенна, ембріотоксичну, мутагенну дію ліків.
Побічні ефекти - ті ефекти, які виникають при застосуванні речовин в терапевтичних дозах і складають спектр їх фармакологічної дії (анальгетик морфін в терапевтичних дозах викликає ейфорію), можуть бути первинними і вторинними:
А) первинні побічні ефекти - як прямий наслідок впливу даного препарату на певний субстрат (гіпосалівація при застосуванні атропіну для усунення брадиаритмии)
Б) вторинні побічні ефекти - побічно виникають несприятливі впливу (АБ, пригнічуючи нормальну мікрофлору, можуть привести до суперінфекції)
токсичні ефекти - небажані ефекти, які проявляються у даного ЛЗ при виході з терапевтичного діапазону (передозування ЛЗ)
Вибірковість дії ЛЗ залежить від його дози. Чим вище доза препарату, тим менше виборчим він стає.
тератогенну дію- здатність ЛЗ при призначенні його вагітній жінці викликати анатомічні аномалії розвитку плода (талідомід: фокомелия, протівобластомние ЛЗ: множинні дефекти)
ембріотоксичну дію - несприятливий вплив, не пов'язане з порушенням органогенезу в перші три місяці вагітності. На більш пізніх термінах проявляється фетотоксіческое дію.
Мутагенну дію ЛЗ - пошкодження зародкової клітини і її генетичного апарату ЛЗ, що проявляється зміною генотипу потомства (адреналін, цитостатики).
Канцерогенну дію ЛЗ - здатність деяких ЛЗ індукувати канцерогенез.
45. Медичні та соціальні аспекти боротьби з лікарською залежністю, наркоманії та алкоголізмом. Поняття про токсикоманіях.
« Те, що людство в цілому буде коли-небудь обходитися без штучного раю, малоймовірно. Більшість чоловіків і жінок ведуть таку тяжку життя, яка в кращому випадку так монотонна, убога і обмежена, що бажання «піти» від неї, відключитися хоча б на кілька миттєвостей, є і завжди було одним з основнихба ний душі»(Huxley, робота« The Doors of Perception »)
1) Лікарська залежність - стан психіки і / або фізичний стан, яке є наслідком впливу на організм ЛЗ і характеризується специфічними поведінковими реакціями, важко переборним прагненням повторно приймати ЛЗ, щоб домогтися особливого психічного ефекту або уникнути дискомфорту при відсутності ЛЗ в організмі. Лікарська залежність характеризується:
А) психологічною залежністю - розвитком емоційного дистресу при припиненні прийому ЛЗ. Людина відчуває себе спустошеним, занурюється в депресію, відчуває почуття страху, тривоги, його поведінка стає агресивною. Всі ці психопатологічні симптоми виникають на тлі думок про необхідність ввести собі ЛЗ, що викликало залежність. Прагнення до прийому ЛЗ може коливатися від простого бажання до жагучої спраги прийому ЛЗ, яка поглинає всі інші потреби і перетворюється в сенс життя людини. Вважають, що психологічна залежність розвивається тоді, коли у людини з'являється свідомість того, що оптимального самопочуття він може досягти виключно завдяки введенню ЛЗ. Основа психологічної залежності - віра людини в дію ліки (в літературі описані випадки розвитку психологічної залежності до плацебо).
Б) фізичною залежністю - порушенням нормального фізіологічного стану організму, яке вимагає постійної присутності в ньому ЛЗ для підтримання стану фізіологічної рівноваги. Припинення прийому ліків викликає розвиток специфічного симптомокомплексу - абстинентного синдрому - комплексу психічних і нейровегетативних розладів у вигляді порушення функції в сторону, протилежну тій, яка характерна для дії (морфін усуває біль, пригнічує дихальний центр, звужує зіниці, викликає запор; при абстиненції у пацієнта виникають нестерпний біль, часте гучне дихання, зіниці розширені і розвивається наполеглива діарея)
В) толерантністю. Толерантність до засобів, що викликають лікарську залежність часто носить перехресний характер, т. Е. Виникає не тільки Вашого хімічній сполуці, але і до всіх структурно подібним з'єднанням. Наприклад, у пацієнтів з лікарською залежністю до морфіну толерантність виникає не тільки до нього, а й до інших опіоїдних анальгетиків.
Для розвитку лікарської залежності наявність всіх 3 критеріїв не є необхідною умовою, в таблиці 3 представлені основні види лікарської залежності і складові її компоненти.
Опіоїди, барбітурати, алкоголь викликають сильні фізичну, психологічну залежність і толерантність. Анксиолитики (діазепам, альпразолам) переважно викликають психологічну залежність.
2) Наркоманія (наркотична залежність)- це вкрай важка форма лікарської залежності, компульсивний застосування ЛЗ, що характеризується все зростаючим, непереборним потягом до введення даного ліки все збільшуючи його дози. Компульсивність потягу означає, що потреба у введенні ліки домінує у пацієнта над усіма іншими (навіть вітальними) потребами. З позицій даного визначення, потяг до морфіну - наркоманія, тоді як потяг до нікотину - лікарська залежність.
3) Пристрасть до ліків - характеризує менш інтенсивне потяг до прийому ліків, коли відмова від ліків викликає тільки відчуття легкого дискомфорту, без розвитку фізичної залежності або розгорнутої картини психологічної залежності. Т. о. пристрасть охоплює ту частину лікарської залежності, яка не підпадає під визначення наркоманії. Наприклад, згадана вище залежність від ліків до нікотину - форма пристрасті.
4) Зловживання лікарськими засобами - самовільне застосування лікарських засобів в таких дозах і такими способами, які відрізняються від прийнятих медичних або соціальних стандартів в даній культурі і в даний час. Т. о. зловживання ЛЗ охоплює тільки соціальні аспекти застосування ліків. Прикладом зловживання є використання анаболічних стероїдів в спорті або для поліпшення статури молодими чоловіками.
5) алкоголізм - хронічне зловживання алкоголю (етилового спирту), що приводить до тимчасовий до поразки ряду органів (печінки, шлунково-кишкового тракту, ЦНС, серцево-судинної системи, імунної системи) і супроводжується психико-фізичною залежністю.
6) токсикоманія - хронічне зловживання різними ЛЗ (в т. Ч. Наркотиками, алкоголем, галюциногенами), що виявляється різноманітними психічними і соматичними розладами, порушенням поведінки, соціальною деградацією.
Лікування лікарської залежності важка і невдячна задача. До сих пір не створено ефективної методики, яка б забезпечувала б успіх лікування більш ніж у 30-40% пацієнтів. Досягнення скільки-небудь помітних результатів можливо тільки при повній кооперації зусиль пацієнта, лікаря і того соціального оточення, в якому знаходиться хворий (принцип добровільності і індивідуальності). В основі сучасних методик лежать наступні принципи:
ü психотерапевтичні і трудотерапевтических методи;
ü групове лікування і реабілітація (товариства анонімних алкоголіків, наркоманів)
ü поступова або раптова відміна препарату на тлі детоксикаційної терапії
ü проведення замісної терапії (заміна наркотичного засобу повільно і длітельнодействующіе аналогами з їх подальшим скасуванням; наприклад, т. зв. програма метадонової замісної терапії у героїновий наркоманів)
ü лікування специфічними антагоністами (налоксоном і налтрексон) або сенсибилизирующими засобами (тетурамом)
ü нейрохірургічний методи кріодеструкції поясної звивини і гіпокампу
47. Види фармакотерапії. Деонтологічні проблеми фармакотерапії.
Фармакотерапія (ФТ) - сукупність методів лікування, заснованих на застосуванні ЛЗ. Основні види ФТ:
1. Етіотропна ФТ - корекція і усунення причини захворювання (АБ при інфекційних захворюваннях)
2. патогенетична ФТ - вплив на механізм розвитку хвороби (інгібітори АПФ при АГ)
3. симптоматична ФТ - усунення симптомів захворювання при неможливості впливу на його причину або патогенез (НПЗЗ при грипі)
4. замісна ФТ - застосування ЛЗ при недостатності природних БАР (інсулін при СД)
5. профілактична ФТ (вакцини, сироватки, ацетилсаліцилова кислота при ІХС)
Ставлення суспільства до ЛЗ на сучасному етапі : 1) бажання отримати вигоди без ризику 2) надія на диво, Надочікувань 3) нерозуміння ризику використання ЛЗ 4) обурення і «праведне обурення», поспішні оцінки ЛЗ 5) бажання отримання нових ЛЗ
Ставлення лікаря до ЛЗ: Терапевтичний оптимізм (надія на ЛЗ, як потужний компонент терапії), терапевтичний нігілізм (заперечення нових ЛЗ, прихильність до певних ЛЗ, недовіра новим ЛЗ)
Комплаентность (прихильність) хворого до лікування: 1) розуміння інструкцій лікаря і цілей лікування 2) прагнення точно виконувати розпорядження лікаря.
В даний час в світі порядку 100.000 ЛЗ, більш 4.000 зареєстровано в РБ, з них життєво важливих близько 300 препаратів. Вивчення фармакології допомагає не потонути в морі препаратів.
48. Основні принципи лікування та профілактика отруєнь лікарськими речовинами. Антидотная терапія.
Класифікація отруйних речовин (ОР):
1. По приналежності до певних класів хімічних сполук: барбітурати, бензодіазепіни, ціаніди.
2. За походженням: небиологической природи (кислоти, луги, солі важких металів), токсичні продукти життєдіяльності деяких МБ (ботулотоксин), рослинного походження (алколоїди, глікозиди), тваринного походження (отрути змій, бджіл)
3. За ступенем токсичності: а) надзвичайно токсичні (DL50< 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. За токсикологическому дії: а) нервово-паралітичного (бронхоспазм, ядуха) б) шкірно-резорбтивних в) общетоксические (гіпоксичні судоми, кома, паралічі) г) задушливі д) сльозоточиві і дратівливі е) психотропні (порушення психічної активності, свідомості)
5. В залежності від сфери переважного використання: промислові отрути, отрутохімікати, побутові отрути, бойові отруйні речовини, лікарські речовини.
6. В залежності від токсичності ЛЗ: список А - ЛЗ, призначення, застосування, дозування і зберігання яких в зв'язку з високою токсичністю повинні проводитися з високою обережністю. До цього ж списку відносяться ЛЗ, що викликають наркоманію; список В - ЛЗ, призначення, застосування, дозування і зберігання яких повинні проводитися з обережністю у зв'язку з можливими ускладненнями при їх застосуванні без медичного контролю.
Вибірково токсичну дію ЛЗ.
А) кардиотоксическое: серцеві глікозиди, препарати калію, антидепресанти
Б) нейротоксическое: психофармакологічні кошти, оксихинолином, аміноглікозиди
В) гепатотоксичні: тетрациклін, левоміцетин, еритроміцин, парацетамол
Г) нефротоксичний: ванкоміцин, аміноглікозиди, сульфаніламіди
Д) гастроентеротоксіческое: стероїдні протизапальні засоби, нестероїдні протизапальні засоби, резерпін
Е) гематотоксичних: цитостатики, левоміцетин, сульфаніламіди, нітрати, нітрити
Ж) пневмотоксичних
Токсікокінетіка - вивчає всмоктування, розподіл, метаболізм і виведення ЛЗ, прийнятих в токсичних дозах.
Надходження отруйних речовин в організм можливо а) ентерально б) парентерально. Швидкість і повнота всмоктування відображає швидкість розвитку токсичного ефекту і його вираженість.
Розподіл в організмі: Vd \u003d D / Cmax - дійсний обсяг, в якому розподіляється в організмі отруйну речовину. Vd\u003e 5-10 л / кг - ОВ важко допустимо для його видалення (антидепресанти, фенотіазини). Vd< 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Передозування - зміна фармакокінетичних процесів: розчинності, зв'язку з білками, метаболізму ® значне підвищення вільної фракції ЛЗ ® токсичні ефект.
Кінетика першого порядку при збільшенні концентрації ЛЗ переходить в кінетику нульового порядку.
Токсигенних стадія - дезінтоксикаційна терапія, соматогенна стадія - симптоматична терапія.
токсікодінамікі . Основні механізми токсичної дії:
А) медіаторний: прямий (по типу конкурентної блокади - ФОС, психоміметиками) і непрямий (активатори або інгібітори ферментів)
Б) взаємодія з биомолекулами і внутрішньоклітинними структурами (гемолітичні речовини)
В) метаболізм за типом летального синтезу (етиловий спирт, тиофос)
Г) ферментний (отрути змій та ін.)
Види дії: місцеве, рефлекторне, резорбтивное.
Класифікація отруєнь:
1. Етіопатогенетична:
а) випадкове (самолікування, помилковий прийом)
б) навмисне (з метою самогубства, вбивства, розвитку у потерпілого безпорадного стану)
2. Клінічна:
а) в залежності від швидкості розвитку отруєння: гостре (надходження одноразово або з коротким інтервалом часу токсичної дози речовини), підгострий (уповільнений розвиток клінічної картини після одноразового прийому), хронічне
б) в залежності від прояву основного синдрому: поразка ССС, ураження ДС і ін.
в) в залежності від тяжкості стану хворого: легкої, середньої, важкої, вкрай важкої
3. Нозологічна: враховує назва ЛЗ, назва групи речовин
Загальний механізм смерті при отруєнні:
А) ураження ССС:
1) зниження артеріального тиску, гіповолемія периферичних судин, колапс, браді - або тахікардія (трициклічніантидепресанти, бета-блокатори, блокатори кальцієвих каналів)
2) аритмії (шлуночкова тахікардія, фібриляція - трициклічніантидепресанти, теофілін, амфетамін)
Б) поразку ЦНС: ступор, кома ® пригнічення дихання (наркотики, барбітурати, алкоголь, гипно-седативні ЛЗ)
В) судоми, м'язова гіперреактивність і ригідність ® гіпертермія, міоглобінурія, ниркова недостатність, гіперкаліємія
Токсикологічна тріада:
1) тривалість застосування, доза і речовина ® анамнез.
2) оцінка стану свідомості за симптомами: дихання, артеріальний тиск, температура тіла
3) лабораторні дані
Основні принципи лікування:
I. Перша невідкладна допомога: Штучне дихання, масаж серця, протишокова терапія, контроль за водно-сольовим балансом
II. Затримка всмоктування і видалення з організму не всмоктаної ОВ:
Мета: припинити контакт з ОВ
1. Парентеральний шлях:
а) через легені:
1) припинити інгаляцію
2) подразнюючі речовини (нашатирний спирт, формальдегід) ® закріпити активні рухи, зігріти, дати кисень і піногасники (у нашатирного спирту пеногаситель оцет, а у формальдегіду - розбавлений розчин нашатирного спирту)
б) через шкіру: змити великою кількістю теплої води з милом або миючим засобом, специфічні протиотрути, нейтралізація і припинення дії ОР на шкіру (ФОС: обмивають водою, видаляють за допомогою 10-15% нашатирного спирту або 5-6% розчину бікарбонату натрію з водою; фенолкрезол: рослинне масло або етиленгліколь, але не можна вазелінове масло, KMNO4: 0,5-1% -ий розчин аскорбінової кислоти або рівні об'єми 3% перекису водню і 3% розчину оцтової кислоти, CCl4, скипидар, бензин: тепла мильна вода )
в) при ін'єкції в кінцівку: джгут вище місця ін'єкції
г) при попаданні в очі: промивання теплим фізрозчином або молоком протягом 10-20 хвилин, закапати місцевий анестетик; при попаданні кислот і лугів не можна нейтралізувати. Обов'язкова консультація офтальмолога.
2. Ентеральний шлях: звільнити шлунок від ОВ, прискорити пасаж
а) видалення ОВ:
1) попередньо прийом води. Не можна приймати молоко (виняток - їдкі отруйні речовини) і етанол (виняток -метанол).
2) блювота - показана переважно при отруєнні великими таблетками або капсулами, які не можуть пройти через зонд. Можна спровокувати рефлекторно або блювотними засобами (NaCl: 1 столова ложка на 1 склянку води; сироп іпекакуани: дорослим 2 столові ложки, дітям 2 чайні ложки; гірчиця: 1-2 чайні ложки на склянку води; апоморфин: 5-10 мг / кг підшкірно , крім дітей до 5 років). Не можна викликати блювоту після прийому: органічних розчинників - небезпека інгаляцій, миючих засобів - піноутворення, судомних ОВ - небезпека аспірації, їдких речовин - пошкодження стравоходу)
3) зондове промивання шлунка - є екстреним і обов'язковим заходом. Шлунок промивають, якщо з моменту отруєння минуло не більше 4-6 годин, іноді до 10 годин; при отруєнні ацетилсаліциловою кислотою - через 24 години. Попередньо интубируют пацієнта трубкою з раздувной манжетою: в коматозному стані при відсутності кашльового і ларингеального рефлексу. Шлунок промивають водою або фізіологічним розчином 30 ° С, час процедури 4 години і більше. В кінці промивання - активоване вугілля і сульфат натрію.
б) зниження всмоктування з шлунково-кишкового тракту: активоване вугілля всередину після спорожнення шлунка + сульфат натрію або магнію. Особливості заходів щодо зниження всмоктуваності:
1) органічні розчинники: не можна викликати блювоту, промивання шлунка після інтубації, активоване вугілля + вазелінове масло
2) миючі засоби: не можна викликати блювоту і промивати шлунок, необхідно давати багато води + піногасники (симетикон)
3) кислоти і луги: не можна викликати блювоту, промивання шлунка через зонд, змащений олією після введення наркотичного анальгетика - єдине показання для дачі молока. При отруєнні кислотами - антациди, при отруєнні лугу - лимонна або оцтова кислоти.
III. Видалення з організму всмоктався ОВ
а) форсований діурез (умови: достатній нирковий кровообіг і клубочкова фільтрація; за 24 години влити-вилити 20-25 літрів)
б) перитонеальний гемодіаліз
в) гемосорбция
г) обмінне переливання крові
д) форсована гіпервентиляція
IV. Симптоматична терапія функціональних порушень.
Антидоти: 1) токсікотропние - зв'язуючі, нейтралізують і попереджуючі всмоктування ОВ: що діють за принципом активованого вугілля, Що діють по хімічному принципу (унітіол, пеніциламін, пентацин)
2) токсікокінетіческіе - прискорюють біотрансформацію ОВ (трімедоксіма бромід, натрію тіосульфат, етанол, АТ)
3) фармакологічні - атропін, налоксон
4) імунологічні протиотрути
Унітіол, сукцімер - зв'язує важкі метали, металоїди, серцеві глікозиди. Есмолол пов'язує теофілін, кофеїн. Кальцію тринатрію пентотат - утворює комплекси з двох і тривалентними металами.
49. Рецепт і його структура. Загальні правила виписування рецепта. Державна регламентація правил виписування і відпуску ліків.
рецепт - це письмове звернення лікаря до фармацевта з вимогою відпустити ліки в певній формі і дозуванні із зазначенням способу його застосування
У рецепті розрізняють наступні частини:
1. Inscriptio - заголовок, напис. Тут пишеться дата видачі рецепта, прізвище, ініціали та вік хворого, прізвище та ініціали лікаря.
2. Invocatio - звернення до фармацевта. Виражається словом "Recipe" (візьми) або скороченим позначенням (Rp.)
3. Designatio materiarum - позначення або найменування лікарських препаратів із зазначенням їх доз. В складному рецепті перерахування лікарських речовин робиться в певній послідовності. Першим вказується основне лікарська речовина (basis). Потім пишуть допоміжні речовини (adjuvans). Після цього вказують інградієнти, що виправляють смак, запах, колір ліки (corrigens). Останніми пишуться речовини, які надають ліків певну лікарську форму (constituens).
4. Subscriptio - припис (вказівка) фармацевту. Тут вказується лікарська форма, фармацевтичні операції, необхідні для її виготовлення, кількість відпускаються доз ліки.
5. Signatura - вказівка \u200b\u200bхворому про те, як користуватися ліками.
6. Subscriptio medici - підпис лікаря, який виписав рецепт, його особиста печатка.
Звернення лікаря до фармацевта, назва ліків, що входять до складу рецепта, назва лікарської форми і характер фармацевтичних операцій пишуться на латинською мовою. Назва ліків, ботанічні назви рослин пишуться з великої літери. Припис хворому пишеться російською або національною мовами.
Загальні правила виписування рецепта:
1. Рецепт пишеться на спеціальній формі в залежності від виписується ЛЗ чітким почерком, чорнилом або кульковою ручкою без виправлень.
2. У рецепті вказується число, місяць, рік, прізвище, ім'я, по батькові та вік хворого, прізвище, ім'я та по батькові лікаря. Потім йде текст рецепта, де перераховуються входять в рецепт назви речовин в родовому відмінку із зазначенням їх кількості
3. Одиниця маси в рецептах - грам або ОД.
4. Якщо перевищують максимальну дозу отруйних і сильнодіючих речовин, її підтверджують прописом
5. Рецепт підтверджується підписом і особистою печаткою лікаря
У РБ діє Державна регламентація правил виписування і відпуску ліків.
50. Правила виписування отруйних, наркотичних і сильнодіючих засобів.
До списку А віднесені ЛЗ, призначення, застосування, дозування і зберігання яких в зв'язку з високою токсичністю повинні проводитися з високою обережністю. До цього ж списку відносяться ЛЗ, що викликають наркоманію.
До списку В віднесені ЛЗ, призначення, застосування, дозування і зберігання яких повинні проводитися з обережністю у зв'язку з можливими ускладненнями при їх застосуванні без медичного контролю.
Для отруйних і сильнодіючих лікарських засобів встановлені максимальні вищі разові і добові дози. Ці дози розраховані на дорослих людей, які досягли 25 років. При перерахунку доз для людей старше 60 років враховується вікова чутливість до різних груп ЛЗ. Дози препаратів, що пригнічують ЦНС, а також серцевих глікозидів та діуретиків зменшуються на 50%, дози інших отруйних і сильнодіючих лікарських засобів знижуються до 2/3 від дози дорослого. Дози АБ, сульфаніламідів і вітамінів зазвичай однакові для всіх вікових груп, Починаючи з 25 років.
1. Наркотичні лікарські засоби (список А) виписуються на рецептурному бланку форми 2. Один бланк - одні ліки. Повинні бути: підпис і печатку лікуючого лікаря, підпис головного лікаря ЛПУ, кругла печатка ЛПЗ.
2. Отруйні лікарські засоби (список А), сильнодіючі (список Б) виписуються на рецептурному бланку форми 1. Чи повинні бути підпис і особиста печатка лікаря, друк ЛПУ.
51. Лікарські засоби, що знаходяться під контролем. Ліки, заборонені для виписування в рецептах.
Під контролем знаходяться наркотичні, отруйні та сильнодіючі лікарські засоби (див. Ст. 20)
А) ЛЗ, які не зареєстровані в РБ і не дозволені до офіційного застосування
Б) ЛЗ на прохання хворих і їх родичів без огляду хворого і встановлення діагнозу
В) рецепти на наркотичні ЛЗ для ін'єкцій, ефір наркозний, хлоретил, пентамін, фторотан, натрію оксибутират в ампулах, літію оксибутират, барію сульфат для рентгеноскопії.
52. Фармакокінетичні моделі (однокамерна і двокамерна), кількісні закони всмоктування та елімінації ліків.
![]() Однокамерна модель.
Однокамерна модель.
Весь організм - єдиний однорідний контейнер. допущення:
1) встановлюється швидке динамічний розвиток між вмістом препарату в кров'яному руслі і його концентрацією в Екстраваскулярний тканинах
2) ЛЗ швидко і рівномірно розподіляється по всьому об'єму крові
3) Виведення ЛЗ підпорядковується кінетиці першого порядку: швидкість зменшення вмісту препарату в крові пропорційна його концентрації
Якщо механізми для усунення лікарського засобу (біотрансформація в печінці, ниркова секреція) не насичені при введенні терапевтичної дози, логнормального графік зміни плазмової концентрації в часі буде лине.
нахил логнормального осі - Kel, де Kel - постійна швидкості елімінації і має розмірність час-1. Значення С0 виходить екстраполяцією графіка до перетину з віссю ординат. Плазмова концентрація ЛВ (Ct) в будь-який час t після введення в організм становить:
Ln Ct \u003d Ln C0 - kt. Константа елімінації Kel, Vd, і загальний кліренс (CL) пов'язані виразом: CL \u003d k × Vd
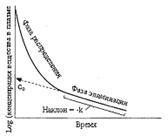 Двокамерна модель.
Двокамерна модель.
Часто після надходження ЛЗ в організм не вдається швидко досягти рівноваги між вмістом ЛЗ в крові і його концентрацією в Екстраваскулярний рідини. Тоді вважають, що в сукупності тканин і біологічних рідин організму можна виділити дві камери, які відрізняються ступенем доступності для проникнення ЛЗ. До центральної камері відноситься кров (часто з інтенсивно перфузіруемих органами - печінку, нирки), до периферичної - інтерстиціальна рідина внутрішніх органів і тканин.
Результуючий графік показує початкову Фазу розподілу (Час, необхідний ЛЗ для досягнення рівноважного стану між центральної і периферичної камерами і наступну за нею повільну фазу елімінаціїПершого порядку.
Значення С0, виходить екстраполяцією фази елімінації до перетину з віссю ординат. С0 використовується для обчислення об'єму розподілу та константи елімінації. Формули для розрахунку Сt і Cl, наведені для однокамерною моделі, також застосовуються протягом фази елімінації для препаратів, які задовольняють умовам моделі з двома камерами.
53. Селективність і специфічність дії ліків. Терапевтичні, побічні та токсичні ефекти ліків, їх природа з позицій концепції рецепторів. Терапевтична стратегія боротьби з побічними і токсичними ефектами ліків.
специфічність - це коли ЛЗ зв'язується зі строго специфічним йому типом рецептора.
селективність - це коли ЛЗ здатне зв'язуватися з одним або декількома типами рецепторів більш точно, ніж з іншими.
Більш переважно використовувати термін селективність, т. К. Малоймовірно, що будь-яка молекула ЛЗ може зв'язатися тільки з одним типом рецепторних молекул, оскільки число потенційних рецепторів у кожного пацієнта має астрономічне значення.
терапевтична дія - основний бажаний фармакологічний ефект, очікуваний від даного фармакологічного препарату.
Побічні ефекти- ті ефекти, які виникають при застосуванні речовин в терапевтичних дозах і складають спектр їх фармакологічної дії.
токсичні ефекти - небажані ефекти, які проявляються у даного ЛЗ при виході з терапевтичного діапазону.
Зв'язки терапевтичного і токсичної ефектів ЛЗ на основі аналізу рецепторно-ефекторних механізмів:
1) терапевтичний і токсичний ефекти, опосередковувані одним і тим же рецепторно-ефекторних механізмом (празозин діє як альфа-селективний антагоніст на рецептори ГМК судин і має гіпотензивну дію при есенціальнійгіпертензії, але при його великій дозі у хворого може виникнути постуральна гіпотензія)
2) терапевтичний і токсичний ефекти, опосередковувані ідентичними рецепторами, але різними тканинами або різними ефекторними шляхами (серцеві глікозиди використовують для збільшення скорочувальної здатності міокарда, в той же час вони порушують функцію шлунково-кишкового тракту, зору за рахунок блокади Na + / K + -АТФази клітинної мембрани)
3) терапевтичний і токсичний ефекти, опосредуемий різними типами рецепторів (наприклад, норадреналін надає гіпертензивну дію через a1-Ар, але при цьому викликає тахікардію через b1-Ар)
Терапевтична стратегія боротьби з терапевтичними і побічними ефектами ЛЗ:
1. ЛЗ завжди слід вводити у найменшій дозі, яка викликає прийнятний терапевтичний ефект
2. Зниження дози одного ЛЗ за рахунок призначення іншого ЛЗ з подібним дією, але через інші рецептори і з іншим профілем токсичності.
3. Селективність дії ЛЗ може бути збільшена шляхом управління концентрацією ЛЗ в районі рецепторів різних відділів організму (місцеве застосування ЛЗ - інгаляційне застосування сальбутамолу при бронхіальній астмі)
